Molekül
Photoschaltbarer Tumorwirkstoff bewährt sich im Labor
Photoschaltbare Wirkstoffe könnten die Nebenwirkungen einer Chemotherapie verringern. Bisher sind photodynamische Therapien auf Sauerstoff im Gewebe angewiesen. Doch in bösartigen, schnell wachsenden Tumoren ist Sauerstoff knapp. Eine Forschergruppe des KIT und der Universität Kiew hat nun mit einem photoschaltbaren Molekül die Grundlage für eine Sauerstoff-unabhängige Methode entwickelt.
Zur photodynamischen Therapie (PDT) in der Medizin wird üblicherweise eine Substanz eingesetzt, die auf Licht reagiert und den Sauerstoff im Gewebe in aggressive Radikale verwandelt. Diese reaktiven Stoffe sind toxisch und schädigen die umliegenden Zellen, sodass etwa Tumore abgebaut werden können. Da jedoch viele Tumore durch ihr schnelles Wachstum einen hohen Sauerstoffverbrauch haben, verringert dies die verfügbare Konzentration im Gewebe, was eine konventionelle PDT erschweren kann.
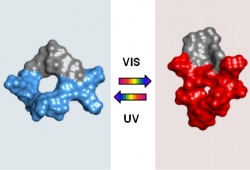
Forscherinnen und Forscher des KIT und der Universität Kiew entwickelten nun ein neues photoschaltbares Molekül, das eine sauerstoffunabhängige PDT ermöglicht. Die Wirkung des Moleküls GS-DProSw lässt sich vor der Therapie durch ultraviolettes Licht „ausschalten“. Erst nach Verabreichung wird es durch sichtbares Licht gezielt im Tumorgewebe „angeschaltet“, um ausschließlich dort die gewebeschädigende Wirkung zu entfalten. „Die umliegenden Organe bleiben dabei im Dunkeln und werden so vom aktiven Wirkstoff verschont“, erklärt Anne S. Ulrich, Professorin für Biochemie und Direktorin am Institut für Biologische Grenzflächen des KIT. „Dadurch lassen sich die Nebenwirkungen deutlich verringern.“
Erstmals getestet wurde das neue Konzept nun an Tiermodellen. Einmal täglich wurde das photoschaltbare Molekül GS-DProSw verabreicht, und die Tumorgeschwüre wurden anschließend für je zwanzig Minuten mit sichtbarem Licht lokal bestrahlt. Nach zehn Tagen PDT-Behandlung waren die Tumore deutlich geschrumpft gegenüber den Vergleichsgruppen, die nicht mit Licht behandelt wurden.
Um bei einer PDT eine sauerstoffunabhängige Reaktion hervorzurufen, muss das eingesetzte Molekül zytotoxisch sein – also unabhängig von anderen Reaktionspartnern das Tumorgewebe direkt angreifen. Ein geeignetes Molekül mit zytotoxischen Eigenschaften gegen Tumore ist das Biomolekül Gramicidin S (GS), ein natürliches Antibiotikum. Um zu vermeiden, dass es in gesundem Gewebe Schaden anrichtet, baute das Forschungsteam ein photoschaltbares Diarylethen-Segment in seine ringförmige Struktur ein. Dadurch lässt sich nun die Gestalt des GS-DProSw Moleküls mit Hilfe von Licht zwischen zwei Zuständen hin- und herschalten: Der Wirkstoff kann im inaktiven Zustand verabreicht werden und wird erst durch gezielte Lichtbestrahlung am gewünschten Ort aktiviert. Dort greift er das umliegende Tumorgewebe an und benötigt dafür gegenüber der herkömmlichen PDT keinen Sauerstoff.
„Mit diesem ersten Funktionsnachweis sind wir in der Grundlagenforschung für Tumorwirkstoffe einen wichtigen Schritt vorangekommen“, erklärt Ulrich. „Es ist aber noch ein weiter Weg: Um diese Art der photoschaltbaren Moleküle für eine photodynamische Therapie am Menschen zuverlässig nutzbar zu machen, sind noch viele weitere Studien zusammen mit unseren Partnern in Kiew erforderlich.“
Publikation:
Oleg Babii, Sergii Afonin, Liudmyla V. Garmanchuk, Viktoria V. Nikulina, Tetiana V. Nikolaienko, Olha V. Storozhuk, Dmytro V. Shelest, Olga I. Dasyukevich, Liudmyla I. Ostapchenko, Volodymyr Iurchenko, Sergey Zozulya, Anne S. Ulrich and Igor V. Komarov: Direct photocontrol of peptidomimetics: an alternative to oxygen dependent photodynamic cancer therapy. Angewandte Chemie (2016). DOI: 10.1002/ange.201600506
Quelle: Karlsruher Institut für Technologie
07.04.2016