News • Knochenmarkkrebs
Multiples Myelom: Warum der Krebs wiederkehrt
Selbst nach einer zunächst erfolgreichen Behandlung kehrt ein Multiples Myelom, der häufigste Knochenmarkkrebs in Deutschland, fast immer zurück. Die Ursachen für die Therapieresistenz, wie genetische Veränderungen, und die damit verbundene Rückkehr der Erkrankung sind jedoch nur in wenigen Fällen bekannt.
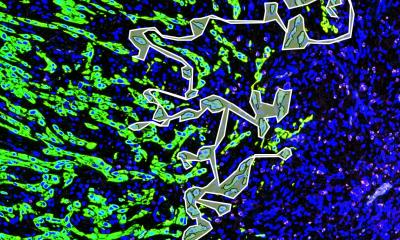
© Jan Krönke l Charité
Wie ein Forschungsteam der Charité – Universitätsmedizin Berlin, des Berlin Institute of Health in der Charité (BIH) und des Max-Delbrück-Centrums für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC) jetzt zeigt, macht die vermehrte Produktion eines bestimmten Proteins den Krebs unempfindlich gegen die Therapie. Die im Fachmagazin Nature Communications veröffentlichten Ergebnisse eröffnen neue Behandlungsperspektiven.
Das Multiple Myelom ist eine Krebserkrankung, bei der Immunzellen im Knochenmark, die Plasmazellen, entarten. Das kann zur Schwächung des Immunsystems, Nierenversagen und starkem Knochenabbau und daraus folgenden Knochenbrüchen führen. Die durchschnittliche Überlebensdauer der Betroffenen hat sich mittlerweile durch neue Behandlungsmöglichkeiten deutlich verbessert. Beispielsweise drängt eine Therapie mit den Medikamenten Lenalidomid und Pomalidomid den Krebs häufig erfolgreich zurück. Allerdings wird der Tumor in fast allen Fällen unempfindlich gegen die Substanzen, entwickelt also eine Therapieresistenz. Trotz Behandlung fängt er wieder an zu wachsen, was mit einer schlechten Prognose für die Patienten einhergeht.
Mit zukunftsweisenden Methoden der Proteomanalyse hat ein interdisziplinäres Berliner Forschungsteam jetzt einen bisher unbekannten Mechanismus entschlüsselt, der einen solchen Rückfall verursachen kann. „Wir konnten zeigen, dass der Zellteilungsregulator CDK6 von den Krebszellen zum Zeitpunkt der Therapieresistenz übermäßig stark produziert wird“, erklärt Prof. Dr. Jan Krönke von der Medizinischen Klinik mit Schwerpunkt Hämatologie, Onkologie und Tumorimmunologie am Charité Campus Benjamin Franklin und einer der beiden Leiter der Studie. „Auf Basis unserer Daten gehen wir davon aus, dass die Hemmung von CDK6 ein neuer Ansatz für die Behandlung eines zurückgekehrten Multiplen Myeloms sein könnte.“
Beim Multiplen Myelom wurden bislang trotz umfangreicher DNA-Sequenzierung nur selten Veränderungen auf der genetischen Ebene, wie beispielsweise Mutationen oder Genverluste, gefunden, die die Therapieresistenz erklären. „Das deutet darauf hin, dass es in den Krebszellen auf anderer Ebene Veränderungen geben muss, die den Rückfall erklären“, sagt der zweite Studienleiter Dr. Philipp Mertins. Der MDC-Forscher leitet die Technologieplattform „Proteomics“ von MDC und BIH. „Zum Beispiel können die Gene der Krebszellen auch auf Proteinebene unterschiedlich reguliert sein. Das ist ein Effekt, den wir hier für das Protein CDK6 beobachtet haben.“ Um herauszufinden, ob solche Veränderungen auf Proteinebene den Tumor resistent gegen die Therapie machen, nutzte das Forschungsteam neueste Entwicklungen der Massenspektrometrie-Technologie. So gelang es, in Tumorproben, die bei Patienten vor und nach dem Rückfall entnommen wurden, mehr als 6.000 Proteine zu quantifizieren.
Dieser Artikel könnte Sie auch interessieren

News • Molekulare Prozesse
Krebsforschung: Tiefer Einblick in Tumore
Forschende haben Methoden entwickelt, um Proteine in fixierten Proben von Krebsgeweben umfassend zu analysieren. Damit lassen sich neue Erkenntnisse über die Krankheitsabläufe bei verschiedenen Krebsarten gewinnen.
Die Forschenden stellten auf diese Weise für eine ganze Reihe von Proteinen fest, dass sie in den Krebszellen nach dem Rückfall in größeren oder auch kleineren Mengen vorlagen als vor der Therapie. Ein Großteil dieser Effekte ließ sich jedoch durch statistische und bioinformatische Analysen auf ein einzelnes Protein zurückführen: CDK6. Die Abkürzung steht für Cyclin Dependent Kinase 6 und bezeichnet ein Enzym, das in der Zelle den Eintritt in die Zellteilung reguliert. Dass CDK6 eine zentrale Rolle in der Entwicklung einer Therapieresistenz beim Multiplen Myelom spielt, wies das Forschungsteam zunächst in der Zellkultur nach. „Als wir die Menge von CDK6 in kultivierten Myelomzellen künstlich erhöhten, wurden diese Zellen unempfindlich gegen die Wirkstoffe Lenalidomid und Pomalidomid“, erläutert Dora Ng, Wissenschaftlerin an der Medizinischen Klinik mit Schwerpunkt Hämatologie, Onkologie und Tumorimmunologie am Charité Campus Benjamin Franklin und Erstautorin der Studie. „Gaben wir jedoch zusätzlich einen CDK6-Hemmer hinzu, zeigten die Medikamente wieder Wirkung und die Krebszellen gingen zugrunde. Das zeigt, dass sich die Resistenz der Myelomzellen gegen die Therapie zumindest teilweise aufheben lässt, indem man CDK6 hemmt.“
Diesen Effekt konnte das Team ebenso im Tiermodell bestätigen: Wurde neben Pomalidomid auch ein CDK6-Hemmer verabreicht, waren die Überlebenschancen bei einer solchen Erkrankung deutlich besser. „Diese Daten weisen darauf hin, dass auch Patientinnen und Patienten mit einem therapieresistenten Multiplen Myelom von einer zusätzlichen CDK6-Hemmung profitieren könnten“, sagt Prof. Krönke, der durch das Emmy Noether-Programm der Deutschen Forschungsgemeinschaft (DFG) gefördert und auch Wissenschaftler des Deutschen Konsortiums für Translationale Krebsforschung (DKTK) am Partnerstandort Berlin ist: „Um diese Annahme zu überprüfen, sind nun weitere Studien nötig. Dabei ist von Vorteil, dass einige CDK6-Hemmer bereits für die Behandlung von Brustkrebs zugelassen sind.“
Dr. Evelyn Ramberger, zweite Erstautorin der Studie, hat die Proteinanalysen für das Projekt durchgeführt. Die Postdoktorandin an der Charité und Technologieplattform „Proteomics“ von MDC und BIH ist von dem hohen Nutzen der Methode für die Krebsforschung überzeugt: „In Zukunft wollen wir den neuen Ansatz moderner, umfassender Proteinanalysen an Tumorgewebe beim Multiplen Myelom und weiteren Krebserkrankungen zur Aufdeckung therapeutischer Ziele und Biomarker für die personalisierte Krebsmedizin weiterverfolgen“, sagt sie.
Quelle: Charité – Universitätsmedizin Berlin
28.02.2022