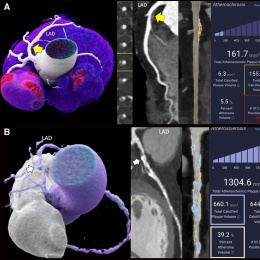
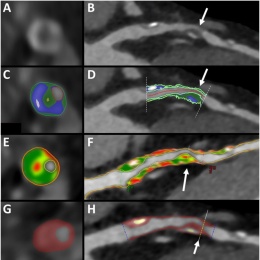
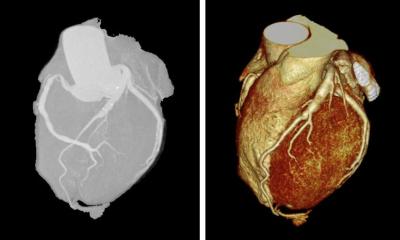
Bildquellen: links: Slivnick JA, Hawkes W, Oliveira J et al., European Heart Journal 2025 (CC BY 4.0); Mitte: Feuchtner GM, Lacaita PG, Bax JJ et al.; Circulation: Cardiovascular Imaging 2025 (CC BY 4.0); rechts: Bhuva AN, Bai W, Lau C et al.; Circulation: Cardiovascular Imaging 2019 (CC BY-NC-ND 4.0)
Artikel • Experten liefern auf dem ESC 2025 Einblicke
Schneller und smarter: Neue Technik für die Zukunft der Herz-Bildgebung
Die Herzbildgebung schreitet voran, und neue Techniken eröffnen Kardiologen, die sie zu nutzen wissen, neue Einblicke in die Geheimnisse des Herzens. Auf dem ESC-Kongress 2025 in Madrid stellten vier Experten die neuesten Entwicklungen für verschiedene Modalitäten vor. Von der KI-gestützten Ultraschallbildgebung und beschleunigten MRT-Protokollen bis hin zu fortschrittlichen Prognosetools für die CT- und nuklearmedizinische Bildgebung bieten diese neuen Ansätze einen vielversprechenden Ausblick darauf, was die nächste Generation der Herzbildgebung leisten kann.
Artikel: Wolfgang Behrends
Zum Auftakt der Expertenrunde erklärte Dr. William A. Zoghbi vom Houston Methodist DeBakey Heart & Vascular Center in den USA, wie künstliche Intelligenz dazu beitragen kann, die für ihre steile Lernkurve bekannte Ultraschallbildgebung zu vereinfachen. Dabei hilft ein automatisierter Gradmesser für die Bildqualität nach dem Vorbild von WLAN-Empfangsbalken dem Schaller bei der Erstellung relevanter Aufnahmen, etwa bei rheumatischen Herzerkrankungen.1 „Diese Technik hilft vor allem unerfahrenen Sonografen, und kann dazu beitragen, die Verfügbarkeit der Bildgebung in ländlichen und unterversorgten Gebieten zu erhöhen“, prognostizierte er. Der Ansatz lasse sich nicht nur für rheumatische Herzerkrankungen nutzen, sondern auch für Herzinsuffizienz und weitere Vorsorgeuntersuchungen.
KI ist keine Bedrohung, sondern eine Chance für die Echokardiographie, zu wachsen und mehr Einfluss zu gewinnen
William A. Zoghbi
Auch für versierte Untersucher eröffnen sich neue Vorteile, beispielsweise durch KI-gestützte Quantifizierung von Herzvolumina und automatisierte Befundung.2 Auch wenn die KI-generierten Inhalte weiterhin von Menschen verifiziert werden müssten, verringere sich dadurch die Untersuchungsdauer erheblich, betonte Dr. Zoghbi. Auf dieser Grundlage seien Algorithmen inzwischen sogar in der Lage, bestimmte Erkrankungen zu erkennen und zu interpretieren. Als Beispiel nannte er ein kürzlich vorgestelltes KI-Modell, das anhand eines einzigen Videos eine kardiale Amyloidose erkennen kann.3
Dieser Artikel könnte Sie auch interessieren
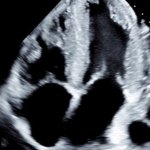
News • Neural network screening tool
AI-enhanced ultrasound early detects cardiac amyloidosis
A neural network AI has been trained to detect cardiac amyloidosis from a single echocardiogram video of the heart's apical four-chamber view and differentiate it from similar heart conditions.
Bei der Verlagerung von der Detektion zur Prognose sollten Kardiologen die Fähigkeit der Technologie nutzen, Daten aus mehreren Quellen für die Risikobewertung zu extrapolieren, riet der Experte: „Das ist es, was die Patienten wirklich interessiert.“4
Wird die Echokardiographie also durch die neue Technologie florieren oder unter ihrem Einfluss leiden? Für Dr. Zoghbi ist die Antwort klar: „KI ist keine Bedrohung, sondern eine Chance für die Echokardiographie, zu wachsen und mehr Einfluss zu gewinnen“, lautete sein Fazit.
Kardio-CT: weniger Strahlenbelastung und Artefakte, mehr Einsatzbereiche
Diese Begeisterung teilte auch Prof. Dr. Dr. Christoph Gräni. Als Fürsprecher der Computertomografie war es ihm ein Leichtes, die vielen Fortschritte aufzuzählen, die diese Modalität – die ohnehin schon eine starke Position in der Herzbildgebung einnahm – in den letzten Jahren erfahren hat: Zusätzlich zu ihrer hohen Aufnahmegeschwindigkeit hat sich durch neue Technologien auch die Bildqualität erheblich verbessert, während die Strahlenbelastung auf ein Minimum reduziert werden konnte. Vor allem von der prognostischen Aussagekraft zeigte sich der Leiter der kardiologischen Bildgebung am Universitätsspital Bern beeindruckt: „Mit einer normalen Koronar-CT können wir dem Patienten eine Garantie geben, dass er in den nächsten zehn Jahren keinen Myokardinfarkt erleiden wird – das ist eine wirklich starke Aussage.“5
Auf der Hardware-Ebene hat vor allem die Einführung der Photon-Counting-CT neue diagnostische Möglichkeiten eröffnet. Die neue Technologie erhöht die Auflösung und reduziert gleichzeitig Bildartefakte wie Blooming, erklärte Gräni. Dadurch lassen sich neue Erkenntnisse bei Patienten mit Kalzifikationen der Herzkranzgefäße oder Stents gewinnen.6
Dieser Artikel könnte Sie auch interessieren
Artikel • Herzbildgebung
Photon Counting CT: Mehrwert auch für die Kardiologie
Hochauflösende Aufnahmen, Reduktion von Artefakten und Strahlendosis, Potential für die funktionale Bildgebung – Photon Counting CT bringt einige Eigenschaften mit, die auch für die Kardiologie hochinteressant sind. Prof. Dr. Christopher Schlett spricht über die Vorteile der neuen Modalität und warum die Technik das Zeug dazu hat, Radiologen und Kardiologen näher zusammenzubringen.
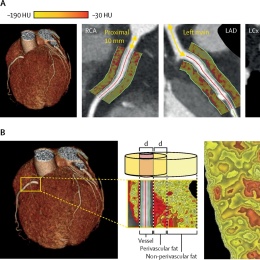
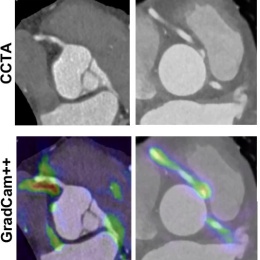
„Vor allem die Scannertechnologie hat sich weiterentwickelt, aber auch die Nachbearbeitung“, sagte er. „Und dieser gesamte Prozess wird durch künstliche Intelligenz beschleunigt und verbessert.“ Unter den vielversprechenden CT-Anwendungen für KI hob der Experte Lösungen hervor, die die Variabilität zwischen einzelnen Untersuchern reduzieren7, das prognostische Potenzial koronarer Plaques und Entzündungsaktivität im Fettgewebe (fat attenuation index; FAI) nutzen8,9,10, und seltene Krankheitsbilder wie Anomalien der Koronararterien erkennen.11
Eine weitere spannende Entwicklung sieht der Experte in der Simulation von Behandlungsergebnissen: Während frühere Ansätze bereits datengesteuerte digitale Zwillinge implementierten, konzentriert sich neuere Forschung auf die Herstellung 3D-gedruckter physischer Zwillinge für hämodynamische Belastungstests.12 „Man erstellt einen 3D-Druck aus dem CT-Scan und wendet ihn dann in einem Flow-Loop an“, erklärte Gräni. Er prognostizierte, dass diese Zwillingsmodelle Kardiologen in Zukunft dabei helfen werden, koronare Obstruktionen und Rupturen vorherzusagen, das Lebenszeitmanagement von Herzimplantaten zu verbessern und vieles mehr. Wie weit in der Zukunft? Der Experte zeigte sich überzeugt, dass „diese patientenspezifischen digitalen und physischen Zwillingsmodelle sicherlich schon sehr bald verfügbar sein werden“.
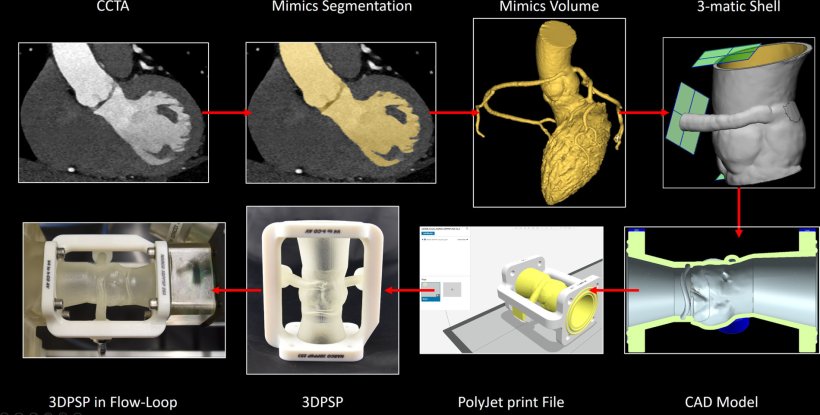
Bildquelle: Illi J, Stark AW, Ilic M et al.; JACC: Case Reports 2024 (CC BY 4.0)
CMR: Fortschritte bei Geschwindigkeit und Nutzerfreundlichkeit
Bleibt die kardiale Magnetresonanztomographie (CMR) angesichts dieser starken Konkurrenz auf der Strecke? Dr. Chiara Bucciarelli-Ducci hegte in dieser Hinsicht keinerlei Bedenken, denn ihr zufolge ist diese Methode weder veraltet noch langsam: „CMR kann schnell sein, und sie ist schnell, wenn man weiß, was man tut“13, erklärte die Kardiologin vom Royal Brompton and Harefield Hospital, UK. Zudem liefere sie klinisch relevante Informationen, betonte sie. Mit den richtigen Protokollen seien in weniger als 20 Minuten umfassende Stress-CMR-Untersuchungen zur Diagnose ischämischer Herzerkrankungen zuverlässig möglich.14 Mit neuen Features wie der Ein-Klick- Bildauswertung15 und KI-gestützter Auto-Konturierung16 stehe Kardiologen eine sehr leistungsfähige Modalität zur Verfügung: „Als ich vor 20 Jahren in der CMR angefangen habe, dauerte die Analyse eine Stunde und war zudem sehr anwenderabhängig“, so die Expertin. „Heute genügt ein Klick, und die KI übernimmt die Konturierung – nicht nur der Volumina, sondern auch der späten Kontrastmittelanreicherung.“

Bildquelle: Bustin A, Stuber M, Sermesant M, Cochet H; European Heart Journal 2023 (CC BY-NC 4.0)
Auch um die Zukunft der Modalität ist Bucciarelli-Ducci nicht bang: Von CMR-Fingerprinting für die simultane und reproduzierbare Messung von T1- und T2-Bildgebung in einem einzigen Scan17 über Multitasking für eine einrichtungsfreie Bildgebung18 und quantitative Perfusionsbildgebung zur nicht-invasiven Diagnose von Ischämien19 bis hin zu Sauerstoff-sensitiver CMR für die kontrast- und nadelfreie Diagnose von Herzversagen20 – es gibt zahlreiche neue Ansätze, um das bereits solide Fundament zu verbessern und die Implementierungslücke zu schließen. „Indem wir die CMR schneller und einfacher machen, mehr Anwendern den Zugang ermöglichen und sie sicherer gestalten, können wir darauf hinarbeiten, sie so verfügbar und schnell wie die CT zu machen – und wir sind auf dem besten Weg dahin“, befand sie abschließend.
Nuklearbildgedung: Das kardiovaskuläre System als Ganzes betrachten
Im Vergleich zur MRT, die bei vielen kardiovaskulären Erkrankungen als diagnostisches Mittel der Wahl gilt, spielt die nuklearmedizinische Bildgebung eine eher untergeordnete Rolle. Dennoch sollte man sie nicht unterschätzen, riet Marc Dweck, Professor für klinische Kardiologie und Berater an der Universität Edinburgh und letzter Redner des Expertengremiums. „Ich bin sogar der Meinung, dass die nuklearmedizinische Bildgebung im Vergleich zu anderen Verfahren die spannendste Zukunft hat, zumindest was die zusätzlichen Informationen angeht, die sie uns meiner Meinung nach in den nächsten Jahren liefern wird“, erklärte er.
[Diese neuen Tracer] eröffnen uns wirklich interessante Möglichkeiten, Krankheiten besser zu verstehen, aber auch bessere Diagnosen zu stellen, das Therapieansprechen zu beurteilen und vieles mehr
Marc Dweck
Insbesondere die molekulare PET-Bildgebung biete in dieser Hinsicht großes Potenzial, da sich mit ihr nicht nur die Anatomie der Herzfunktion beurteilen, sondern auch die Aktivität spezifischer Prozesse überwachen lasse. Beispielsweise wird die FDG-PET-Bildgebung bereits zur Erkennung von Entzündungen und Infektionen bei prothetischer Herzklappenendokarditis und Sarkoidose des Herzens eingesetzt.21 Neue Tracer wie 18F-Fluorid, 18F-Fluorid GP1 und FAPI liefern noch detailliertere Einblicke in Entzündungen, Thrombusbildung, Kalzifizierungsaktivität und Fibroseaktivität.22 „Wir haben jetzt Tracer, die Aufschluss über jede der wichtigsten pathologischen Prozesse geben, die Herz-Kreislauf-Erkrankungen verursachen“, betonte Dweck. „Dies eröffnet uns wirklich interessante Möglichkeiten, Krankheiten besser zu verstehen, aber auch bessere Diagnosen zu stellen, das Therapieansprechen zu beurteilen und vieles mehr.“ Dies sei besonders relevant für Krankheiten ohne eindeutige Ursache, wie beispielsweise Schlaganfälle, fügte er hinzu.
Die Einführung von Ganzkörper-PET-Scannern sei ein weiterer Meilenstein für die nukleare Bildgebung, da diese einen umfassenden Blick auf das gesamte Herz-Kreislauf-System ermöglichten. „Wir können das Gehirn betrachten, das Herz und auch die peripheren Gefäße“, sagte Dweck. „Das erlaubt uns, Wechselwirkungen zwischen verschiedenen Organsystemen zu betrachten. Wenn wir das mit den neuen Tracern kombinieren, stimmen Sie mir hoffentlich zu, dass die Zukunft der nuklearen kardiovaskulären Bildgebung hochspannend ist.“
Wem gehört die Zukunft?
Und was bedeuten diese Fortschritte für die Zukunft der Herzbildgebung? Gräni fand vielleicht die passendsten Worte: „Multimodale Bildgebung ist der Schlüssel; das ist es, was wir bereits heute tun, aber es ist auch die Zukunft. Der Patient mit seiner klinischen Fragestellung steht im Mittelpunkt, und wir versuchen, diese bestmöglich zu beantworten, indem wir entscheiden, welche Bildgebungstechnik oder welche Kombination wir dafür einsetzen. Es gibt also nicht die eine beste Modalität, und keine Methode ist per se besser als die andere.“
Profile:
William A. Zoghbi, MD, ist Elkins Family Distinguished Chair in Cardiac Health, Vorsitzender der Abteilung für Kardiologie am Houston Methodist DeBakey Heart and Vascular Center und Professor für Medizin am Weill Cornell Medical College und am Houston Methodist Academic Institute, USA. Er hat seine Karriere der Weiterentwicklung der klinischen Kardiologie gewidmet und konzentriert sich dabei auf die Verbesserung nicht-invasiver Verfahren zur Beurteilung und Behandlung von Herzerkrankungen mittels kardiovaskulärer Bildgebung. Zu seinen Fachgebieten zählen Erkrankungen der Herzklappen, die koronare Herzkrankheit und Herzversagen, wobei er einen patientenorientierten Ansatz in der Medizin und der allgemeinen Kardiologie verfolgt.
Dr. Dr. Christoph Gräni ist Professor für Kardiologie an der Universität Bern und Leiter der Abteilung für Herzbildgebung, die sich mit Echokardiographie, Herz-MRT, Herz- CT und Nuklearkardiologie am Universitätsspital Bern befasst. Zu seinen Forschungsschwerpunkten zählt die Verbesserung der Diagnose und Risikostratifizierung verschiedener Kardiomyopathien, Myokarditis und kardialer Amyloidose mithilfe multimodaler Herzbildgebung, Myokardfunktionsanalyse und Fibrosebewertung. Darüber hinaus umfasst seine Forschung die nicht-invasive Beurteilung von koronaren Herzerkrankungen, insbesondere von Anomalien der Koronararterien.
Dr. Chiara Bucciarelli-Ducci ist Kardiologin am Royal Brompton and Harefield Hospital in Großbritannien und außerordentliche Professorin an der School of Biomedical Engineering & Imaging des King's College London. Sie ist eine international anerkannte Expertin für den Einsatz der kardialen Magnetresonanztomographie (CMR) in der Herz-Kreislauf-Medizin und verfügt über mehr als 20 Jahre klinische Erfahrung und Fachwissen. Der Schwerpunkt ihrer Karriere liegt auf der Verbesserung der Patientenversorgung durch optimierte Erkennung von Herzfehlern bei einer Vielzahl von Erkrankungen und Symptomen.
Dr. Marc Dweck ist Professor für klinische Kardiologie und Facharzt an der Universität Edinburgh, Großbritannien. Er ist Vizepräsident der EACVI und befasst sich mit der multimodalen Bildgebung sowie dem Einsatz von Herzimplantaten. Im Mittelpunkt seiner Forschungen steht der Einsatz multimodaler Bildgebung (Echokardiographie, CT, CMR, PET) für ein besseres Verständnis der kardiovaskulären Pathophysiologie und letztlich für eine Verbesserung der Patientenbeurteilung, -versorgung und -ergebnissen. Er veröffentlichte zahlreiche Artikel in führenden medizinischen und kardiovaskulären Fachzeitschriften und wurde mit vielen nationalen und internationalen Preisen ausgezeichnet.
Literatur:
- Peck D, Rwebembera J, Nakagaayu D et al.: The Use of Artificial Intelligence Guidance for Rheumatic Heart Disease Screening by Novices; Journal of the American Society of Echocardiography 2023; https://doi.org/10.1016/j.echo.2023.03.001
- Hirata Y, Nomura Y, Saijo Y, Sata M, Kusunose K: Reducing echocardiographic examination time through routine use of fully automated software: a comparative study of measurement and report creation time; Journal of Echocardiography 2024; https://doi.org/10.1007/s12574-023-00636-6
- Slivnick JA, Hawkes W, oliveira J et al.: Cardiac amyloidosis detection from a single echocardiographic video clip: a novel artificial intelligence-based screening tool; European Heart Journal 2025; https://doi.org/10.1093/eurheartj/ehaf387
- Valsaraj A, Kalmady SV, Sharma V et al.: Development and validation of echocardiography-based machine-learning models to predict mortality; eBioMedicine 2023; https://doi.org/10.1016/j.ebiom.2023.104479
- Finck T, Hardenberg J, Will A et al.: 10-Year Follow-Up After Coronary Computed Tomography Angiography in Patients With Suspected Coronary Artery Disease; JACC Cardiovascular Imaging 2018; https://doi.org/10.1016/j.jcmg.2018.07.020
- Sakai K, Shin D, Singh M et al.: Diagnostic Performance and Clinical Impact of Photon-Counting Detector Computed Tomography in Coronary Artery Disease; JACC 2024; https://doi.org/10.1016/j.jacc.2024.10.069
- Feuchtner GM, Lacaita PG, Bax JJ et al.: AI-Quantitative CT Coronary Plaque Features Associate With a Higher Relative Risk in Women: CONFIRM2 Registry; Circulation: Cardiovascular Imaging 2025; https://doi.org/10.1161/CIRCIMAGING.125.018235
- Nieman K, García-García HM, Hideo-Kajita A et al.: Standards for quantitative assessments by coronary computed tomography angiography (CCTA); Journal of Cardiovascular Computed Tomography 2024; https://doi.org/10.1016/j.jcct.2024.05.232
- Oikonomou EK, Marwan M, Desai MY et al.: Non-invasive detection of coronary inflammation using computed tomography and prediction of residual cardiovascular risk (the CRISP CT study): a post-hoc analysis of prospective outcome data; Lancet 2018; https://doi.org/10.1016/S0140-6736(18)31114-0
- Chan K, Wahome E, Tsiachristas A et al.: Inflammatory risk and cardiovascular events in patients without obstructive coronary artery disease: the ORFAN multicentre, longitudinal cohort study; Lancet 2024; https://doi.org/10.1016/S0140-6736(24)00596-8
- Shiri I, Baj G, Mohammadi Kazaj P et al.: AI-based detection and classification of anomalous aortic origin of coronary arteries using coronary CT angiography images; Nature Communications 2025; https://doi.org/10.1038/s41467-025-58362-9
- Illi J, Stark AW, Ilic M et al.: Hemodynamic Relevance Evaluation of Coronary Artery Anomaly During Stress Using FFR/IVUS in an Artificial Twin; JACC: Case Reports 2024; https://doi.org/10.1016/j.jaccas.2024.102729
- Raman SV, Markl M, Patel AR et al.: 30-minute CMR for common clinical indications: a Society for Cardiovascular Magnetic Resonance white paper; Journal of Cardiovascular Magnetic Resonance 2022; https://doi.org/10.1186/s12968-022-00844-6
- Foley JRJ, Richmond C, Fent GJ et al.: Rapid Cardiovascular Magnetic Resonance for Ischemic Heart Disease Investigation (RAPID-IHD); JACC: Cardiovascular Imaging 2020; https://doi.org/10.1016/j.jcmg.2020.01.029
- Bustin A, Stuber M, Sermesant M, Cochet H: Smart cardiac magnetic resonance delivering one-click and comprehensive assessment of cardiovascular disease; European Heart Journal 2023; https://doi.org/10.1093/eurheartj/ehac814
- Bhuva AN, Bai W, Lau C et al.: A Multicenter, Scan-Rescan, Human and Machine Learning CMR Study to Test Generalizability and Precision in Imaging Biomarker Analysis; Circulation: Cardiovascular Imaging 2019; https://doi.org/10.1161/circimaging.119.009214
- Liu Y, Hamilton J, Rajagopalan S et al.: Cardiac Magnetic Resonance Fingerprinting: Technical Overview and Initial Results; JACC: Cardiovascular Imaging 2018; https://doi.org/10.1016/j.jcmg.2018.08.028
- Christidoulou AG, Shaw JL, Ngyuen C et al.: Magnetic resonance multitasking for motion-resolved quantitative cardiovascular imaging; Nature biomedical Engineering 2018; https://doi.org/10.1038/s41551-018-0217-y
- Kotecha T, Martinez-Naharro A, Boldrini M et al.: Automated Pixel-Wise Quantitative Myocardial Perfusion Mapping by CMR to Detect Obstructive Coronary Artery Disease and Coronary Microvascular Dysfunction: Validation Against Invasive Coronary Physiology; JACC: Cardiovascular Imaging 2019; https://doi.org/10.1016/j.jcmg.2018.12.022
- Hillier E, Friedrich MG: The Potential of Oxygenation-Sensitive CMR in Heart Failure; Current Heart Failure Reports 2021; https://doi.org/10.1007/s11897-021-00525-y
- Pizzi MN, Roque A, Cuéllar-Calabria H et al.: 18F-FDG-PET/CTA of Prosthetic Cardiac Valves and Valve-Tube Grafts: Infective Versus Inflammatory Patterns; JACC: Cardiovascular Imaging 2016; https://doi.org/10.1016/j.jcmg.2016.05.013
- Rubeaux M, Joshi NV, Dweck MR et al.: Motion Correction of 18F-NaF PET for Imaging Coronary Atherosclerotic Plaques; Journal of Nuclear Medicine 2016; https://doi.org/10.2967/jnumed.115.162990
14.10.2025