Foto: Universitätsklinikum Heidelberg
News • Liquid Biopsy
Der erste marktfähige Bluttest für Brustkrebs ist da (Update: Sachbericht wird zurückgehalten)
Ein Meilenstein in der Brustkrebsdiagnostik: Die Universitäts-Frauenklinik des Universitätsklinikums Heidelberg hat ein neues Verfahren entwickelt, das mit Hilfe eines Bluttests die Erkennung von Brustkrebs verbessern kann.
Update V, 22.10.2019:
Das Verwaltungsgericht Karlsruhe hat auf Antrag des Rechtsanwalts von Herrn Prof. Dr. Christof Sohn eine sog. Einstweilige Anordnung erlassen. Mit dieser Anordnung wird es dem Universitätsklinikum vorläufig untersagt, sich zu wesentlichen Ergebnissen des Sachberichts der unabhängigen Kommission zu äußern, soweit sie Herrn Prof. Sohn und das gegen ihn geführte Disziplinarverfahren betreffen. Eine aussagekräftige Vorstellung der zentralen Ergebnisse des Berichts der Kommission ist damit nicht möglich. Die für heute angesetzte Pressekonferenz kann daher leider nicht stattfinden.
Das Universitätsklinikum prüft im Moment die Rechtsbehelfe dagegen. „Der Aufsichtsrat hat die externe Kommission damit beauftragt, den Sachverhalt in der Causa ,Bluttest/HeiScreen' möglichst lückenlos aufzuklären. Wir haben großes Interesse, dass diese Aufklärung in der größtmöglichen Transparenz geschieht. Wir setzen daher alles daran, dass wir zu einem späteren Zeitpunkt die Kommissionsergebnisse vorstellen können", sagte die Aufsichtsratsvorsitzende Dr. Simone Schwanitz.
Für die Kommission ist schwer nachvollziehbar, dass trotz des Verlustes der Wissensträger die Investorensuche und der Vertragsabschluss für HeiScreen von der tth und dem Projektverantwortlichen in großer Eile weiter vorangetrieben worden ist
Christine Hohmann-Dennhardt, Matthias Kleiner
Update IV, 26. Juli 2019:
Im Kontext der HeiScreen-Vorgänge ist nun der Dekan der Medizinischen Fakultät, Prof. Dr. Andreas Draguhn, zurückgetreten. Prof. Dr. Draguhn hatte das Amt des Dekans zum 1. Oktober 2018 als Nachfolger von Prof. Dr. Wolfgang Herzog angetreten.„Das Handeln des Dekans im Verlauf der HeiScreen-Affäre ist zum Gegenstand offizieller Untersuchungen geworden und wird in Teilen der Öffentlichkeit anhaltend kritisch diskutiert. Mit meinem Entschluss möchte ich hierfür die Verantwortung übernehmen und hoffe, damit dem Amt, der Fakultät und der Universität zu dienen“, so Prof. Draguhn, der weiterhin als Abteilungsleiter Neuro- und Sinnesphysiologie am Institut für Physiologie und Pathophysiologie der Medizinischen Fakultät Heidelberg tätig sein wird.
Die anstehenden Amtsvorgänge wurden an den Stellvertreter des Dekans, Prof. Dr. Hans-Georg Kräusslich, Abteilungsleiter Infektiologie und Virologie am Zentrum für Infektiologie des Universitätsklinikums Heidelberg, übergeben.
Update III, 16. Juni 2019:
Die Kommission, die zur umfassenden Aufklärung der Causa „Bluttest/HeiScreen" eingesetzt wurde, hat nun erste Zwischenergebnisse vorgestellt: Zur Entbindung der ersten Projektleiterin Prof. Dr. Sarah Schott gebe es zwar "divergierende Angaben", nach Einschätzung der Kommission handele es sich bei der Entscheidung, die Forscherin vollständig vom Projekt auszuschließen, um eine "Überreaktion der Entscheidungsverantwortlichen". Der Umgang mit der Forscherin wurde als "fragwürdig" bezeichnet. Das gelte auch für die Vergabe des Forschungsprojekts an einen Investor ohne Erfahrung in diesem Bereich – obwohl es Alternativen gegeben habe.
Deutliche Worte fand die Kommission auch für die Art der Bekanntmachung der Forschungsergebnisse: "Boulevard und bunte Blätter statt seriöser Wissenschaftskommunikation", lautet das Urteil – die Ankündigung sei zu früh erfolgt, obwohl die klinische Studie noch nicht abgeschlossen war. „Für die Kommission ist schwer nachvollziehbar, dass trotz des Verlustes der Wissensträger die Investorensuche und der Vertragsabschluss für HeiScreen von der tth und dem Projektverantwortlichen in großer Eile weiter vorangetrieben worden ist. Und dies – soweit uns bekannt ist – ohne die vorliegenden Forschungsergebnisse gegengeprüft zu haben“, sagten die Leiter der siebenköpfigen Kommission Dr. Christine Hohmann-Dennhardt und Professor Dr. Matthias Kleiner.
Da die Kommission weiterhin Unterlagen zur Durchsicht und Auswertung bearbeitet und Gespräche mit beteiligten Personen führt, sei eine abschließende Beurteilung ist noch nicht möglich, vermeldete das Klinikum. "Das Universitätsklinikum Heidelberg und der gesamte Medizinstandort Heidelberg genießt – zu Recht – einen international hervorragenden Ruf. Dieser Ruf hat durch den voreilig angekündigten Bluttest auf der Basis noch nicht tragfähiger Forschungsergebnisse Schaden genommen. Wir werden alles daransetzen, dass dies ein einmaliger Vorgang bleibt“ ", sagte Aufsichtsratsvorsitzenden Dr. Simone Schwanitz im Rahmen eines Pressetermins. Sie dankte der Kommission im Namen des Aufsichtsrats für die bereits geleistete Arbeit. „Der Aufsichtsrat wird die neuen Erkenntnisse umgehend beraten und Schlussfolgerungen ziehen“, so Dr. Schwanitz.
Die externe Kommission werde sich nach Abschluss der Sachverhaltsaufklärung in einem zweiten Schritt mit Empfehlungen zu Strukturen und Standards im Bereich Technologietransfer befassen, hieß es abschließend.
Update II, 5. April 2019:
Nach eigener Angabe hat das Universitätsklinikum am 4. April 2019 bei der Staatsanwaltschaft Heidelberg Strafanzeige gegen Unbekannt unter allen rechtlichen Gesichtspunkten gestellt. "Als öffentliche Einrichtung sieht sich das Universitätsklinikum aufgrund der Anzeichen eines unlauteren Vorgehens bei der Entwicklung und Ankündigung des potentiellen Bluttests zur Brustkrebsdiagnostik, der am 21. Februar der wissenschaftlichen Fachwelt und Öffentlichkeit vorgestellt worden war, zu diesem Schritt veranlasst. Die Entscheidung über die Aufnahme von Ermittlungen obliegt nun der Staatsanwaltschaft", so die Mitteilung. Die ersten Ergebnisse der unabhängigen Kommission werden in wenigen Wochen erwartet.
Update I, 25. März 2019:
Nach der Bekanntmachung des Bluttests war das Universitätsklinikum Heidelberg scharf wegen der Art und zum Zeitpunkt der Veröffentlichung kritisiert worden: Diese sei viel zu früh und aufgrund unüberprüfbarer wissenschaftlicher Ergebnisse erfolgt und habe damit ungerechtfertigte Hoffnungen geweckt. In einer Pressemitteilung reagiert das Universitätsklinikum auf diese Kritik: "Das Universitätsklinikum Heidelberg bedauert, dass es zu Irritationen gekommen ist und nimmt die Kritik ernst. Eine interne Arbeitsgruppe hat bereits die Aufarbeitung aufgenommen. Ebenfalls hat der Klinikumsvorstand die gemeinsame Stellungnahme von sechs Fachgesellschaften vom 27. Februar 2019 umgehend beantwortet. Um alle Aspekte umfassend und aus neutraler Perspektive zu analysieren wurde eine unabhängige Kommission aus überwiegend externen Experten eingerichtet. Sie wird dem Universitätsklinikum und der Medizinischen Fakultät ihre Ergebnisse berichten und Empfehlungen aussprechen."
Das neue blutbasierte Verfahren ist deutlich weniger belastend für Frauen, weil es weder schmerzhaft ist noch mit einer Strahlenbelastung einhergeht
Sarah Schott
Originalmeldung vom 21. Februar 2019:
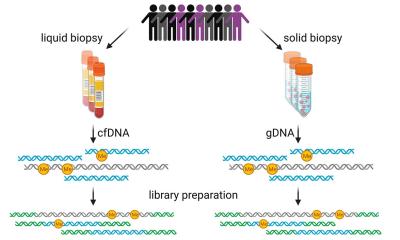
Auf Basis eines innovativen Liquid Biopsy-Verfahrens ist es möglich, die Erkrankung nicht-invasiv zu diagnostizieren. Das neue Verfahren erkennt eine Krebserkrankung anhand von Biomarkern und kann somit das Diagnosespektrum optischer Diagnoseverfahren wie Mammografie, Ultraschall oder MRT erweitern. Im Blut von an Brustkrebs erkrankten Frauen konnten 15 verschiedene Biomarker (miRNA und Methylierungsmarker) identifiziert werden, mit deren Hilfe auch kleine Tumore nachweisbar sind. "Der von unserem Forscherteam entwickelte Bluttest ist eine neue, revolutionäre Möglichkeit, eine Krebserkrankung in der Brust nicht-invasiv und schnell anhand von Biomarkern im Blut zu erkennen", sagte Prof. Dr. Christof Sohn, Geschäftsführender Ärztlicher Direktor der Universitäts-Frauenklinik Heidelberg. Prof. Dr. Sarah Schott, Sektionsleiterin Translationale Frauenheilkunde und Leiterin für Familiäre Krebserkrankungen an der Universitäts-Frauenklinik Heidelberg, die das Projekt gemeinsam mit Prof. Dr. Sohn leitet, ergänzt: "Das neue blutbasierte Verfahren ist deutlich weniger belastend für Frauen, weil es weder schmerzhaft ist noch mit einer Strahlenbelastung einhergeht."
Der Bluttest basiert auf dem Prinzip der Liquid Biopsy. Dabei handelt es sich um Verfahren, bei denen Informationen über eine Erkrankung aus Körperflüssigkeiten wie beispielsweise Blut, Urin oder Speichel gewonnen werden, indem Botenstoffe von Tumorzellen in einer Flüssigprobe untersucht werden. Für den Test sind nur wenige Milliliter Blut notwendig, er soll von jedem Labor durchgeführt werden können. Der Test kann bei Frauen aller Altersgruppen durchgeführt werden; besonders profitieren jüngere Frauen unter 50 Jahren und Frauen mit familiärer Hochrisikosituation für eine Brustkrebserkrankung, bei denen eine Mammografie beispielsweise aufgrund des dichten Brustdrüsengewebes wenig Aussage liefert oder aufgrund anderer Risikofaktoren herkömmliche bildgebende Verfahren kontraindiziert sind. Hier konnte eine Sensitivität von 80 bis 90 Prozent erreicht werden. Die Sensitivität gibt an, zu welchem Prozentsatz erkrankte Patientinnen durch den Test tatsächlich erkannt werden.
Dieser Artikel könnte Sie auch interessieren
Artikel • Therapiemonitoring
Wettlauf: Liquid Biopsy versus Radiomics
Die Entwicklung neuer Verfahren für präzises Therapiemonitoring in der Onkologie nimmt Fahrt auf. Die sogenannte Liquid Biopsy (Flüssigbiopsie) ist eines davon. Dank dieser neuen Labortechnik kann anhand einer Blutprobe nichtinvasiv freie Tumor-DNA identifiziert, charakterisiert und überwacht werden. Die Liquid Biopsy hat das Potenzial, die onkologische Diagnostik zu revolutionieren – und…
Das Universitätsklinikum Heidelberg hat sich bereits seit Jahren in der Forschung im Bereich Liquid Biopsy engagiert: 2016 wurde das dem Test zugrunde liegende Verfahren als Patent angemeldet und erste Fördermittel wurden gewonnen. Seitdem wurde das Verfahren verfestigt, weiterentwickelt und die Genauigkeit in diversen Untersuchungen bestätigt. Untersucht wurde in den letzten 12 Monaten eine Kohorte von über 900 Frauen mit über 500 Brustkrebspatientinnen und 400 gesunden Frauen. Die Studie ist auf eine Teilnehmerzahl von 2.000 ausgelegt und wird als Multizenterstudie fortgeführt. Aktuelle Ergebnisse zeigen bei den 500 Brustkrebspatientinnen insgesamt eine Sensitivität von 75 Prozent. Altersabhängige Unterschiede konnten gefunden werden. Hier zeigt sich bei den unter 50‑jährigen eine Sensitivität von 86 Prozent bzw. bei den über 50-jährigen von 60 Prozent.
Ziel der fortlaufenden Studie ist es, die Aussagekraft, Sensitivität und Einsatzmöglichkeit durch zukünftige Analysen weiter zu spezifizieren und zu verbessern. Auch wird der Einsatz bei weiteren Krebsarten, so z. B. Eierstockkrebs, erforscht. Die derzeitigen Zwischenergebnisse erreichen eine Sensitivität von bis zu 80 Prozent bei rund 200 untersuchten Patientinnen.
Markteinführung noch in diesem Jahr geplant
Neben der Erkennung einer Krebserkrankung kann der Bluttest zur Analyse weiterer Daten dienen. So soll zukünftig anhand von Biomarkern auch eine Metastasenbildung oder ein Rezidiv frühzeitiger erkannt werden und der Test bei der Langzeitüberwachung eingesetzt werden. Daneben dienen die gewonnenen Informationen auch der Therapie: Die Biomarker können Auskunft darüber geben, ob eine Behandlung anspricht oder eine Therapieresistenz eintritt. Die ersten Erkenntnisse deuten zudem darauf hin, dass das individuelle Ansprechen auf eine Chemotherapie über Liquid Biopsy überwacht werden kann und so langfristig personalisiertere Chemotherapiebehandlungen erfolgen können.
Um die notwendigen Zertifizierungen voranzutreiben und die Marktreife sicherzustellen, wurde nun eine Gesellschaft mit dem Namen HeiScreen GmbH ausgegründet. Die Gesellschaft wird die Markteinführung des Verfahrens voranbringen und Vertriebskanäle entwickeln. Die CE-Zertifizierung hat bereits begonnen, um den Bluttest noch in diesem Jahr in die klinische Anwendung zu bringen.
Quelle: Universitätsklinikum Heidelberg
16.07.2019