© nerthuz – stock.adobe.com
Artikel • Zukunft der operativen Therapie des Mammakarzinoms
Senologie 2034 – ein Blick auf die Brustkrebs-Behandlung von morgen
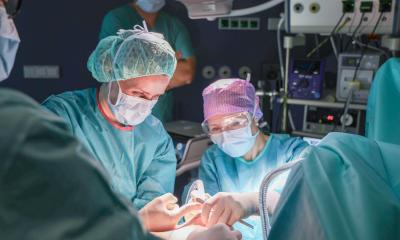
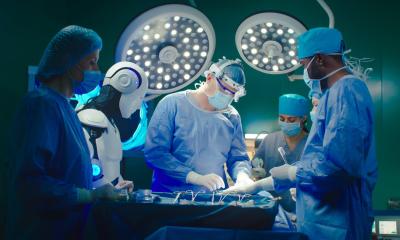
Wir schreiben das Jahr 2034. Brustkrebspatientinnen profitieren von perfekt auf sie zugeschnittene Diagnostik und Therapien. Endlose Nachbehandlungen sind dank KI, Datenbrillen und Robotik nicht mehr nötig. Ist das Zukunftsmusik oder bald schon klinische Realität? Auf dem Jahreskongress der Deutschen Gesellschaft für Senologie warf Prof. Dr. Marc Thill vom Agaplesion Markus Krankenhaus Frankfurt am Main einen Blick in die Glaskugel. Dabei beleuchtete er das Potenzial neuer Techniken und mehr Personalisierung, aber auch drohende Engpässe bei Diagnostika und Fachkräften.
Artikel: Wolfgang Behrends
Die Entwicklung gehe klar in Richtung der weiteren Verschlankung von Therapiepfaden und Deeskalation operativer Therapien, stellte der Experte fest. „Es tut unseren Patienten natürlich gut, wenn sie weniger Termine haben und wenn weniger an ihnen durchgeführt wird.“ So sinke mit der Zahl der Vor- und Nachbehandlungen etwa das Risiko kosmetisch schlechterer Ergebnisse und OP-bedingter Komplikationen wie Infektionen. Dieses Ziel der Verschlankung, zeigte er sich überzeugt, führt über die Ambulantisierung der Brustkrebs-Behandlung, wie sie etwa in Großbritannien und Dänemark schon weit vorangeschritten ist.1
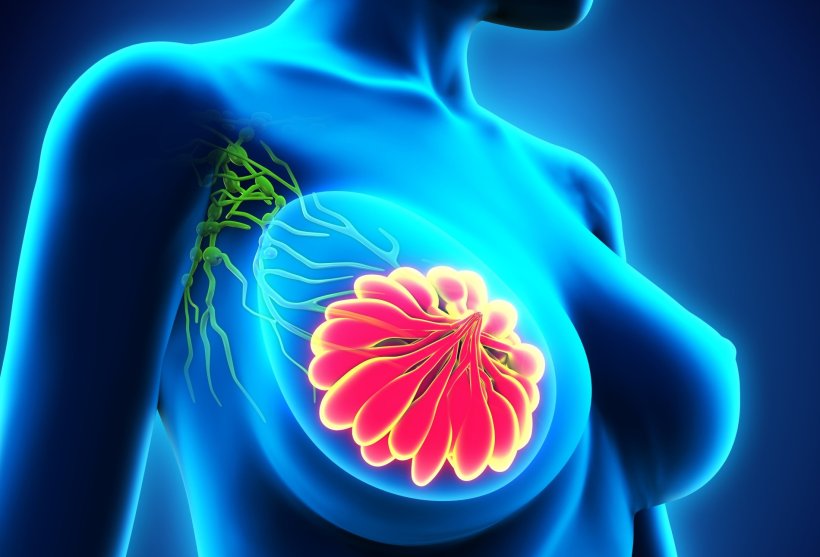
Zur Verschlankung der Prozesse beitragen werde auch die Etablierung nicht-radioaktiver Tracer zur Markierung von Sentinel-Lymphknoten (SLN), beispielsweise Indocyaningrün (ICG) und super-paramagnetischem Eisenoxid (SPIO). Diese Substanzen bieten mittlerweile eine Detektionsrate auf Augenhöhe mit Radiotracern2,3, jedoch ohne Abhängigkeit von nuklearmedizinischer Begleitung. Bei der Verwendung von ICG entfalle sogar der Vorbereitungstermin zur Verabreichung des Tracers, erklärte Thill – die Gabe erfolgt unkompliziert zehn Minuten vor der OP.
Dieser Artikel könnte Sie auch interessieren
Artikel • Forschung, Diagnostik, Behandlung
Themenschwerpunkt: Brustkrebs
Das Mammakarzinom ist in vielen Ländern der häufigste Krebs bei Frauen sowie die Krebserkrankung mit der höchsten Todesrate. Entsprechend vielfältig sind Diagnostik- und Therapieoptionen. Hier lesen Sie alles zu aktuellen Entwicklungen in der Früherkennung, Staging, Therapie und Forschung.
In Deutschland wird bei einem Großteil der Eingriffe mit SLN-Markierung auf radioaktive Marker wie Technetium-99m (99mTc) zurückgegriffen.4 Dabei sei deren Verfügbarkeit keineswegs immer gesichert, gab der Experte zu bedenken – etwa bei einem Ausfall der wenigen produzierenden Reaktoren.
3D-Druck, VR-Operationen und mehr: Was bringt die Zukunft?
Auch die Verwendung Sonden-basierter Markierungsverfahren führe zu einer Reduktion von Patiententerminen, da der Zwischenschritt der Draht- oder Clip-Lokalisierung entfalle. In Zukunft könnte der Behandlungspfad sogar noch weiter verschlankt werden, blickte Thill voraus: Ein neues Verfahren des US-Herstellers Cairn Surgical nutzt personalisierte, 3D-gedruckte Brustkappen mit integrierten Drahtkanälen, sodass komplett auf eine Markierung vor der OP verzichtet werden kann.
Noch weiter gehen Ansätze auf Basis virtueller Realität (VR), bei denen die Lage der Läsionen in der Brust und weitere Informationen über verschiedene Bildmodi im Headset eingeblendet werden. Prof. Thill, der auf dem US-Fachkongress der ASBrS Gelegenheit hatte, das Verfahren mit VR-Brille anzutesten, zeigte sich fasziniert von der Technik. „In den nächsten zehn Jahren werden wir aber voraussichtlich noch nicht so weit sein“, lautete seine Einschätzung.
© H_Ko – stock.adobe.com
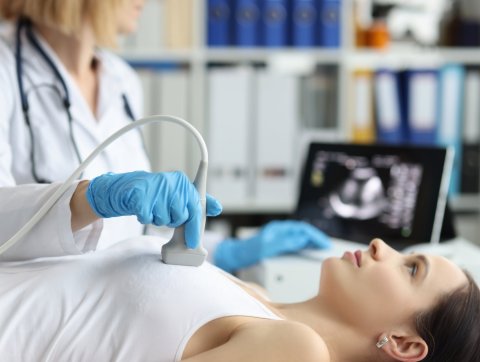
Bewegung sieht der Experte auch im Bereich der Ultraschall-Bildgebung zur intraoperativen Lokalisation von Läsionen: Die Aufnahme des Verfahrens in die aktuelle AGO-Leitlinie5 spiegele den diagnostischen Mehrwert der Sonografie6 wider – adäquate Geräte und entsprechende Expertise des Befunders vorausgesetzt. Als technischen Fortschritt nannte Thill in diesem Zusammenhang die gerade neu auf den Markt gekommenen ‚Hockeystick‘-Sonden, die die Befundung erleichtern.
Therapieansprechen per KI vorhersagen: „Freaky, aber funktioniert“
Als weiteres bildgebendes Verfahren zeigt auch die – bislang vorwiegend aus der Augenheilkunde bekannte – optische Kohärenztomographie (OCT) vielversprechende Ergebnisse für den Bereich der Senologie. Die OCT ermöglicht die Unterscheidung feinster Gewebeunterschiede, etwa zur Detektion von Tumorrückständen nach einer OP. Aktuelle klinische Studien beleuchten bereits die Kombination von OCT mit KI- und Machine-Learning-Methoden zur diagnostischen Unterstützung. Auch bei der Auswertung von Gewebescans aus der Pathologie oder integriert in Handheld-MRT-Systeme7 steht die KI-Unterstützung bereits in den Startlöchern.
KI kann aber in Zukunft wahrscheinlich noch viel mehr, blickt Thill nach vorne: Mittels Machine Learning lässt sich voraussagen, welche Patientinnen auf eine Chemotherapie so gut ansprechen, dass sie keine OP mehr benötigen.8,9 Noch einen Schritt weiter geht der Ansatz der US-Firma SimBioSys, deren Algorithmus aus Biopsie-Ergebnissen, verschiedener Bildgebung und weiteren klinischen Parametern ein 4D-Modell erstellt, das mithilfe biophysikalischer Simulationen vorhersagt, welche Patientin auf welche Therapie anspricht. „Das ist total freaky, aber es funktioniert“, bemerkt der Experte mit Blick auf die ersten Ergebnisse großer Kohortenstudien.
Helfende Roboter, stützende Scaffolds, fehlende Mitarbeiter
Mit einigen Hürden hätten derzeit zwei weitere vielversprechende Techniken zu kämpfen, erklärte Thill: So könnten sich durch Roboter-Assistenz die Ergebnisse Brustwarzen-erhaltender Mastektomien (RNSM) verbessern lassen.10 Hier gebe es aktuell aber noch zu viele Schwächen im Ablauf, so dass der Einzug in die klinische Routine wohl noch auf sich warten lassen werde.
Wir müssen uns um unseren Nachwuchs kümmern, denn ansonsten haben wir einen Qualitätsverlust und die Gefährdung der Versorgung
Marc Thill
Mit großem Interesse blickte der Experte zudem auf die implantatlose Brustrekonstruktion durch Lipotransfer. Dabei wird eine umgebende Scaffold-Struktur mit körpereigenem Fett ‚geflutet‘, so dass ein biokompatibler Ersatz entsteht.11 Anders als bei bisherigen Verfahren wäre auch hier idealerweise nur noch ein Eingriff nötig, aktuell sei der Fortschritt bei dieser Technik aber offenbar etwas zum Erliegen gekommen, resümierte Thill.
Zu guter Letzt sprach der Experte noch ein Zukunftsthema an, dessen Relevanz schon heute deutlich wird: „Seien Sie freundlich zu unseren Mitarbeiterinnen, denn diese sind derzeit viel schwerer zu bekommen als Patienten.“ Dieser scherzhafte Appell zielte auf den zunehmenden Fachkräftemangel ab, der auch die Senologie nicht verschont. „Wir müssen uns um unseren Nachwuchs kümmern, denn ansonsten haben wir einen Qualitätsverlust und die Gefährdung der Versorgung.“
Literatur:
- Albrecht M, Mansky T, Sander M, Schiffhorst G: Gutachten nach § 115b Abs. 1a SGB V; IGES Institut 2022
- Liu P, Tan J, Song Y, Huang K, Zhang Q, Xie H: The Application of Magnetic Nanoparticles for Sentinel Lymph Node Detection in Clinically Node-Negative Breast Cancer Patients: A Systemic Review and Meta-Analysis; Cancers 2022
- Kedrzycki MS et al.: Meta-analysis Comparing Fluorescence Imaging with Radioisotope and Blue Dye-Guided Sentinel Node Identification for Breast Cancer Surgery; Annals of Surgical Oncology 2021
- Lux MP, Untch M, Kolberg HC, Friedrich M, Thill M, Schütz F: Können wir uns innovative OP-Verfahren noch leisten?; Senologie 2023
- Kommission „Mamma“ der Arbeitsgemeinschaft Gynäkologische Onkologie (AGO): Diagnostik und Therapie früher und fortgeschrittener Mammakarzinome; Leitlinie 2024
- Banys-Paluchowski M et al.: Intraoperative Sonographie zur Entfernung von nicht-palpablen und palpablen Mammakarzinomen: systematisches Review und Meta-Analyse; Ultraschall in der Medizin 2022
- Thill M et al.: Magnetic resonance imaging system for intraoperative margin assessment for DCIS and invasive breast cancer using the ClearSight™ system in breast‐conserving surgery—Results from a postmarketing study; Journal of Surgical Oncology 2021
- Heil J et al.: Diagnosing Pathologic Complete Response in the Breast After Neoadjuvant Systemic Treatment of Breast Cancer Patients by Minimal Invasive Biopsy: Oral Presentation at the San Antonio Breast Cancer Symposium on Friday, December 13, 2019, Program Number GS5-03; Annals of Surgery 2022
- Pfob A et al.: Intelligent Vacuum-Assisted Biopsy to Identify Breast Cancer Patients With Pathologic Complete Response (ypT0 and ypN0) After Neoadjuvant Systemic Treatment for Omission of Breast and Axillary Surgery; Journal of Clinical Oncology 2020
- Kim JH, Lee J, Kim JY, Lee H, Park HS: Clinical Perspectives on Robot-assisted Nipple-sparing Mastectomy; Annals of Robotic and Innovative Surgery 2021
- Rehnke RD et al.: Breast Reconstruction Using a Three-Dimensional Absorbable Mesh Scaffold and Autologous Fat Grafting: A Composite Strategy Based on Tissue-Engineering Principles: Correction; Plastic and Reconstructive Surgery 2020
23.07.2024