News • Antibakterielle Cellulose
Ein Wundverband, der Bakterien abtötet
Damit bakterielle Infektionen direkt in der Wunde bekämpft werden können, haben Schweizer Forscher Membranen aus Cellulose entwickelt, die mit antimikrobiellen Eiweißbausteinen ausgestattet sind.
Erste Ergebnisse, die die Forscher der Empa nun im Journal Advanced Healthcare Materials veröffentlichten, zeigen: Die hautfreundlichen Membranen aus Pflanzenmaterial töten Bakterien äusserst effizient ab.
Dringen Keime in eine Wunde ein, können sie eine dauerhafte Infektion auslösen, die nicht abheilen mag oder sich sogar im Körper ausbreiten und zu einer lebensgefährlichen Blutvergiftung (Sepsis) führen kann. Gerade bei komplexen Wunden stellt sich heute immer häufiger das Problem der Antibiotika-Resistenz, da Bakterien wie etwa Staphylokokken unempfindlich gegen die einstige Wunderwaffe der Medizin geworden sind. Forschende der Empa haben daher Cellulose-Membranen entwickelt, mit denen sich derartige Infektionen im Keim ersticken lassen.
Das Team um Empa-Forscherin Katharina Maniura vom "Biointerfaces"-Labor in St. Gallen stellte hierzu feine Membranen aus pflanzlicher Cellulose mittels Electrospinning her. Die Cellulosefasern mit einem Durchmesser unter einem Mikrometer wurden zu einem zarten dreidimensionalen Gewebe in mehreren Schichten gesponnen. Besonders flexibel und gleichzeitig stabil wurden die Membranen, nachdem die Forschenden zusätzlich das Polymer Polyurethan mit eingesponnen hatten.
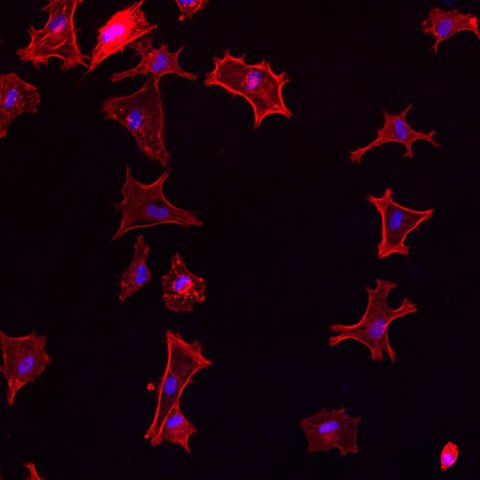
Bild: Empa
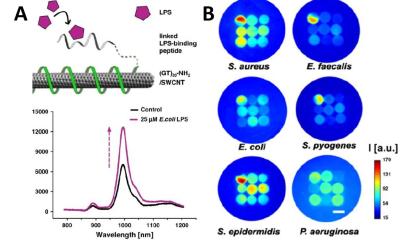
Um einen antibakteriellen Effekt zu erzielen, entwarfen die Forschenden multifunktionale Eiweißbausteine – so genannten Peptide –, die sich einerseits an die Cellulosefasern binden können und zudem eine antimikrobielle Aktivität aufweisen. Diese Peptide haben den Vorteil, dass sie einfacher herzustellen sind und stabiler bleiben als größere Proteine, die empfindlicher auf die chemischen Bedingungen in einer Wunde reagieren.
Behandelte man die Cellulose-Membranen mit einer derartigen Peptidlösung, sättigte sich das Faserngerüst mit den Eiweißbausteinen. In Zellkulturexperimenten wiesen die Forschenden daraufhin nach, dass die Peptid-haltigen Membranen für menschliche Hautzellen gut verträglich sind. Für Bakterien wie Staphylokokken, die häufig in schlechtheilenden Wunden zu finden sind, waren die Cellulose-Membranen hingegen ein Todesurteil. "In Bakterienkulturen wurden über 99.99 Prozent der Keime durch die Peptid-haltigen Membranen abgetötet", so Maniura.
Künftig sollen die antimikrobiellen Membranen zudem mit weiteren Funktionen ausgestattet werden. "Die Peptide könnten beispielsweise mit Bindungsstellen funktionalisiert werden, die eine kontrollierte Abgabe von weiteren therapeutischen Wirkstoffen ermöglichen", so Maniura.
Quelle: Eidgenössische Materialprüfungs- und Forschungsanstalt (Empa)
12.08.2020