© Sagittaria – stock.adobe.com
News • Resistenztestung in wenigen Minuten
Forscher entwickeln neuen Schnelltest gegen resistente Keime
Die rasante Zunahme antibiotikaresistenter Bakterien stellt eine der drängendsten Herausforderungen für die globale Gesundheit dar. Ein neues transatlantisches Fraunhofer-Forschungsprojekt zielt darauf ab, diesen Bedrohungen mit einem innovativen Diagnoseansatz zu begegnen:
Ein mikrofluidisches Schnelltestsystem soll mithilfe von Kohlenstoff-Nanoröhrchen (SWCNT) bakterielle Resistenzen in wenigen Minuten sichtbar machen und damit deutlich schneller als herkömmliche Verfahren.
Der breite und unspezifische Einsatz von Antibiotika hat dazu geführt, dass sich mikrobielle Resistenzen gegen Antibiotika rasant ausgebreitet haben. Antibiotikaresistente Keime verursachen jährlich etwa 700.000 Todesfälle weltweit. In vielen dieser Fälle wurden Patienten mit nicht wirksamen Antibiotika therapiert, weil Resistenzen der Erreger zu spät nachgewiesen wurden.
Dieser Artikel könnte Sie auch interessieren

Artikel • AMR-Themenkanal
Antibiotikaresistenz: eine globale Bedrohung
Antibiotikaresistenz (AMR) stellt eine zunehmende Bedrohung für die öffentliche Gesundheit auf der ganzen Welt dar. Bakterien, die gegen verfügbare Antibiotika resistent werden, machen alltägliche medizinische Verfahren aufgrund des hohen Infektionsrisikos unmöglich. Lesen Sie weiter und erfahren Sie mehr über die AMR-Forschung, die Entwicklung neuer Antibiotika und Antibiotika-Alternativen.
Ein transatlantisches Fraunhofer-Forschungsprojekt will mit einem neuen Ansatz nun eine Diagnostikplattform entwickeln, die schnell und einfach nachweist, ob eine Infektion mit resistenten Bakterien vorliegt. Leitende Institution des Projekts ist das Fraunhofer USA Center for Manufacturing Innovation CMI mit Sitz in Boston. Gemeinsam mit dem Fraunhofer-Institut für Mikroelektronische Schaltungen und Systeme IMS in Duisburg und dem Fraunhofer-Institut für Grenzflächen- und Bioverfahrenstechnik IGB in Stuttgart wird in den kommenden 18 Monaten eine neuartige Plattform zur schnellen phänotypischen Antibiotikaresistenztestung (AST) entwickelt.
"Die klinische Mikrobiologie braucht dringend flexible und schnelle AST-Tools, die mit der Geschwindigkeit des Infektionsgeschehens Schritt halten können", erklärt Jan Stegemann, Projektleiter am Fraunhofer IMS. "Unser Ziel ist eine funktionale Plattform, die noch deutlich vor dem Zelltod des Erregers metabolische Veränderungen als zelluläre Stressreaktion auf ein Antibiotikum erkennt und so eine frühzeitige, evidenzbasierte Therapieentscheidung unterstützt."
© Fraunhofer USA CMI
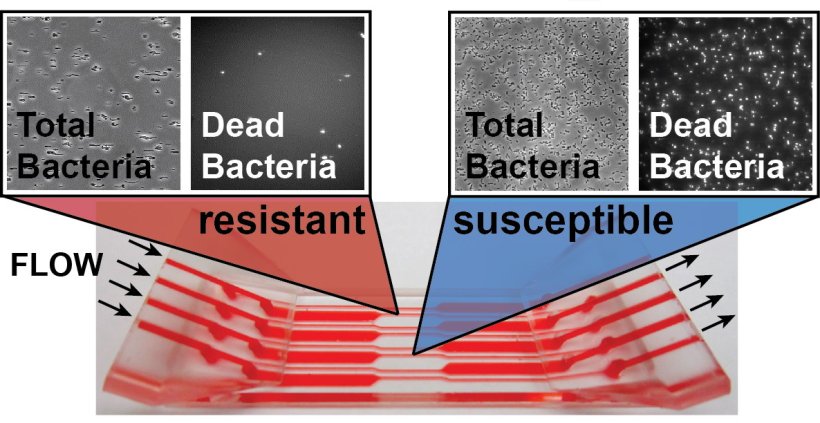
Derzeit basieren viele marktübliche Systeme auf Zellwachstum in Mikrotiterplatten und benötigen acht bis 16 Stunden, um zu einem Ergebnis zu kommen. Die neue Plattform 'µFLOWDx' soll künftig in nur wenigen Minuten verwertbare Erkenntnisse liefern und damit einen potenziellen Durchbruch für Forschung, Klinik und Pharmazie ermöglichen.
Dies will das interdisziplinäre Projektteam mit einem innovativen Lösungsansatz erreichen. Damit der schnelle Nachweis funktioniert, müssen die aus Patientenproben stammenden Bakterien zum einen in der Messzelle angebunden werden. Dazu wird das mikrofluidische System der Diagnostikplattform mit speziellen Oberflächen ausgestattet, die eine hohe Adhäsion zu den Erregern zeigen. Zum anderen beinhaltet das System hochsensitive optische Sensoren auf Basis von fluoreszierenden Kohlenstoff-Nanoröhrchen. Werden als Reaktion auf ein Antibiotikum Moleküle freigesetzt, die zellulären Stress anzeigen, etwa ATP oder Wasserstoffperoxid (H2O2), verändern die Sensoren ihre Fluoreszenz. So kann die mikrobielle Resistenz in Echtzeit durch Überströmen der adhärierten Patientenbakterien mit typischen Antibiotika untersucht werden: Ist der Erreger gegen das getestete Antibiotikum resistent, ändert sich das Fluoreszenzsignal des Sensors nicht.
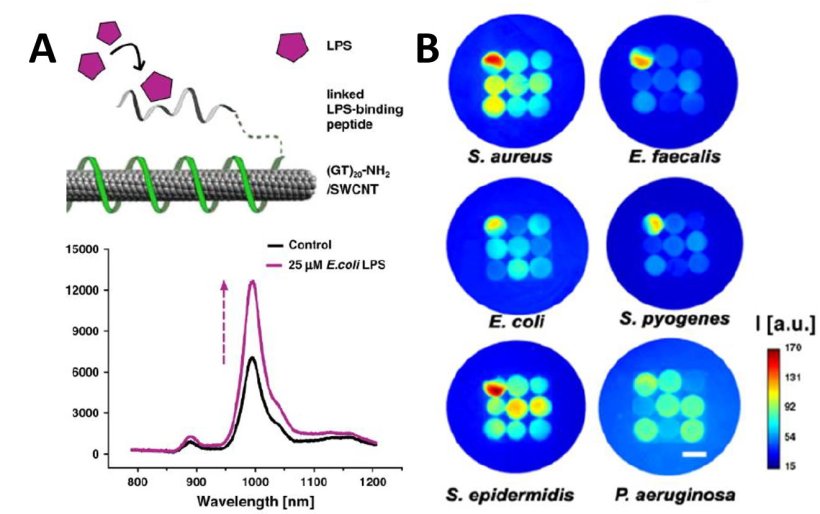
Bildquelle: Fraunhofer IMS; adaptiert von: Nißler R, Bader O, Dohmen M et al., Nature Communications 2020 (CC BY 4.0)
Die Projektpartner bringen unterschiedliche Expertisen ein, um das angestrebte Ziel zu realisieren: Um eine hohe bakterielle Adhäsion an der Oberfläche der Mikrofluidik zu erreichen, entwickelt das Fraunhofer IGB geeignete Oberflächenmodifikationen. Für die Detektion von zellulären 'Stress'-Molekülen bringt das Fraunhofer IMS seine Expertise in der Entwicklung sensitiver optischer Biosensoren basierend auf Kohlenstoff-Nanoröhrchen ein. Beide Komponenten werden in der mikrofluidischen Plattform vom Fraunhofer USA CMI integriert.
Im Rahmen des Projekts soll ein funktionsfähiger Prototyp entstehen, der unter praxisnahen Bedingungen validiert werden kann. Perspektivisch ist auch eine Kommerzialisierung als Diagnostik-Tool geplant. Erste Marktanalysen zeigen ein hohes Interesse: Das Segment der klinischen Mikrobiologie wächst und wird von international führenden Unternehmen dominiert, jedoch ohne Lösungen, die eine vergleichbare Geschwindigkeit und Sensitivität bieten.
Gefördert wird das Projekt im Rahmen des Fraunhofer-internen PACT-Programms (Fördernummer: 40-11763) zur Stärkung transatlantischer Forschung. Es läuft vom 01.07.2025 bis 31.12.2026. Neben der angestrebten Technologieentwicklung stehen auch gemeinsame Publikationen, Messeauftritte sowie Folgeanträge bei internationalen Förderprogrammen auf der Agenda.
Quelle: Fraunhofer-Institut für Mikrolektronische Schaltungen und Systeme IMS
05.09.2025