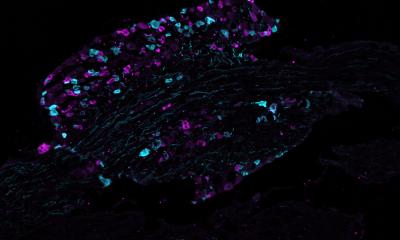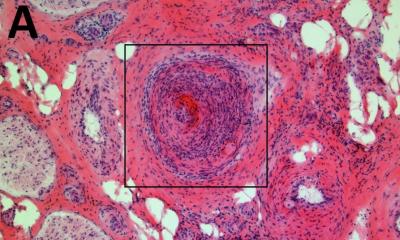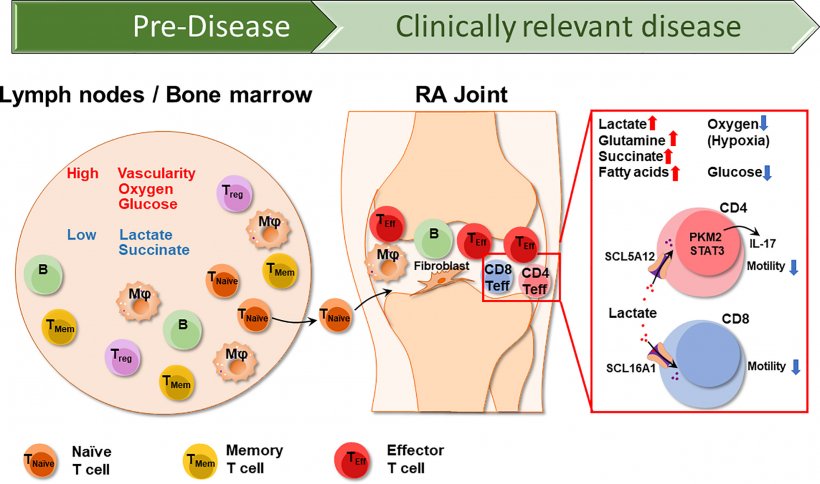
Bildquelle: Qiu et al., Frontiers 2021 (CC BY 4.0)
News • Neue Therapieansätze erwartet
Rheumatoide Arthritis: Einzelzell-Analyse erlaubt neue Einblicke
Zur rheumatoiden Arthritis kommt es, wenn das Immunsystem die Synovialmembran der Gelenkhaut angreift. Unter den Folgen, schmerzhaften Schwellungen in wechselnden Gelenken, leiden in Deutschland über eine halbe Million Menschen, bei denen es ohne Behandlung zur allmählichen Zerstörung der Gelenke käme.
Neue Einblicke in das Krankheitsgeschehen liefern derzeit Massenuntersuchungen einzelner Zelltypen. Über diese Forschungsergebnisse und inwiefern sie neue Anregungen für die Behandlung von Rheumapatienten erwarten lassen, berichtete ein Experte des Kompetenznetzes Rheuma auf der Pressekonferenz zur Jahrestagung der Deutschen Gesellschaft für Rheumatologie e.V. (DGRh).
Dieser Artikel könnte Sie auch interessieren
Artikel • Digitale Lösungen für Rheumapatienten
Interesse groß, Möglichkeiten ausbaufähig
Die Covid-19-Pandemie erwies sich als Katalysator für Gesundheits-Apps, Wearables und Videosprechstunden. Patienten mieden den Besuch beim Arzt aus Angst, sich mit dem Virus anstecken zu können, und nutzten vermehrt digitale Lösungen. Über die Vor- und Nachteile dieser technischen Errungenschaften für Menschen mit Rheuma diskutierten Experten im Rahmen des Deutschen Rheumatologiekongresses.
Die Behandlung der rheumatoiden Arthritis hat in den letzten Jahrzehnten stark von den Erkenntnissen der Grundlagenforschung profitiert. „Die Rheumatologen können den Krankheitsverlauf mittlerweile durch die Injektion oder Infusion von verschiedenen biologischen Antikörpern von Abatacept bis Rituximab gut beeinflussen“, erklärt der Sprecher der Arbeitsgemeinschaft Kompetenznetz Rheuma, Professor Dr. Ulf Wagner vom Universitätsklinikum Leipzig. Zuletzt seien noch synthetische Medikamente wie Baricitinib oder Tofacitinib hinzugekommen, die als Tablette eingenommen werden können. „Die neuen Mittel machen die Behandlung für viele Patienten erträglicher“, so der Experte.
Die genannten Wirkstoffe blockieren einzelne Zytokine oder deren Rezeptoren, die im Rahmen der Entzündungsprozesse von den Zellen des Immunsystems freigesetzt werden. Die Grundlagenforschung hat sich mittlerweile den unterschiedlichen Entzündungszellen zugewandt, die diese Zytokine produzieren. Neuere sogenannte Omics-Methoden wie Einzelzell-RNA-Sequenzierung, Ribosomen-Profiling, oder die Massenspektrometrie ermöglichen erstmals einen Einblick in einzelne Zellen. „Die Untersuchungen zeigen, welche Zellgruppen sich bei Rheumapatienten anders verhalten als bei Gesunden und welche deshalb wahrscheinlich am Krankheitsprozess beteiligt sind“, erläutert Professor Wagner.
Unser Ziel müsste es sein, die ‚bösen‘ T-Zellen in ‚gute‘ T-Zellen zu verwandeln und den Krankheitsprozess gleich zu Beginn zu stoppen
Ulf Wagner
Einer der zentralen Akteure der rheumatoiden Arthritis sind die Gewebsmakrophagen, die auch bei gesunden Menschen in der Synovialmembran vorhanden sind. „Die Forschung will klären, was diese Zellen dazu bewegt, die entzündlichen Zytokine freizusetzen, und wie dies verhindert werden könnte“, so der Experte. Die Grundlagenforscher haben beispielsweise herausgefunden, dass es zwei Gruppen von Gewebsmakrophagen gibt, die sich durch die Oberflächenmarker MerTK und CD206 unterscheiden. Eine kürzlich in Nature Medicine publizierte Studie ergab, dass MerTK-negative und CD206-negative Gewebsmakrophagen eine Reihe von entzündungsfördernden Zytokinen und Alarminen produzieren und damit die Entzündungsreaktionen in der Synovialmembran fördern. Im Gegensatz dazu scheinen MerTK-positive und CD206-positive Gewebsmakrophagen die Entzündungsreaktionen zu hemmen. Diese Zellen werden vor allem bei Patienten gefunden, deren Entzündung vollständig abgeklungen ist. Professor Wagner erklärt: „Die Idee für einen Therapieansatz wäre, die Gewebsmakrophagen durch Medikamente in einen dauerhaften Ruhezustand zu versetzen und dadurch die Krankheit langfristig zu stoppen.“
Ein weiterer neuer Behandlungsansatz könnte sich aus Erkenntnissen zum Stoffwechsel in den B-Zellen und T-Zellen ergeben. „Wir gehen derzeit davon aus, dass am Anfang der Erkrankung ein Verlust der Selbsttoleranz steht, der T-Zellen normalerweise davon abhält, körpereigene Zellen in der Synovialmembran zu attackieren“, sagt der Rheumatologe. „Die T-Zellen beginnen, die Synovialzellen anzugreifen, und sie veranlassen die B-Zellen zur Bildung von Antikörpern, von denen der Rheumafaktor das bekannteste Beispiel ist.“ Die Omics-Untersuchungen zeigen nach Auskunft des Experten, dass sich der Stoffwechsel von T-Zellen im Verlauf der Erkrankung komplett umstellt. Die Energieversorgung werde beispielsweise von der Glykolyse auf den Pentosephosphatweg umgestellt. „Diese veränderten Stoffwechselvorgänge liefern möglicherweise völlig neue Möglichkeiten zur therapeutischen Beeinflussung von chronisch-entzündlichen Autoimmunerkrankungen“, sagt Professor Wagner. „Unser Ziel müsste es sein, die ‚bösen‘ T-Zellen in ‚gute‘ T-Zellen zu verwandeln und den Krankheitsprozess gleich zu Beginn zu stoppen.“
Quelle: Deutsche Gesellschaft für Rheumatologie
17.09.2021