News • Photothermische Tumortherapie
Infrarotlicht könnte Tumoren kräftig einheizen
Neuer Ansatz für wirksamere photothermische Tumortherapie mit Infrarotlicht
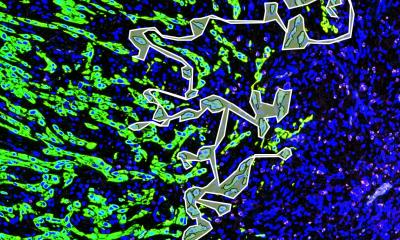
Nanostäbchen aus Bismutsulfid lassen Tumorzellen den Hitzetod sterben, wenn sie mit nahem Infrarot-Licht (NIR) bestrahlt werden. Chinesische Wissenschaftler machen diese Waffen jetzt noch leistungsstärker, indem sie die Defektstruktur des Kristallgitters durch winzige Goldpünktchen umgestalteten. Wie sie in der Zeitschrift Angewandte Chemie berichten, könnte dies ein Ausgangspunkt für eine effektivere photothermische Tumortherapie sein.
Bei der Photothermie wird ein Wirkstoff in den Tumor eingeschleust und diese Region mit NIR bestrahlt, einer Wellenlänge, die sehr tief in Gewebe eindringt, ohne es zu schädigen. Der Wirkstoff absorbiert das NIR und wandelt es in Wärme um. Die Tumorzellen werden durch die lokale Überhitzung abgetötet, während gesundes Gewebe geschont wird. Besonders praktisch ist es, wenn der Wirkstoff gleichzeitig als Kontrastmittel für bildgebende diagnostische Verfahren dient, wie die Computertomographie (CT), mit deren Hilfe sich der Tumor lokalisieren lässt.
Nanomaterialien aus dem Halbleiter Bismutsulfid (Bi2S3) sind für diese Aufgaben gut geeignet. Forschern um Haiyuan Zhang von der Chinesischen Akademie der Wissenschaften (Changchun, Jilin, China) ist es nun gelungen, die Mechanismen, die den photothermischen Eigenschaften dieser Materialien zugrunde liegen, genauer aufzuklären. Darauf aufbauend konnten sie die photothermische Effektivität von Bismutsulfid-Nanostäbchen weiter steigern, indem sie Nanodots („Nanopünktchen“) aus Gold auf die Oberfläche der Stäbchen aufbrachten.
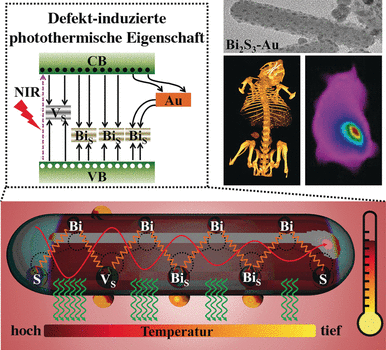
Stark vereinfacht funktioniert das Ganze so: Licht kann bei Halbleitern negativ geladene Elektronen so anregen, dass sie in ein höheres Energieniveau, das Leitungsband, gelangen. Zurück bleiben positiv geladene „Löcher“. Bei der Rekombination von Elektronen und Löchern wird wieder Energie frei, die an das Kristallgitter abgegeben wird und es in Schwingungen versetzt. Die Schwingungsenergie wird dann in Form von Wärme an die Umgebung abgegeben. Bestimmte Defekte im Kristallgitter, sogenannte tiefe Fallen, fördern diese Art der Elektronen-Loch-Rekombination.
In Bi2S3-Nanomaterialien, die unter Bi-Überschuss und S-Mangel synthetisiert werden, entstehen Schwefel-Fehlstellen und Substitutionen, bei denen ein Bi- ein S-Atom ersetzt. Beide können als tiefe Fallen wirken. Eine Erhöhung der Zahl tiefer Fallen oder ein verstärktes Einbringen von Elektronen in diese Fallen könnte also die photothermische Effizienz von Bi2S3-Nanomaterialien verbessern. Hier kommen die Gold-Atome ins Spiel. Sie binden Schwefel-Atome und halten diese von ihren Gitterplätzen fern. So entstehen mehr Defekte. Außerdem bieten die Kontaktstellen zwischen Bi2S3 und Gold den angeregten Elektronen ein Energieniveau, über das sie leichter als auf direktem Weg auf das Energie-Niveau der Substitutionsfehlstellen kommen, sodass mehr Elektronen in diesen Typ „Falle“ gelangen.
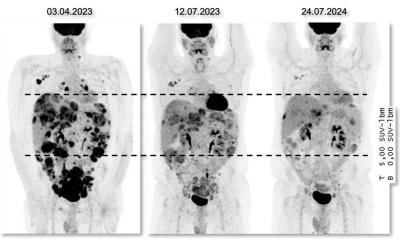
Als Kontrastmittel für CT-Aufnahmen zeigten die Stäbchen Tumore in Mäusen sehr gut an, da sie sich bevorzugt in Tumorzellen anreichern. Das Tumorwachstum wurde mit der Gold-Version unter NIR-Bestrahlung deutlich stärker gehemmt als mit goldfreien Stäbchen. Nach 14-tägiger Behandlung der Mäuse waren einige der Tumore sogar völlig verschwunden. Toxische Nebeneffekte und Beeinträchtigungen des umgebenden Gewebes wurden nicht beobachtet.
Quelle: Gesellschaft Deutscher Chemiker e.V.
13.12.2017