News • PSP, CBS
Atypisches Parkinson-Syndrom: Tau "wandert" über Hirn-Netzwerke
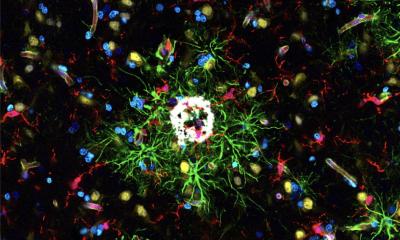
Neben dem „typischen“ Parkinson-Syndrom gibt es seltene, sogenannte atypische Formen, bei dem sich fehlgefaltete „Tau-Proteine“ in den Hirnzellen der Patienten ablagern. Nun hat ein internationaler Forschungsverbund unter Federführung des Klinikums der Universität München und des Deutschen Zentrums für Neurodegenerative Erkrankungen herausgefunden: Die krankhaften Tau-Proteine verteilen sich nicht wahllos im Gehirn
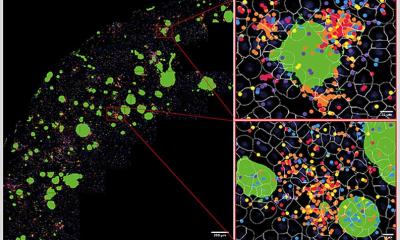
Bildquelle: Franzmeier et al., Nature Communications 2022 (CC BY 4.0)
Vielmehr dienen Verbindungen zwischen den Nervenzellen als Ausbreitungsroute für die krankhaft veränderten Eiweiße. Die Studie wurde im Fachjournal „Nature Communications“ veröffentlicht.
Atypische Formen des Parkinsonsyndroms wie die „Progressive Supranukleäre Parese“ (PSP) und das „Corticobasale Syndrom“ (CBS) sind tödliche neurodegenerative Erkrankungen. Wirksame Behandlungsmöglichkeiten gibt es nicht. Die Krankheiten schreiten typischerweise rasch fort, wobei die Betroffenen zunehmende Beeinträchtigungen der Körper- und Blickmotorik sowie Stürze und Störungen der Hirnleistung zeigen. In Untersuchungen an den Gehirnen verstorbener Patienten zeigte sich: In ihren Neuronen breiten sich mit zunehmender Krankheitsschwere krankhafte Tau-Proteine in Nervenzellen aus und die Neuronen sterben ab. „Daher ist es besonders wichtig, zu verstehen, über welche Wege sich die Tau-Eiweiße im Gehirn ausbreiten, um mögliche therapeutische Ansatzpunkte zu identifizieren, die das Fortschreiten der Erkrankung bremsen könnten“, sagt Dr. Nicolai Franzmeier.
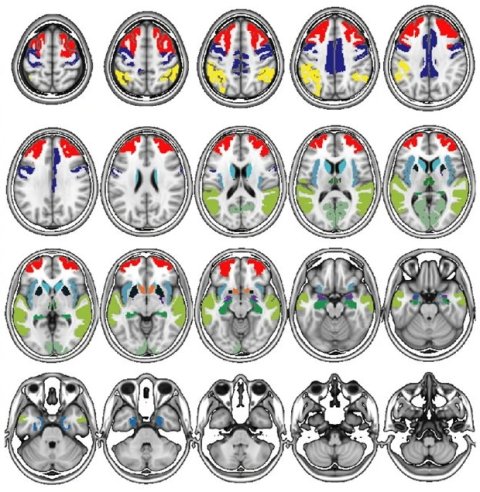
So haben sich der Forscher vom Institut für Schlaganfall- und Demenzforschung (ISD) und seine Kollegen an die Arbeit gemacht. Zunächst haben die Forschenden eine neuartige Bildgebungsmethode namens Tau-PET verwendet. Damit haben sie Tau-Ablagerungen in den Gehirnen von 46 lebenden Patienten mit PSP und CBS sichtbar gemacht. „So haben wir gezeigt, dass die Tau-Ablagerungen zuerst im Hirnstamm und in zentralen, für die Motorik relevanten Bereichen des Gehirns – den Basalganglien – auftreten“, sagt Franzmeier. Der Befund bestätigt Untersuchungen mit Hirngewebe verstorbener Patienten und erklärt vermutlich, warum diese vornehmlich motorisch beeinträchtigt sind.
Anschließend kombinierten die Forschenden ihre Untersuchungsmethode mit der so „funktionellen Magnetresonanztomographie“ (fMRT). Dieses Verfahren enthüllt die Vernetzung zwischen einzelnen Hirnregionen. Über die Kombination von Tau-PET und fMRT „haben wir erstmals nachgewiesen, dass sich das Tau-Eiweiß bei PSP und CBS-Patientinnen und -Patienten vornehmlich entlang vernetzter Hirnregionen ausbreitet“, sagt Franzmeier.
Dieser Artikel könnte Sie auch interessieren
Artikel • Therapieplanung
fMRT blickt Tumorpatienten ins Gehirn
Ursprünglich rein in der Forschung zuhause, hat sich die funktionelle Magnetresonanztomographie (fMRT) inzwischen einen festen Platz in der präoperativen Hirntumordiagnostik erobert. Die Technik macht Hirnaktivität sichtbar – das kann bei der Therapieplanung von Hirntumoren ein entscheidender Vorteil sein.
Ihre Ergebnisse übertrugen die Forschenden auf Daten von knapp 200 verstorbenen PSP-Patienten, bei denen die Tau-Ablagerungen in den Nervenzellen in mehreren Gehirnregionen nach dem Tod gemessen wurden. Last not least kombinierten die Forschenden diese Daten verstorbener PSP-Patienten mit der fMRT-basierten „Netzwerkkarte“ des Gehirns, um zu untersuchen, ob sich die Ergebnisse aus der Tau-PET-Untersuchung bestätigen würden. „Auch hier“, so Franzmeier, „kann die Vernetzung der Hirnregionen das Muster der Tau-Ablagerungen im Gehirn der Verstorbenen erklären.“ Und weiter: „Gehirnnetzwerke und die Verknüpfungen zwischen Hirnregionen spielen vermutlich eine zentrale Rolle in der Ausbreitung der Tau-Eiweiße bei PSP- und CBS-Patientinnen und -Patienten.“
Klinisch haben die Ergebnisse für Diagnose und Therapie der Erkrankten derzeit keine Auswirkungen. Doch langfristig wollen die Forschenden ihr Modell auch zur individuellen Vorhersage der Verbreitung der Tau-Pathologie weiterentwickeln, um eine bessere Krankheitsprognose zu ermöglichen.
Quelle: Klinikum der Universität München
28.03.2022