News • Tumordiagnostik
Neues KI-Modell erkennt mehr als 170 Krebsarten
Auf der Suche nach neuen Wegen für die Diagnosestellung bei Hirntumoren haben Forschende der Charité – Universitätsmedizin Berlin zusammen mit Kooperationspartnern ein KI-Modell entwickelt. Die Grundlage: spezifische Merkmale am Erbgut der Tumoren – ihr epigenetischer Fingerabdruck, gewonnen unter anderem aus Nervenwasser.
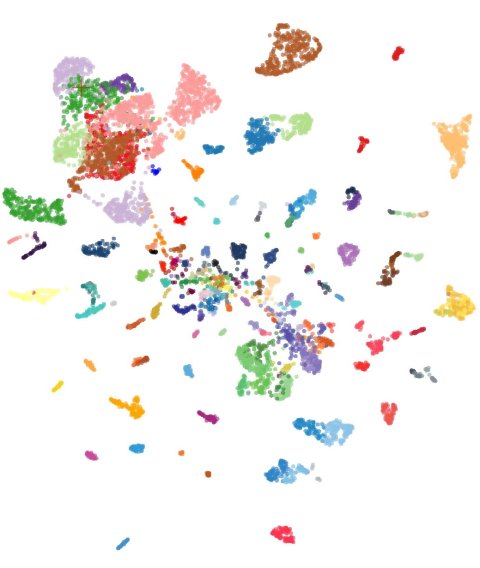
© Charité | Philipp Euskirchen
Wie das Team im Fachmagazin Nature Cancer zeigt, klassifiziert das neue Modell schnell und sehr zuverlässig.
Heute sind weit mehr Tumorarten bekannt als Organe, aus denen sie hervorgehen. Jeder Tumor hat seine eigenen Charakteristika, bestimmte Gewebemerkmale, Wachstumsraten, Stoffwechselbesonderheiten. Dennoch lassen sich Tumortypen mit ähnlichen molekularen Eigenschaften in Gruppen zusammenfassen. Von der Art des Tumors hängt entscheidend die Behandlung der jeweils individuellen Erkrankung ab. Neue, zielgerichtete Therapien sprechen bestimmte Strukturen von Tumorzellen an oder legen deren Signalwege lahm, um dem krankhaften Gewebewachstum Einhalt zu gebieten. Chemotherapien lassen sich nach Tumortyp auswählen und in ihrer Dosierung anpassen. Besonders seltene Tumorarten können möglicherweise im Rahmen von Studien mit neuartigen Therapien behandelt werden.
„Vor dem Hintergrund einer zunehmend personalisierten, sich schnell entwickelnden Krebsmedizin ist eine präzise Diagnosestellung an einem zertifizierten Tumorzentrum wegweisend für eine erfolgreiche Behandlung“, sagt Prof. Martin E. Kreis, Vorstand Krankenversorgung der Charité. Während eine umfassende molekulare, zelluläre und funktionelle Analyse eines Tumors anhand von Gewebeproben die nötigen Informationen liefert, sind Mediziner ebenso mit Fällen konfrontiert, in denen eine Entnahme von Tumorgewebe nicht möglich oder sehr riskant ist. Hinzu kommt: Auch eine feingewebliche Untersuchung allein kann keine so präzisen Diagnosen stellen wie das neue KI-Modell.
Dieser Artikel könnte Sie auch interessieren

News • Themenkanal
Blickpunkt: KI in der Medizin
Künstliche Intelligenz soll menschliche Denkprozesse nachbilden und die Arbeit fast aller medizinischer Teilgebiete erleichtern. Doch was geht im Inneren eines KI-Algorithmus vor, worauf basieren seine Entscheidungen? Kann man einer Maschine gar eine medizinische Diagnose anvertrauen?
Zur Charakterisierung von Hirntumoren hat sich eine Methode etabliert, die nicht auf einer konventionellen mikroskopischen Diagnostik, sondern auf Modifikationen des Tumorerbguts, den epigenetischen Merkmalen, basiert. Sie gehören zum Gedächtnis einer jeden Zelle und bestimmen, welche Teile der Erbinformation wann abgelesen werden. „Hundertausende epigenetische Modifikationen fungieren als An- und Ausschalter einzelner Genabschnitte. Ihre Muster bilden einen unverwechselbaren Fingerabdruck“, erklärt PD Dr. Philipp Euskirchen, Wissenschaftler am Standort Berlin des Deutschen Konsortiums für translationale Krebsforschung (DKTK) und am Institut für Neuropathologie der Charité, Leiter der jetzt veröffentlichten Studie. „In Tumorzellen sind die epigenetischen Informationen auf jeweils charakteristische Weise verändert. Anhand ihrer Profile können wir Tumoren unterscheiden und sie klassifizieren.“ Im Fall von Hirntumoren genügt dazu in manchen Fällen sogar eine Probe des Nervenwassers, die vergleichsweise einfach gewonnen werden kann und keiner Operation bedarf.
Obwohl die Architektur unseres KI-Modells sehr viel einfacher ist als bisherige Ansätze und dadurch erklärbar bleibt, liefert es präzisere Vorhersagen und damit eine höhere diagnostische Sicherheit
Sören Lukassen
Um nun einen unbekannten Fingerabdruck mit Tausenden bekannter Fingerabdrücke verschiedener Krebserkrankungen zu vergleichen und einem bestimmten Tumortyp zuzuordnen, braucht es Methoden maschinellen Lernens, also Künstliche Intelligenz, denn die Daten sind sehr umfangreich und komplex. Hinzu kommt: In der Vergangenheit wurden unterschiedliche Methoden der DNA-Sequenzierung angewendet. Zudem beschränken sich epigenetische Analysen meist auf festgelegte, für einzelne Tumorarten typische Muster und Genabschnitte. „Unser Ziel war es daher, ein Modell zu entwickeln, das Tumoren genau klassifiziert, selbst wenn nur Teile des gesamten Tumor-Epigenoms zugrunde liegen oder die Profile mit unterschiedlichen Techniken und variierender Genauigkeit erhoben wurden“, sagt Bioinformatiker Dr. Sören Lukassen, Leiter der Arbeitsgruppe Medical Omics des Berlin Institute of Health in der Charité (BIH).
CrossNN heißt das neu entwickelte KI-Modell, dessen Architektur auf einem einfachen neuronalen Netzwerk beruht. Es wurde mit einer großen Anzahl an Referenztumoren trainiert und anschließend an mehr als 5000 Tumoren überprüft. „Unser Modell erlaubt in 99,1% aller Fälle eine sehr präzise Diagnosestellung von Hirntumoren und ist genauer als bisherige KI-Modelle“, sagt Philipp Euskirchen. „Darüber hinaus konnten wir auf gleiche Weise ein KI-Modell trainieren, das über 170 Tumorarten aus allen Organen mit einer Treffsicherheit von 97,8% unterscheiden kann. Damit lässt es sich über die relativ seltenen Hirntumoren hinaus für Krebserkrankungen aller Organe anwenden.“ Entscheidend für künftige Zulassungen in der klinischen Anwendung: Die Modelle sind vollständig erklärbar, das heißt, es ist nachvollziehbar, wie die Entscheidungen getroffen werden.
Der molekulare Fingerabdruck, den das KI-Modell zur Bestimmung erhält, kann aus einer Gewebeprobe oder aus Körperflüssigkeiten stammen. Schon jetzt bietet das Institut für Neuropathologie der Charité im Fall spezieller Hirntumoren eine nichtinvasive Diagnostik anhand von Nervenwasser, die sogenannte Liquid Biopsy, an. Sie erlaubt eine Diagnosestellung ohne belastende Operation auch in schwierigen Situationen. Profitiert hat davon unter anderem ein Patient, der sich mit dem Sehen von Doppelbildern vorgestellt hatte und bei dem ein ungünstig gelegener Hirntumor diagnostiziert wurde. „Wir haben das Hirnwasser mittels Nanopore-Sequenzierung, einer neuartigen, sehr schnellen und effizienten Form der Erbgutanalyse, untersucht. Die Klassifikation durch unsere Modelle ergab, dass es sich um ein Lymphom des zentralen Nervensystems handelte. Eine geeignete Chemotherapie konnte zeitnah begonnen werden“, schildert Philipp Euskirchen.
Die Genauigkeit der Methodik überraschte selbst die Forschenden. „Obwohl die Architektur unseres KI-Modells sehr viel einfacher ist als bisherige Ansätze und dadurch erklärbar bleibt, liefert es präzisere Vorhersagen und damit eine höhere diagnostische Sicherheit“, sagt Sören Lukassen. Das Forschungsteam plant daher zusammen mit dem DKTK klinische Studien mit crossNN an allen acht deutschen DKTK-Standorten. Darüber hinaus soll auch ein intraoperativer Einsatz erprobt werden. Ziel ist es, die exakte und vergleichsweise kostengünstige Tumorbestimmung anhand von DNA-Proben in die Routineversorgung zu übertragen.
Quelle: Charité – Universitätsmedizin Berlin
10.06.2025