Artikel • Leberintervention
Perspektiven der SIRT – wer profitiert und warum?
Die selektive interne Radiotherapie (SIRT) wird häufig nur in ihrer palliativen Dimension betrachtet. Inzwischen dringt das Verfahren allerdings zunehmend in den kurativen Bereich vor, wie Prof. Dr. Jens Ricke, Inhaber des Lehrstuhls für Radiologie an der Ludwig-Maximilians-Universität München und Direktor der Klinik und Poliklinik für Radiologie am Klinikum der LMU berichtet.
Bericht: Daniela Zimmermann

„Als lokoregionär eingesetztes Verfahren führt die SIRT maximal eine partielle Remission herbei und ist damit per definitionem kein heilendes Verfahren.“ Im Zusammenspiel mit weiteren Maßnahmen kann sie jedoch unter Umständen auch kurativ eingesetzt werden. „So bedienen wir uns der SIRT beispielsweise durchaus auch zur Hypertrophieinduktion vor Leberteilresektionen. Das so herbeigeführte Wachstum des unbehandelten Leberanteils bietet einen größeren Spielraum für die chirurgische Resektion – das ist ganz klar eine kurative Indikation.“ Zwar führen auch andere Verfahren wie die Pfortaderembolisation zur Hypertrophie, dabei geht jedoch wertvolle Zeit für die eigentliche Behandlung des Tumors verloren, weshalb der Vorteil deutlich bei der Radioembolisation liegt.
Ist die SIRT bei hepatozellulären Karzinomen (HCC) also eine Alternative zur systemischen Therapie mit Sorafenib? Das ist schwer zu beurteilen, sagt Ricke, denn die Datenlage ist bislang schwach. Zwar haben neuere Studien – die multizentrische SARAH-Studie in Frankreich und die asiatische SIRveNIB-Studie – ergeben, dass beide Verfahren eine vergleichbare Überlebensrate aufweisen. „Allerdings waren diese Studien nicht darauf angelegt, eine Nicht-Unterlegenheit zu beweisen“, betont der SIRT-Experte. „Da die Radioembolisation im Vergleich jedoch deutlich weniger Nebenwirkungen nach sich zieht und dadurch eine höhere Lebensqualität erzielt, haben wir für das Patientengespräch in der Ambulanz eine echte Option neben der Systemtherapie.“ Nicht zuletzt verschließt die SIRT auch nicht die Option auf eine anschließende systemische Therapie, wohingegen eine zuerst durchgeführte antiangiogene Sorafenib-Gabe die intraarterielle Aplikation des Y-90 behindern dürfte. Große Hoffnungen setzt Ricke daher auf eine von ihm organisierte Multicenter-Studie, SORAMIC aus Magdeburg, bei der die synergistischen Effekte der Sequenz SIRT gefolgt von systemischer Therapie mit Sorafenib untersucht werden. Deren Ergebnisse werden Anfang 2018 vorliegen.
Effektiv gegen rechte Tumoren, wirkungslos gegen linke
Jetzt fehlt uns nur noch die Erklärung, woran das liegt
Jens Ricke
Unklar ist die Situation auch bei kolorektalen Karzinomen. Eine sehr große internationale kumulative Studie, prospektiv und randomisiert mit mehr als 1.000 Patienten, ergab in der Erstlinie keine Überlebensverbesserung durch SIRT im Vergleich zur systemischen Chemotherapie. Interessantes und Unerwartetes fördern allerdings die Substudien zu Tage, so Ricke: „Offenbar spielt die Tumorlokalisation eine große Rolle: Die primär rechtsseitig im Darm gelegenen Tumoren profitieren außerordentlich von der SIRT, die linksseitigen dagegen nicht. Jetzt fehlt uns nur noch die Erklärung, woran das liegt.“
Vielversprechend sind zudem die Ergebnisse in der zweiten, dritten und vierten Linien bei fortgeschrittenen Krankheitsverläufen bei metastasiertem Darmkrebs. Ricke: „Gerade im palliativen Bereich, also in Salvage-Situationen, in denen der Patient die Chemotherapie nicht verträgt, eine Chemopause eingelegt werden soll, oder es keine weiteren Chemo-Optionen gibt, wird die SIRT in der Therapie des metastasierten kolorektalen Karzinoms eine große Rolle spielen.“ Prospektiv randomisierte Studien zu anderen metastasierten Tumoren fehlen derzeit. Sehr vielversprechend sind Ergebnisse von einarmigen Kohortenstudien bei neuroendokrinen und Mammakarzinomen. Aus den Phase-2-Daten geht hervor, dass ausgesuchte Patientinnen mit Mammakarzinom erheblich von der SIRT profitieren, bestätigt der Radiologe. „Bei funktionellen neuroendokrinen Karzinomen ist die Symptomlinderung häufig eindrucksvoll und besser als durch Chemoembolisation, genauso wie die Ansprechraten insbesondere in frühen Stadien. Es bedarf zur Validierung jedoch prospektiv randomisierter Studien, auch in der Erstliniensituation.“
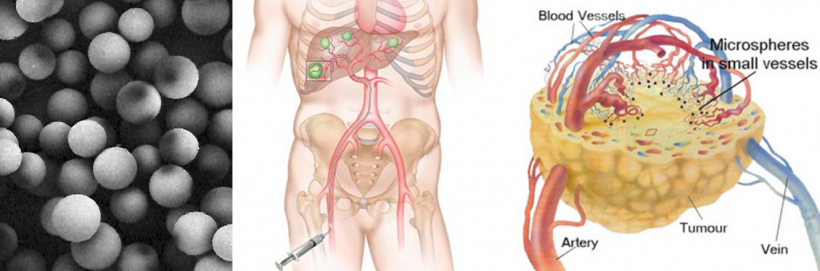
Deutliches Verbesserungspotenzial sieht Ricke vor allem hinsichtlich der Patientenselektion: „Welche Patienten profitieren wirklich von der SIRT? Derzeit können wir das leider nur im Nachhinein feststellen.“ Auch in der Dosimetrie eröffnet sich durch neue Forschungsergebnisse zusätzlicher Spielraum; sie erlaubt, die Strahlung gezielter und damit höher dosiert einzusetzen. Denn in der gezielten Anwendung liegt ohnehin eine der großen Stärken der Therapie mittels betastrahlender Kügelchen: „Das Gefäßnetz von Tumoren ist im Gegensatz zum gesunden Lebergewebe völlig atypisch“, erklärt Ricke. „Durch diese veränderte Struktur nimmt das gesunde Parenchym deutlich weniger Kügelchen auf als die Tumoren. Diese Ratio fällt bei der großen Mehrheit der Patienten sehr vorteilhaft aus, so dass ein gezieltes Bestrahlen der Tumoren möglich ist. Durch Modifikation der Strahlendosis wird die SIRT zu einem Präzisionsinstrument. „Wenn die ganze Dosis auf wenige Lebersegmente konzentriert wird, kommt das einer chirurgischen Entfernung eines Tumors gleich“, so Ricke abschließend.
Profil:
Prof. Dr. Jens Ricke, Facharzt für Radiologie, habilitierte an der Charité, Universitätsmedizin Berlin. Dort hatte er zwischen 2004 und 2006 eine C3-Professur für Interventionelle Radiologie an der Klinik für Strahlenheilkunde inne. Von 2006 bis 2017 war Ricke Lehrstuhlinhaber Radiologie an der Otto-von-Guericke-Universität Magdeburg sowie Direktor der Klinik für Radiologie und Nuklearmedizin am Universitätsklinikum Magdeburg. Im Juni 2017 wechselte er an die Ludwig-Maximilians-Universität München, wo er den Lehrstuhl für Radiologie innehat und als Direktor der Klinik und Poliklinik für Radiologie tätig ist.
29.09.2017