Bildquelle: Helmholtz Munich / T. Vitadello
News • Deep-Learning-Modell DeepNeo
KI erleichtert die Nachsorge nach Stent-OP
Ein Forschungsteam von Helmholtz Munich, der Technischen Universität München (TUM) und dem TUM Klinikum hat DeepNeo entwickelt – einen KI-basierten Algorithmus, der die Analyse von koronaren Stents nach der Implantation automatisiert.
Das Tool erreicht die Präzision medizinischer Fachkräfte und verkürzt gleichzeitig die Auswertungszeit erheblich. Dank umfassender Validierung in Human- und Tiermodellen hat DeepNeo das Potenzial, die Nachsorge nach Stent-OPs zu standardisieren – und so die Behandlungsergebnisse bei Herz-Kreislauf-Erkrankungen nachhaltig zu verbessern.
Die Forscher haben ihre Erkenntnisse im Fachjournal Nature Communications Medicine veröffentlicht.
Jährlich werden weltweit mehr als drei Millionen Menschen mit Stents behandelt, um durch Herzkrankheiten verengte Blutgefäße zu öffnen. Die Überwachung des Heilungsprozesses nach der Implantation stellt jedoch nach wie vor eine Herausforderung dar. Entwickelt sich das Gewebe, das über den Stent wächst, unregelmäßig – sei es zu dick oder mit Ablagerungen –, kann dies zu Komplikationen wie einer erneuten Verengung oder Verstopfung des Blutgefäßes führen. Derzeit ist die Analyse dieser Heilungsmuster in intravaskulären optischen Kohärenztomographie (OCT)-Bildern zeitaufwendig und für die routinemäßige klinische Praxis schwer umsetzbar.
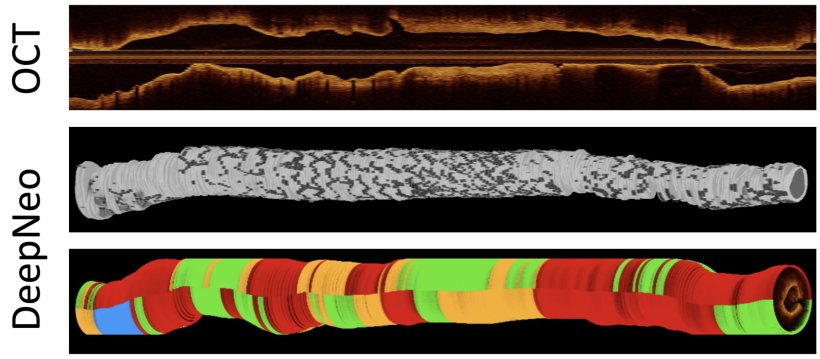
Bildquelle: Helmholtz Munich / Valentin Koch
Ein Forschungsteam von Helmholtz Munich und dem TUM Klinikum hat mit DeepNeo einen KI-Algorithmus entwickelt, der die Heilung von Stents in OCT-Bildern automatisch beurteilen kann. DeepNeo erkennt verschiedene Heilungsmuster mit einer Genauigkeit, die der klinischer Expert:innen entspricht – jedoch in einem Bruchteil der Zeit. Darüber hinaus liefert das KI-Tool präzise Messdaten, etwa zur Gewebedicke und zur Abdeckung des Stents, und bietet so wertvolle Einblicke für das Patientenmanagement. „Mit DeepNeo erreichen wir eine automatisierte, standardisierte und äußerst präzise Analyse der Stent- und Gefäßheilung – etwas, das bislang nur durch aufwendige manuelle Auswertung möglich war“, sagt Valentin Koch, Erstautor der Studie, in der der Algorithmus vorgestellt wurde. „DeepNeo ist so gut wie ein Arzt – nur viel schneller.“
DeepNeo zeigt, wie maschinelles Lernen Ärzte dabei unterstützen kann, schneller und fundierter Therapieentscheidungen zu treffen
Carsten Marr
Für das Training von DeepNeo nutzte das Forschungsteam 1.148 OCT-Bilder aus 92 Patientenscans, die manuell annotiert wurden, um verschiedene Formen des Gewebewachstums zu klassifizieren. Anschließend wurde der KI-Algorithmus in einem Tiermodell getestet – mit überzeugendem Ergebnis: DeepNeo identifizierte krankhaftes Gewebe in 87% der Fälle korrekt, verglichen mit der detaillierten Laboranalyse, dem aktuellen Goldstandard. Auch bei der Auswertung menschlicher Scans zeigte DeepNeo eine hohe Präzision und stimmte eng mit den Einschätzungen medizinischer Fachkräfte überein. „DeepNeo zeigt, wie maschinelles Lernen Ärzte dabei unterstützen kann, schneller und fundierter Therapieentscheidungen zu treffen. Der nächste Schritt besteht nun darin, KI-Algorithmen wie DeepNeo gezielt in die klinische Praxis zu integrieren“, erklärt Dr. Carsten Marr, Direktor des Institute of AI for Health bei Helmholtz Munich.
Seine Kollegin Prof. Julia Schnabel, Leiterin des Instituts für Maschinelles Lernen in der Biomedizinischen Bildgebung und Professorin für Computational Imaging und Künstliche Intelligenz in der Medizin an der TUM, sieht in DeepNeo einen Baustein für ein KI-gestütztes Gesundheitssystem, das künftig klinische Entscheidungen mit bislang unerreichter Sicherheit unterstützen könnte.
Das Projekt wurde mit einem Helmholtz Innovation Grant gefördert, eine Patentanmeldung ist bereits eingereicht. Ascenion, der Technologietransfer-Partner im Bereich Life Sciences, unterstützt das DeepNeo-Team bei der Suche nach potenziellen Industriepartnern. „DeepNeo erleichtert und standardisiert die Auswertung von OCT-Bildgebungen nach Stentimplantationen und trägt so zu fundierteren klinischen Entscheidungen bei“, sagen PD Dr. Philipp Nicol und Prof. Dr. Michael Joner, Kardiologen am TUM Klinikum, die das Projekt klinisch begleitet haben. „Das Verfahren hat das Potenzial, nicht nur die Gesundheitskosten zu senken, sondern auch den Weg für effektivere und personalisierte kardiovaskuläre Therapien zu ebnen.“
Quelle: Helmholtz Munich
24.04.2025