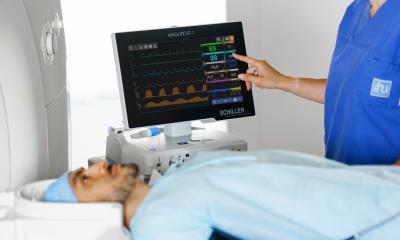
Endoprothesenregister für verbesserte Versorgungsforschung und Qualitätssicherung
Die im BVMed vereinten Hersteller von Hüft- und Knieimplantaten unterstützen eine schnelle Einrichtung eines Endoprothesenregisters als weiteren Baustein zur Sicherstellung und Optimierung der Qualität der Patientenversorgung. Das sagte BVMed-Geschäftsführer und Vorstandsmitglied Joachim M. Schmitt vor dem Hintergrund aktueller Medienberichte über die bevorstehende Einrichtung eines Registers.
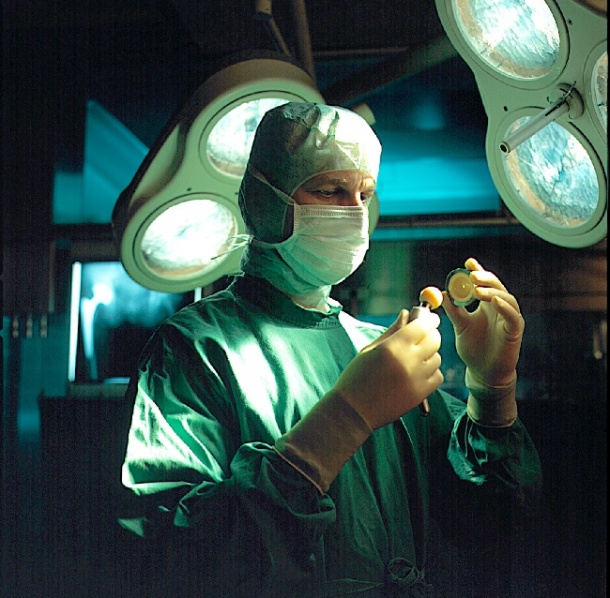
Für die Einrichtung eines Endoprothesenregisters ist die Zusammenführung von drei unterschiedlichen Datensätzen erforderlich: die Routinedaten der Krankenhäuser, die pseudonymisierten Patientendaten der Krankenkassen sowie die Produktdaten der Implantatehersteller. Die BVMed-Mitgliedsunternehmen stellen sich ihrer Verantwortung und sind bereit, die erforderlichen Herstellerdaten zur Verfügung zu stellen und den Aufbau der Implantate-Referenzdatenbank inhaltlich zu begleiten und entsprechend zu finanzieren. Der BVMed verweist darauf, dass seit mehreren Jahren entsprechende Zusagen der Industrie schriftlich vorliegen.
Wesentliche Grundlage für den Erfolg eines Registers ist aus Sicht der Industrie, dass es sich insgesamt um ein unabhängiges Register handelt und die ausgewerteten Daten durch die Sicherstellung der Neutralität eine entsprechende Aussagekraft haben. Daher ist die Zusammenführung der Daten, das Betreiben und die Auswertung des Endoprothesenregisters von den anderen Beteiligten zu finanzieren.
Schon heute gibt es in 19 Ländern, darunter Schweden und Australien, Endoprothesenregister, die in der Regel von den nationalen orthopädischen Fachgesellschaften verwaltet und über die Regierung, in Ausnahmefällen zusätzlich von den Fachgesellschaften finanziert werden. „Sie sind nicht nur für die Medizin und die Kostenträger sondern auch für die forschende Implantateindustrie ein wichtiges Zusatzinstrument zur Qualitätssicherung der jeweiligen Technologie und verfügen über ein großes Nutzenpotential hinsichtlich der Verlängerung der Überlebensrate von Implantaten – zum Wohle der Patienten“, so der BVMed.
Wichtig ist dem BVMed eine angemessene Einbindung der medizinischen Fachgesellschaften und der Expertise der Hersteller in die Entwicklung der Qualitätsparameter und Auswertungen der Registerdaten. Darüber hinaus müssen die Ergebnisse den meldenden Firmen und Krankenhäusern umfänglich und zeitnah zur Verfügung gestellt werden. Nur so kann sichergestellt werden, dass etwaige Auffälligkeiten frühzeitig erkannt und schnell die erforderlichen Maßnahmen getroffen werden können.
Bildquelle: CeramTec AG Geschäftsbereich Medizintechnik
23.09.2010