Quelle: Fotolia
News • DNA unter der Lupe
Die Zukunft der Medikation liegt in der Datenanalyse
Medikamente sollen wirken – und das möglichst gezielt. Aber jeder menschliche Körper verarbeitet Medikamente anders. Wie das Startup BioVariance GmbH mithilfe genetischer Daten und einer neuen Software die Wirkung von Arzneimitteln optimiert.
In den letzten Jahren hat sich der Fortschritt in der Genomanalyse, also dem Verfahren der Entschlüsselung des Erbguts, erheblich beschleunigt. Während noch bis vor wenigen Jahren die Analyse eines einzigen Gens viele Jahre dauern konnte, lässt sich heute mithilfe digitaler Prozesse das gesamte Erbgut tausender Patienten gleichzeitig und binnen weniger Tage untersuchen – für einzelne Patienten sogar binnen Stunden.
Trotz intensiver medizinischer Forschung reagiert jeder Mensch unterschiedlich auf ein und dasselbe Medikament
Josef Scheiber
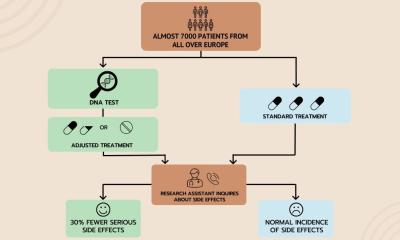
Es ist dieser Fortschritt, den sich das junge Unternehmen BioVariance aus dem bayrischen Waldsassen zu Nutze gemacht hat. Im Jahr 2013 von dem Biologen Dr. Josef Scheiber gegründet, hat sich das Startup auf die Verbesserung der Verträglichkeit und Wirksamkeit von Arzneimitteln spezialisiert. „Trotz intensiver medizinischer Forschung reagiert jeder Mensch unterschiedlich auf ein und dasselbe Medikament“, sagt Scheiber. Studien haben ergeben, dass vielen Patienten die falschen Medikamente verschrieben werden. In einer Vorabstudie des Instituts für Allgemeinmedizin der Universität Witten/Herdecke wiesen über 90 Prozent der Patienten, die im Schnitt 9 Medikamente einnahmen, mindestens eine unbegründete Arzneimittelverschreibung auf. Zudem ergab die Studie, dass 37 Prozent der über 65-jährigen Probanden Medikamente erhielten, die älteren Menschen nicht verordnet werden sollten.
Dieser Artikel könnte Sie auch interessieren
News • Studie
Polypharmazie und Übermedikation sind Seniorenprobleme
Zwischen 12.000 und 58.000 Patienten werden Hochrechnungen zufolge jährlich in Deutschland durch unerwünschte Arzneimittelwirkungen (UAW) dauerhaft geschädigt oder sterben. Zudem sollen in Deutschland etwa 1,5 Prozent aller Klinikeinweisungen im Zusammenhang mit UAW stehen, von denen insbesondere Menschen betroffen sind, die polypharmazeutisch behandelt werden.
Für jeden Patienten das richtige Medikament
Ziel von BioVariance ist es, Ärzte und Apotheker mithilfe einer umfassenden Genomanalyse bei der Medikamentenauswahl zu unterstützen. „Jeder Mensch verarbeitet Medikamente anders und unterschiedlich schnell. Diese Unterschiede spiegeln sich unter anderem in der DNA wieder, aber es spielen auch andere Faktoren wie Geschlecht, Größe, Gewicht, Alter und Ernährung eine Rolle“, sagt Scheiber. „Bei der genetischen Datenanalyse geht es deshalb im Kern um die individuelle Anpassung der Behandlung an die Bedürfnisse des Patienten.“
Der Ablauf einer BioVariance Datenanalyse ist praxisorientiert. Ein Beispiel: Ein Krankenhaus beauftragt BioVariance damit, die Genomanalyse eines Krebspatienten durchzuführen. BioVariance sammelt zunächst die nötigen Rohdaten des Patienten, darunter auch Erbinformationen aus Blutproben, die der Patient dem Unternehmen über den Arzt zur Verfügung stellt. Im ersten Schritt erfolgt eine Analyse der genetischen Daten. BioVariance identifiziert dabei alle pathogenen beziehungsweise genetischen Varianten des Patienten, um alle relevanten Informationen personalisieren zu können. Im Anschluss gleicht BioVariance den Wirkstoff mit allen relevanten Parametern und Stoffwechseleigenschaften des Patienten ab. Aus der durchgeführten Genomanalyse errechnet ein Algorithmus unter Berücksichtigung aktueller klinischer Studien und Forschungsergebnisse dann die Wirksamkeit eines bestimmten Medikaments.
Aus Big Data wird Smart Data
Datenmengen bringen uns nichts, wenn wir keinen Mehrwert daraus generieren können. Die Interpretation dieser Daten ist am Ende das Entscheidende
Josef Scheiber
„Am Ende unserer Analyse erstellen wir einen umfassenden Report mit individualisierten Vorschlägen für die Medikation“, sagt Scheiber. „Der Report enthält nicht nur das Ergebnis, sondern auch die individuell berücksichtigten Eigenschaften und DNA-Marker.“ Der Analyseprozess ist grundsätzlich auf alle Arten von Erkrankungen und für jegliche Medikamententypen anwendbar. Da der Biologe früher selbst auf dem Gebiet der biomedizinischen Informatik tätig war, spielt die Auswertung von Daten für ihn eine besondere Rolle. „Schon damals wollte ich aus Big Data intelligente Daten erstellen, die dem Patienten einen Mehrwert bieten. Datenmengen bringen uns nichts, wenn wir keinen Mehrwert daraus generieren können. Die Interpretation dieser Daten ist am Ende das Entscheidende“, erklärt Scheiber.
Quelle: BioVariance
06.12.2018