
Bildquelle: Leiden University Medical Center (LUMC)
News • Individueller Medikamentenpass
DNA-personalisierte Medikation verringert Nebenwirkungen
Patienten haben 30% weniger schwere Nebenwirkungen, wenn die Medikamentendosis auf ihre genetische Ausstattung angepasst ist. Das hat ein internationales Forschungskonsortium herausgefunden, zu dem auch das Dr. Margarete Fischer-Bosch-Institut für Klinische Pharmakologie am Bosch Health Campus gehört.
Der Ansatz „One-size-fits-all“ (eine Einheitsgröße für alle) ist als allgemeines Prinzip bei der Verschreibung von Medikamenten überholt. Denn aufgrund von Unterschieden in ihrer genetischen Ausstattung können Patienten verschieden auf Medikamente reagieren. So bauen manche Menschen Medikamente sehr verzögert ab und benötigen daher eine niedrigere Dosis, um Nebenwirkungen zu vermeiden. Personalisierte Arzneimitteltherapien sind somit empfehlenswert. Um diese zu ermöglichen, haben die Forschenden einen „DNA-Medikamentenpass“ entwickelt, der die genetische Ausstattung von Patienten mit Medikamenten verknüpft. Die Lancet-Studie ergab, dass Patienten, die den Medikamentenpass aktiv nutzen und deren Dosis entsprechend ihrer DNA angepasst war, 30% weniger schwerwiegende Nebenwirkungen hatten als solche, denen eine Standarddosis verschrieben worden war.
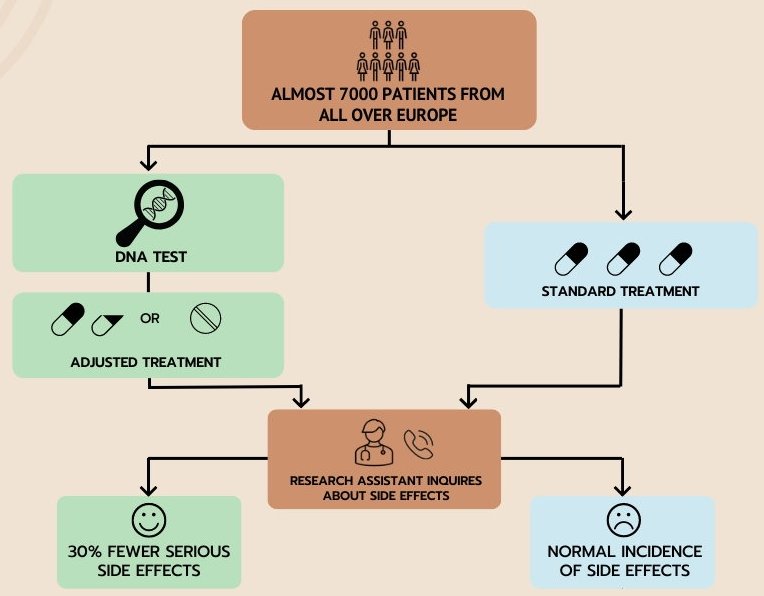
Bildquelle: Leiden University Medical Center (LUMC)
Rund 7000 Patienten aus sieben europäischen Ländern haben an der Studie teilgenommen, die verschiedene medizinische Bereiche berücksichtigte, wie die Onkologie, Kardiologie, Psychiatrie und Allgemeinmedizin. Die Forschenden untersuchten zwölf ausgewählte Gene, für die bereits ein Zusammenhang mit Medikamenten bekannt war. Es zeigte sich, dass 50 Arten von Genvarianten die Wirkung von 39 ausgewählten Medikamenten beeinflussen. Nach der Verschreibung der Medikamente wurden die Patienten weiter begleitet, um eventuelle Nebenwirkungen, wie Muskelschmerzen, Blutbildveränderungen, Durchfall oder Infektionen zu erfassen. Diejenigen, die eine an ihre spezifischen Erbinformationen angepasste Dosierung erhielten, zeigten weniger Nebenwirkungen. Die Verwendung eines DNA-Medikamentenpasses wurde von den Patienten zudem positiv aufgenommen, weil sie das Gefühl hatten, aktiv an ihrer Behandlung beteiligt zu sein.

Bildquelle: Leiden University Medical Center (LUMC)
„Zum ersten Mal haben wir gezeigt, dass eine ‚maßgeschneiderte‘ Strategie in großem Maßstab in der klinischen Praxis funktioniert. Wir haben nun genügend Belege, um mit der Umsetzung zu beginnen“, sagt Henk-Jan Guchelaar vom Leiden University Medical Center. Matthias Schwab, Leiter des IKP am Bosch Health Campus ergänzt: „Die Studie belegt, dass eine genetische Testung zur Vermeidung von Nebenwirkungen von Ärzt:innen, der beteiligten Apotheker:innen und vor allem von Patient:innen sehr gut angenommen wird.“
Mit dem Pass können Ärzte ihre Patienten künftig individualisiert behandeln, das heißt eine auf sie zugeschnittene Dosierung der Medikamente auswählen. Die Forschenden gehen davon aus, dass eine Übernahme der Kosten für personalisierte Arzneimitteltherapien durch die Krankenkassen aufgrund der Studienergebnisse erleichtert wird. „Auf diese Weise können wir die Behandlung für jeden Einzelnen wirksamer und sicherer machen“, so Guchelaar.
Quelle: Bosch Health Campus
06.02.2023





