News • NUFIP-2
Adaptive Immunantwort: Neuer Kofaktor von Roquin identifiziert
Das Protein Roquin hat eine Schlüsselrolle in der adaptiven Immunantwort. So kontrolliert es maßgeblich die Aktivierung und Differenzierung von T-Zellen und beeinflusst damit entscheidend die Immunabwehr.
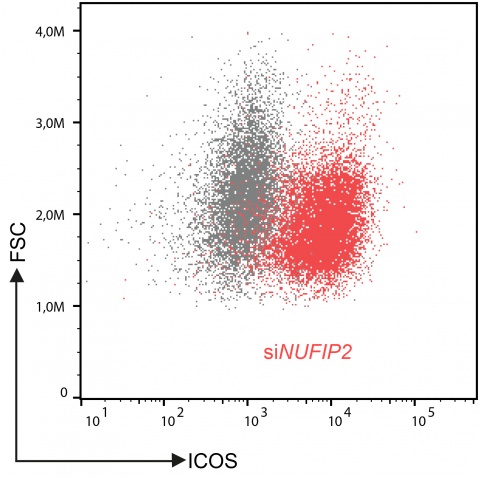
Jetzt hat ein Wissenschaftlerteam des Helmholtz Zentrums München in Kooperation mit Wissenschaftlern der Ludwig-Maximilians-Universität und dem Helmholtz Zentrum für Umweltforschung in Leipzig NUFIP2, ein Protein mit bislang unbekannter Funktion, als Kofaktor Roquins identifiziert und aufgedeckt, dass NUFIP2 die regulatorische Funktion Roquins verstärkt.
In früheren Studien konnte die Forschergruppe um Prof. Dr. Vigo Heissmeyer, Leiter der Abteilung für Molekulare Immunregulation (AMIR) am Helmholtz Zentrum München und Professor an der Ludwig-Maximilians-Universität (LMU), in Zusammenarbeit mit Forschergruppen des Instituts für Strukturbiologie (STB) nachweisen, dass Roquin mit seiner ROQ-Domäne an gefaltete Bereiche der 3’UTR bestimmter mRNAs bindet. Dabei wird sowohl eine spontane Aktivierung von T-Zellen vermindert, als auch nach der Aktivierung Differenzierungsentscheidungen gesteuert. Das begrenzt Immunantworten auf spezifische Reaktionen und verhindert Entzündungsreaktionen in Abwesenheit von Erregern. Nun ist klar, dass Roquin diese Aufgaben nicht allein erfüllt. „Wir haben jetzt entdeckt, dass Roquin mit NUFIP2 als neuem Kofaktor den mRNA-Abbau bewerkstelligt“, sagt Heissmeyer. „NUFIP2 verstärkt in seiner Wirkung als Kofaktor von Roquin das Erkennen und Regulieren von mRNA-Transkripten, wodurch weniger kostimulatorische Rezeptoren produziert werden und die Immunantwort gedämpft wird“, fügt Prof. Dr. Dierk Niessing, Arbeitsgruppenleiter am STB hinzu.
Wir hoffen mit unserer Forschung einen weiteren Schritt zum besseren Verständnis der Immunantwort und somit auch zu neuen Therapien beitragen zu können
Vigo Heissmeyer
„Das von mir in einem Hochdurchsatz-Screen identifizierte NUFIP2 Protein bindet direkt und mit hoher Affinität an Roquin und verändert damit die Roquin-vermittelte Erkennung von Ziel-mRNAs. Diese Bindung stabilisiert im Gegenzug NUFIP2 in der Zelle“ sagt Nina Rehage, frühere Doktorandin des Helmholtz Zentrum München. „Insbesondere für ICOS und Ox40 konnten wir nachweisen, dass der Komplex aus NUFIP2 und Roquin das Erkennen von unkonventionellen Tandemstrukturen in den 3’UTRs verstärkt. ICOS und Ox40 sind kostimulatorische Rezeptoren für T-Zellen und damit wichtig für das Entstehen und die Art einer effizienten Immunantwort. Ihre Regulation ist daher von großer Bedeutung.“ erläutern Elena Davydova, Doktorandin am STB, und Christine Conrad, Doktorandin an der Ludwig-Maximilians-Universität.
Da T-Lymphozyten an vielen Krankheiten, insbesondere Autoimmunerkrankungen, Allergien und chronischen Entzündungsreaktionen beteiligt sind, liegt der Schlüssel zu neuen Therapiemöglichkeiten in der Kenntnis der molekularen Mechanismen. „Wir hoffen mit unserer Forschung einen weiteren Schritt zum besseren Verständnis der Immunantwort und somit auch zu neuen Therapien beitragen zu können“, sagt Heissmeyer.
Quelle: Helmholtz Zentrum München - Deutsches Forschungszentrum für Gesundheit und Umwelt
20.01.2018