Bildquelle: Yimo Yan / ETH Zürich
News • Lebende Mikroroboter
Magnetische Bakterien im Einsatz gegen Krebs
Forschende der ETH Zürich möchten magnetische Bakterien zur Bekämpfung von Krebsgeschwüren nutzen. Sie haben nun einen Weg gefunden, wie die Mikroorganismen die Blutgefäßwand gut durchdringen und anschließend einen Tumor besiedeln können.
Wissenschaftler weltweit erforschen, wie Krebsmedikamente am effizientesten zu Tumoren gelangen, wo sie ihre Wirkung entfalten sollen. Eine Möglichkeit ist, veränderte Bakterien als Fähren zu benutzen, welche die Wirkstoffe durch die Blutbahn hin zu den Tumoren transportieren. Forschende an der ETH Zürich haben es nun geschafft, bestimmte Bakterien so zu steuern, dass sie effizient die Blutgefäßwand durchdringen und ins Tumorgewebe eindringen können. Als Modellbakterien nutzten die Forschenden um Simone Schürle, Professorin für reaktionsfähige biomedizinische Systeme, solche, die natürlicherweise magnetisch sind, weil sie Eisenoxid-Partikel enthalten. Diese Bakterien der Gattung Magnetospirillum reagieren auf Magnetfelder und können von außerhalb des Körpers mit Magneten gesteuert werden.
Das Team veröffentlichte seine Erkenntnisse jetzt im Fachjournal Science Robotics.

Bildquelle: ETH Zürich / Giulia Marthaler
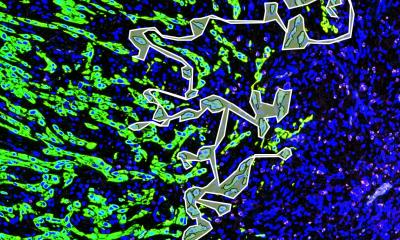
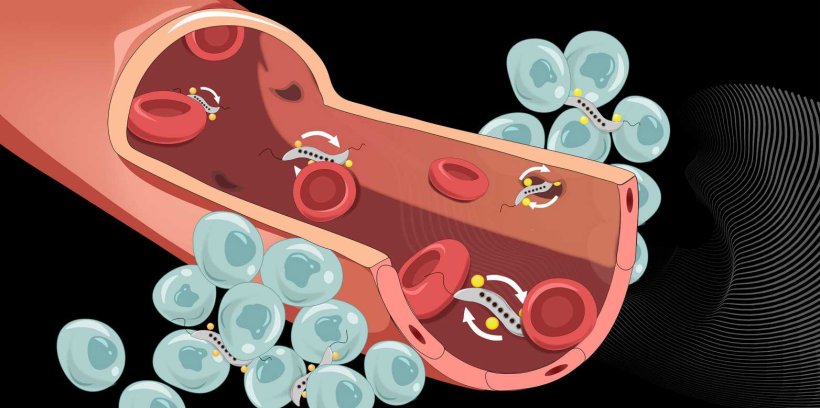
Schürle und ihr Team haben nun in Zellkultur und in Mäusen gezeigt: Ein auf den Tumor gerichtetes rotierendes Magnetfeld eignet sich besonders gut, dass die Bakterien die Blutgefäßwand in Tumornähe durchdringen. An der Gefäßwand treibt das rotierende Magnetfeld die Bakterien zu einer vorwärts gerichteten Drehbewegung an. Um das Durchdringen der Gefäßwand besser zu verstehen, ist ein detaillierter Blick auf diese nötig: Die Blutgefäßwand ist die Barriere zwischen der Blutbahn und dem Tumorgewebe, das von vielen feinen Blutgefäßen durchzogen ist. Sie besteht aus einer Schicht von Zellen. Bestimmte Moleküle aus dem Blutstrom können durch die engen Zwischenräume zwischen den Zellen schlüpfen und damit die Gefäßwand passieren. Wie groß der Zellzwischenraum ist, wird von den Gefäßwandzellen reguliert. Vorübergehend können die Zellen den Zwischenraum auch so weit öffnen, dass andere Zellen (und damit auch Bakterien) die Gefäßwand passieren können.
Ein Antrieb der Bakterien über ein rotierendes Magnetfeld ist aus drei Gründen wirksam, wie die ETH-Forschenden mit Experimenten und Computersimulationen zeigen konnten. Erstens ist diese Antriebsart besonders stark, so dass sich die Bakterien besonders gut durch die engen Zellzwischenräume zwängen können. Der Antrieb über ein rotierendes Magnetfeld ist zehnmal stärker als ein Antrieb über ein statisches Magnetfeld, das nur die Richtung vorgibt und bei dem sich die Bakterien mit eigener Kraft fortbewegen müssen.
Wir nutzen auch die natürliche und autonome Fortbewegung der Bakterien. Haben die Bakterien die Blutgefäßwand einmal passiert und sind sie im Tumor, können sie autonom tief in ihn eindringen
Simone Schürle
Zweitens sind die durch das Rotationsfeld angetriebenen Bakterien ständig in Bewegung; sie tänzeln der Blutgefäßwand entlang. Dadurch ist die Wahrscheinlichkeit, dass sie auf eine sich kurz öffnende Lücke zwischen den Gefäßwandzellen treffen, höher als bei den anderen Antriebsarten, bei denen sich die Bakterien weniger dynamisch bewegen. Und drittens müssen die Bakterien im Gegensatz zu anderen Methoden für die Steuerung nicht über Bildgebung nachverfolgt werden. Ist das Magnetfeld einmal auf den Tumor ausgerichtet, werden vorbeiströmende Bakterien vom Magnetfeld erfasst. "Wir nutzen auch die natürliche und autonome Fortbewegung der Bakterien", erklärt ETH-Professorin Schürle. "Haben die Bakterien die Blutgefäßwand einmal passiert und sind sie im Tumor, können sie autonom tief in ihn eindringen." Den Antrieb über das externe Magnetfeld nutzen die Wissenschafter daher nur während einer Stunde, damit die Bakterien die Gefäßwand effizient überwinden und den Tumor erreichen können.
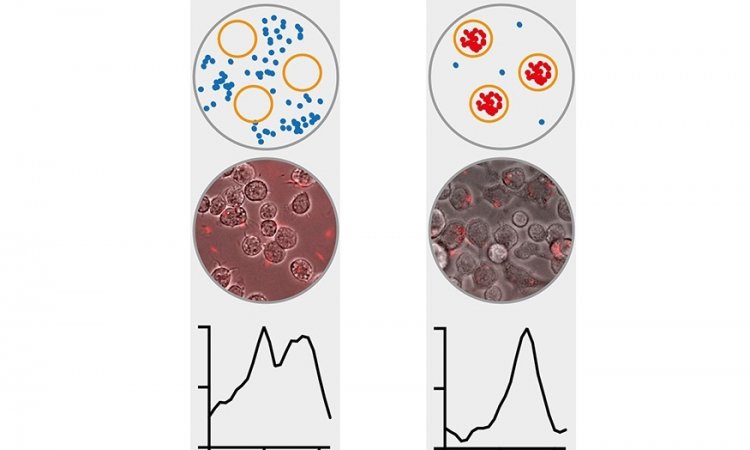
In Zukunft könnten solche Bakterien mit Krebsmedikamenten beladen werden. Im Rahmen ihrer Zellkulturstudien simulierten die ETH-Forschenden dies mittels Liposomen (Nanobläschen aus fettartigen Stoffen), die sie den Bakterien anhängten. Diese Liposomen waren mit einem fluoreszierenden Farbstoff gefüllt. Auf diese Weise konnten die Wissenschaftler in der Petrischale nachweisen, dass die Bakterien ihre Fracht tatsächlich ins Innere von Krebsgewebe gebracht haben, wo sie sich anreicherte. In einer künftigen medizinischen Anwendung würde statt des Farbstoffs ein Medikament verwendet.
Der hier verfolgte Ansatz, Bakterien als Fähren für Wirkstoffe zu nutzen, ist nur einer von zwei Möglichkeiten zur Verwendung von Bakterien in der Krebsmedizin. In der Wissenschaft erlebt derzeit ein weiterer, über hundert Jahre alter Ansatz ein Revival: Bakterien bestimmter Arten können Tumore schädigen. Möglicherweise sind mehrere Wirkmechanismen daran beteiligt. Bekannt ist jedenfalls, dass die Bakterien bestimmte Zellen des Immunsystems anregen, die dann gegen den Tumor vorgehen. Derzeit gibt es mehrere Forschungsprojekte, in denen die Wirksamkeit von Bakterien der Art Escherichia coli gegenüber Tumoren untersucht werden. Heute ist es möglich, die Bakterien mittels synthetischer Biologie zu verändern, um ihre therapeutische Wirkung zu optimieren, Nebenwirkungen zu reduzieren und die Sicherheit zu erhöhen.
Doch auch wenn man die inhärenten Eigenschaften von Bakterien in der Krebstherapie nutzen möchte, stellt sich die Frage, wie diese Bakterien effizient zu einem Tumor gelangen. Bei Krebsgeschwüren nahe der Körperoberfläche ist es möglich, die Bakterien in den Tumor zu injizieren. Bei solchen tief im Köperinnern wird das schwierig. Hier kommt die Mikrorobotik von Prof. Schürle ins Spiel. "Wir denken, dass wir mit unserem Ingenieur-Ansatz die Wirksamkeit der bakteriellen Krebstherapie erhöhen können", sagt sie.
Die in den Krebsstudien verwendeten Bakterien der Art Escherichia coli sind nicht magnetisch und lassen sich daher nicht über ein Magnetfeld antreiben und steuern. Überhaupt ist Magnetismus unter Bakterien ein sehr seltenes Phänomen. Magnetospirillum ist eine der wenigen Bakteriengattungen, welche diese Eigenschaft haben. Schürle möchte daher auch Escherichia-coli-Bakterien magnetisch machen. Damit könnte es dereinst möglich sein, medizinisch wirksame Bakterien ohne natürlichen Magnetismus über ein Magnetfeld zu steuern.
Quelle: ETH Zürich
28.10.2022