News • Ewing-Sarkom
Knochenkrebs: Forscher finden Tumor-Schwachstelle
Forscher in München zeigen, dass das Ewing-Sarkom in einen speziellen Signalweg in der Knochenentwicklung eingreift – und sich damit angreifbar macht. Dies könnte vor allem bei hochaggressiven Tumoren neue therapeutische Möglichkeiten eröffnen.
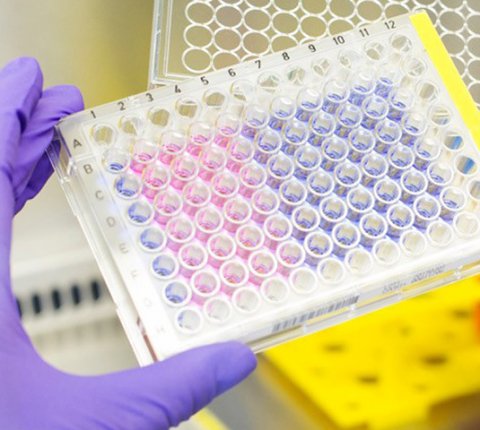
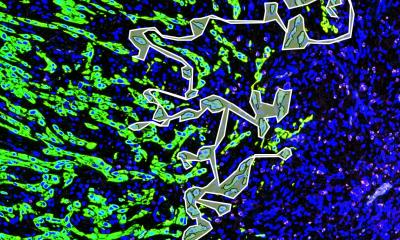
Foto: Judith Glaubitz / LMU
Ewing-Sarkome sind die zweithäufigsten bösartigen Knochentumoren bei Kindern und Jugendlichen. Am Anfang der Erkrankung steht eine einzige spontane Mutation, durch die ein sogenanntes Fusions-Onkogen entsteht. Dieses Fusions-Onkogen aktiviert weitere Gene und setzt einen Prozess in Gang, der den Krebs auslösen kann. In welchem Ausmaß dies geschieht, bestimmen angeborene genetische Variabilitäten der Patienten, sodass es zu unterschiedlich starkem Tumorwachstum kommt. Wissenschaftler der Ludwig-Maximilians-Universität München (LMU) um Thomas Grünewald, Leiter der Max-Eder Nachwuchsgruppe für Pädiatrische Sarkombiologie am Pathologischen Institut der LMU und Abteilungsleiter am Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg, konnten nun zeigen, dass eines der durch das Fusions-Onkogen aktivierten Gene an der Knochenentwicklung beteiligt ist – und dass die Überaktivierung dieses Gens einen vielversprechenden Ansatzpunkt für neue Therapien darstellt. Über die Ergebnisse des insbesondere von der Deutschen Krebshilfe geförderten Projekts berichten die Wissenschaftler im Fachmagazin Nature Communications.
Derzeitige Therapiestrategien können nicht verhindern, dass es bei etwa einem Drittel der Patienten mit Ewing-Sarkom zu Rückfällen mit oft fatalem Ausgang kommt. Grünewald sucht deshalb nach neuen therapeutischen Optionen. „Das Fusions-Onkogen selbst ist aus verschiedenen Gründen keine geeignete Zielstruktur. Deshalb versuchen wir, sogenannte Surrogat-Targets zu finden. Das sind beispielsweise Gene, die durch das Fusions-Onkogen aktiviert werden“, sagt Grünewald. „Wir haben uns dabei auf Gene fokussiert, die in der natürlichen Knochenentwicklung eine Rolle spielen, und festgestellt, dass das Gen SOX6 im Ewing-Sarkom hochreguliert ist.“ Dieses Gen ist normalerweise nur kurze Zeit während des Knochenwachstums aktiv und bewirkt dann eine massive Zellteilung. „Als wir das Gen in Ewing-Sarkom-Zelllinien ausschalteten, ging das Tumorwachstum in unseren Modellsystemen signifikant zurück. Wir gehen davon aus, dass SOX6 durch das Fusions-Onkogen dauerhaft aktiviert wird, sodass sich die Ewing-Zellen stark vermehren“, sagt Grünewald.
Dieser Artikel könnte Sie auch interessieren
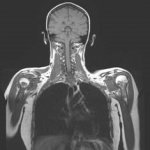
Artikel • Verfahrensfragen
Ganzkörper-MRT bei Knochenmetastasen: unschlagbar, aber …
Knochenmetastasen gehören zu den schwerwiegendsten Spätkomplikation vieler Tumorerkrankungen. Lange galt die Skelettszintigraphie als Goldstandard zur Detektion solcher Knochenmetastasen. Doch Prof. Dr. Andrea Baur-Melnyk plädiert für die Ganzkörper-MRT, da sie „Knochenherde und Organmetastasierungen früher und besser erkennen kann“.
Dass der Tumor den SOX6-Signalweg für seine Zwecke nutzt, birgt allerdings auch eine Chance für die Patienten: Das Gen greift auch in den Stresshaushalt der Zelle ein, sodass Zellen mit hochreguliertem SOX6 höhere Level reaktiver Sauerstoffspezies (ROS) aufweisen als andere Zellen. Dies wiederum macht die Zellen besonders empfindlich gegenüber dem Wirkstoff Elesclomol. Die Substanz wurde ursprünglich zur Therapie maligner Melanome entwickelt und induziert ebenfalls erhöhte ROS-Level. „Wenn der in Zellen mit hochreguliertem SOX6 ohnehin schon erhöhte ROS-Level durch Elesclomol weiter gesteigert wird, wird ein Schwellenwert überschritten, ab dem die Zellen absterben“, sagt Grünewald. „In Zellen ohne erhöhte SOX6-Aktivität dagegen wird dieser Schwellenwert kaum erreicht.“ Aufwendige Zellkultur-Untersuchungen und 3D-Knochenmodelle bestätigten, dass Elesclomol die Viabilität von Ewing-Sarkom-Zellen mit hoher SOX6-Aktivität im Vergleich zu derjenigen von Zellen mit geringer Aktivität tatsächlich signifikant verringert. Auch mit Elesclomol behandelte Mäuse zeigten ein vermindertes Tumorwachstum.
Deshalb könnte Elesclomol nach Ansicht der Wissenschaftler künftig eine vielversprechende Option zur selektiven Behandlung von Ewing-Sarkom Patienten sein, bei denen SOX6 besonders stark hochreguliert ist. „Es gibt Patienten mit höherer und niedrigerer SOX6-Expression. Sehr hoch ist sie vor allem dann, wenn die Patienten Träger einer genetischen Variante sind, die in Zusammenspiel mit dem Fusions-Onkogen dafür sorgt, dass der Tumor besonders stark proliferiert – die also bisher schlechtere Heilungschancen haben“, sagt Grünewald.
Quelle: Ludwig-Maximilians-Universität München (LMU)
20.05.2020