Nicht ganz dicht
Endoleaks mit der Interventionellen Radiologie in den Griff kriegen
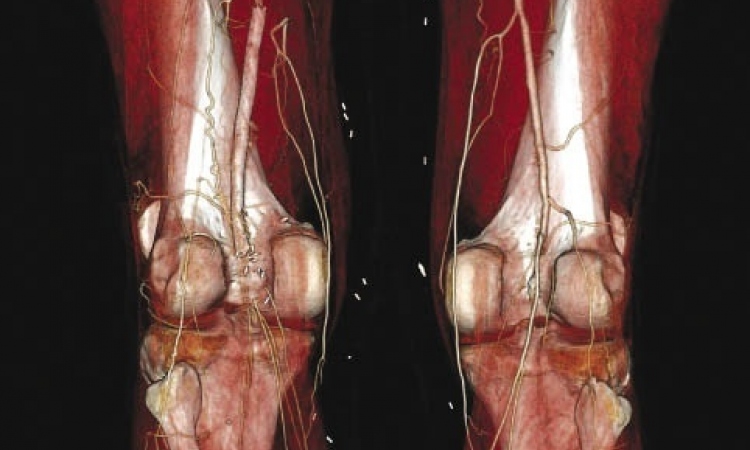
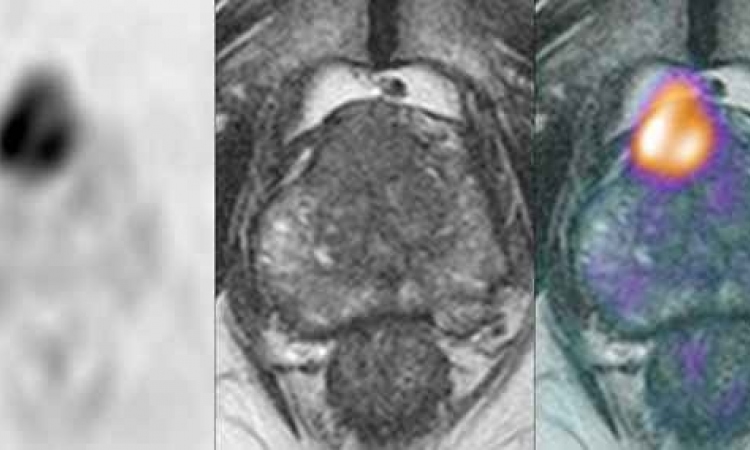
Manchmal ist Stenten wie Klempnern – kaum glaubt man eine undichte Stelle im Rohr repariert zu haben, bricht das Leck andernorts wieder auf. So oder so ähnlich kann es sich zumindest mit den thorakalen oder abdominellen Aortenaneurysmen verhalten. Diese werden immer häufiger minimal-invasiv mit einem Stentgraft therapiert, der das Aneurysmawachstum stoppen und die Ruptur verhindern soll.
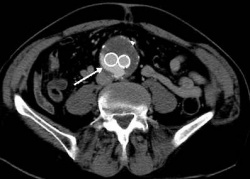
In gut 25 – 30 % der Fälle kommt es allerdings zu Undichtigkeiten, einer sogenannten Endoleckage, welche das Aneurysma trotz Stentgraft weiterwachsen lässt und damit eine abermaligen Rupturgefahr induziert. Was die Interventionelle Radiologie dann leisten kann, darüber berichtet Dr. Marcus Treitl, Oberarzt für Interventionelle Radiologie und Gefäßtherapie am Institut für Klinische Radiologie des Klinikums der Ludwig Maximilians Universität München.
Zunächst einmal leckt nicht jede Bruchstelle gleich. Deshalb werden Endoleaks in fünf verschiedene Typen eingeteilt. Bei Typ 1 besteht eine Undichtigkeit im distalen oder proximalen Stentende. Typ 2 beschreibt eine Blutflussumkehr in den Seitenästen der Bauchaorta, welche im Bereich des Aneurysmas entspringen und durch den Stentgraft überdeckt werden. Das passiert, wenn diese Gefäße weiterhin über Umgehungskreisläufe mit Blut versorgt werden, das zurück in die Aussackung fließt. Eine Typ-3-Leckage dagegen meint einen Defekt in den verschiedenen Stent-Einzelteilen, die im Körper nach dem Steckprinzip ineinander gesetzt werden oder gar einen Bruch des Stentgrafts. Der Typ 4 beschreibt eine Porosität des Stentgrafts, die sich unmittelbar nach Implantation sehr häufig beobachten lässt und fast immer spontan versiegt. Typ 5 umfasst die Gruppe der Aortenaneurysmen, die aus unerfindlichen Gründen auch nach dem Eingriff weiterwachsen. Hier spricht man von Endotension.
Die Klassifikation der Endoleaks erfolgt über kontrastmittelverstärkten Ultraschall und/oder einen 2-Phasen-CT-Scan mit einer arteriellen und einer spätvenösen Kontrastmittelphase nach 60 – 120 Sekunden Wartezeit. Das ist nötig, weil Endoleaks nur sehr langsam anreichern. Ist der Grund für die Undichtigkeit gefunden, gibt es unterschiedliche Lösungsansätze. Komplikationen des Typs 1, 3 und 4 werden meist mit einem neuen Stent versorgt, Typ 2 mit einer Embolisation und Typ 5 mit einer Operation therapiert.
Die Typ-2-Leckagen gehören zu den häufigsten. Sie stellen darüber hinaus die einzige Gruppe dar, die nicht sofort therapiert wird, denn oftmals hilft hier ein wenig Geduld: Über 40 % verschließen sich spontan wieder. Oft reicht es auch, die medikamentöse Behandlung mit Thrombozytenaggregationshemmern umzustellen oder ganz abzusetzen, damit sich das Endoleak von selbst verschließt. Tritt dieser Fall nicht ein und kommt es dennoch zu einem Größenwachstum des Aneurysmasacks, dann ist eine Therapieindikation gegeben. Es gibt dann zwei Wege, um erneut an das Aortenaneurysma heranzukommen: die endovaskuläre oder die CT-gesteuerte Therapiemethode.
„Eine endovaskuläre Therapie ist nur dann möglich, wenn die Gefäße auch gut zu erreichen sind, z.B. bei der Arteria mesenterica inferior. Häufig sind aber die Lumbalarterien betroffen. Dann ist der Zugang über die Gefäße nur bedingt möglich, weshalb die Rezidivrate bei endovaskulärer Versorgung bei bis zu 80 % liegt. In diesen Fällen ist die CT-gesteuerte perkutane Intervention eindeutig die bessere Variante“, so Treitl.
Bei der CT-gestützten Intervention wird der Aneurysmasack zunächst mit einer translumbalen Aortographienadel punktiert. Dann wird ein Mikrokatheter in das Endoleak eingeführt und ein Flüssigembolisat in die Endoleak-Höhle injiziert. Als Flüssigembolisat dient Dr. Treitl ein Ethylen-Vinylalkohol-Copolymer, das unter dem Produktnamen Onyx von der Firma ev3 bekannt ist. Sobald die Substanz in Kontakt mit dem Blutstrom tritt, trennt sich das Lösungsmittel Dimethylsulfoxid (DMSO) von dem Copolymer ab und es bildet sich ein schwammartiges Embolisat (sog. Cast) an der Katheterspitze. Dieser Cast bleibt lang genug elastisch und weich, um sowohl die Endoleak-Höhle auszugießen als auch direkt die zu- und abführenden Gefäße zu versiegeln. Damit das Material an der Kathetherspitze präzipitiert und nicht wegschwimmt, muss es sehr langsam bei einer Geschwindigkeit von etwa 0,3 ml pro Minute injiziert werden. Deshalb sollte die Intervention mit einer CT-Fluoroskopie visualisiert werden.
Bereits seit 10 Jahren wird Onyx für Neurointerventionen eingesetzt. Aber erst seit zwei Jahren hat Dr. Treitl das Flüssigembolisat auch für seine Zwecke in der abdominellen und thorakalen Aorta entdeckt. Einen kleinen Nachteil hat das Onyx für die neue Indikation noch: Der Gehalt des Tantal-Pulvers, das die Substanz röntgendicht macht, ist zurzeit noch sehr hoch, weil es sich primär um ein Neuroprodukt handelt, das für die Durchleuchtung im Schädel gedacht ist. Der CT-Strahl wird dadurch bei der Anwendung im Thorax oder Abdomen praktisch komplett ausgelöscht und es kommt zu starken Aushärtungsartefakten. Das heißt, um den Onyx-Cast bildet sich ein blinder Bereich, der die Nachkontrolle schwierig gestaltet. Dr. Treitl und sein Team führen daher gerade wissenschaftliche Studien durch, um den Tantal-Gehalt zu reduzieren. Dies ist ihnen bereits auf experimenteller Ebene geglückt.
Bleibt die letzte offene Frage, ob ein Endoleak nicht von vornherein verhindert werden kann. Dazu Dr. Treitl: „Eine Undichtigkeit ist häufig nicht vorhersehbar. Im Moment wird allerdings diskutiert, ob nicht zumindest die sofort sichtbaren Seitengefäße, die vom Aneurysma abgehen, noch vor der Stent-Implantation prophylaktisch verschlossen werden sollten. Ob das nicht auch negative Effekte auf die Durchblutung sensibler Strukturen haben kann, muss jedoch noch geklärt werden.“ Seit einem halben Jahr läuft deshalb am Gefäßzentrum der LMU eine prospektive Studie, um dieser Fragestellung auf den Grund zu gehen. Erste Ergebnisse werden mit Spannung erwartet.
Im Profil
Dr. Marcus Treitl, Jahrgang 1971, studierte Medizin in seiner Heimatstadt München. Seinen AiP absolvierte er in der Inneren Medizin am Augustinum München und in der Radiologie am Institut für Klinische Radiologie der LMU.
Als Assistenzarzt in der Abteilung für Gefäßchirurgie der Chirurgischen Klinik und Poliklinik des Klinikum Innenstadt der LMU vertiefte sich Dr. Treitl in den vaskulären und endovaskulären Schwerpunkt.
Seit 2008 arbeitet er als Oberarzt am Institut für Klinische Radiologie, wo er den Funktionsbereich Interventionelle Radiologie und Gefäßtherapie abdeckt.
05.01.2012