News • Symbiont statt Parasit
Milben in unseren Hautporen werden Teil von uns
Mikroskopisch kleine Milben, die nahezu unser gesamtes Leben in unseren Poren leben, könnten bald gänzlich mit uns eins werden: Forschende haben die DNA der Demodex folliculorum-Milbe erstmals vollständig untersucht, um die Lebensweise des winzigen Parasiten zu erkunden. Ihre Untersuchung zeigt, dass die in den Hautporen lebenden Milben in Folge von Inzucht und Isolation zahlreiche Gene und Zellen abgeworfen haben und sich einer dauerhaften Existenz mit uns annähern.
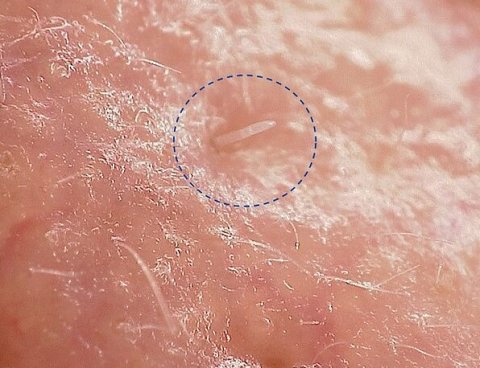
Die Demodex folliculorum-Milben leben in den Gesichts-Haarfollikeln, einschließlich der Wimpern, und an den Brustwarzen nahezu jedes Menschen. Sie sind etwa 0,3 mm lang und ernähren sich vom Talg, der von den Zellen in den Poren abgegeben wird. Sie werden nachts aktiv und bewegen sich zwischen den Follikeln, um sich zu paaren. Außerhalb der Poren können sie jedoch nicht überleben. "Aufgrund dieser engen und dauerhaften Verbindung zum Menschen hat die Milbe enorm an Größe und zahlreiche Gene verloren. Sie überleben mit einem minimalen Repertoire an Proteinen – der geringsten Anzahl, die je bei dieser und verwandten Arten beobachtet wurde", erklärt Alejandro Manzano Marín, Co-Erstautor der Studie und Mikrobiologe am Zentrum für Mikrobiologie und Umweltsystemwissenschaft. "Erstaunlicherweise zeigte unsere Untersuchung, dass die Milben in jungen Jahren viel mehr Zellen als im Erwachsenenstadium haben. Dies widerspricht der bisherigen Annahme, dass parasitische Tiere ihre Zellzahl schon früh in der Entwicklung reduzieren. Wir folgern daraus, dass sich die Milben von einem externen Parasiten zu einem permanenten Symbionten des Menschen entwickeln", berichtet Manzano Marín. Inwieweit dies für den Menschen vorteilhaft ist, könne man bisher aber noch nicht sagen.
Für die Studie kooperierte Manzano Marín mit Kolleg*innen der Bongor Universität (Wales), der Universität Reading (England), der Universität Valencia (Spanien) und der Nationalen Universität von San Juan (Argentinien). Die Forscher*innen drangen dabei mittels Genomsequenzierung – einer vollständigen Aufschlüsselung der Erbgutinformation – tief in die Biologie des winzigen Organismus ein. Aus der Art, dem Umfang, der besonderen Anordnung der Gene und dem ermittelten Genverlust konnten sie Informationen über ungewöhnliche Körpermerkmale und Lebensweisen der winzigen Organismen ziehen.
Die Analyse erklärt daher nicht nur die Nachtaktivität der Milben: Die Mikroorganismen haben unter anderem ihr UV-Schutzgen und das so genannte Zeitlos-Gen – jenes, das dafür verantwortlich ist, dass wir bei Tageslicht aufwachen – verloren. Die Untersuchung lässt auch Schlüsse auf die Physiologie der Milben zu. "Einige Forscher*innen waren bisher davon ausgegangen, dass die Milben keinen Anus haben und daher im Laufe ihres Lebens ihren gesamten Kot ansammeln müssen, bevor sie ihn beim Absterben freisetzen und dadurch Hautentzündungen verursachen", sagt Manzano Marín. "Unsere Studie bestätigte jedoch, dass sie doch einen After haben und daher zu Unrecht für viele Hautkrankheiten verantwortlich gemacht werden."
Da die Milben so isoliert existieren, sind sie keinen äußeren Bedrohungen ausgesetzt, sie müssen nicht um den Befall von Wirten konkurrieren – die Studie belegt, dass die Milben mütterlicherseits übertragen werden – und sie treffen auch nicht auf andere Milben mit anderen Genen. Der fehlende Kontakt zu potenziellen Partnern, die ihren Nachkommen neue Gene hinzufügen könnten, könnte die Milben in eine evolutionäre Sackgasse. "Die Inzucht hat eine Anhäufung schädlicher Mutationen zur Folge, schlechte Genvarianten verbreiten sich schließlich schnell", erklärt Manzano Marín. "Dieser evolutionäre Weg wurde bereits bei in Zellen lebenden Bakterien beobachtet, bei einem Tier jedoch noch nicht klar nachgewiesen." Diese Entwicklung könnte die Milben möglicherweise zum Aussterben bringen.
Die Studie ist in der Fachzeitschrift Molecular Biology and Evolution erschienen.
Quelle: Universität Wien
26.06.2022





