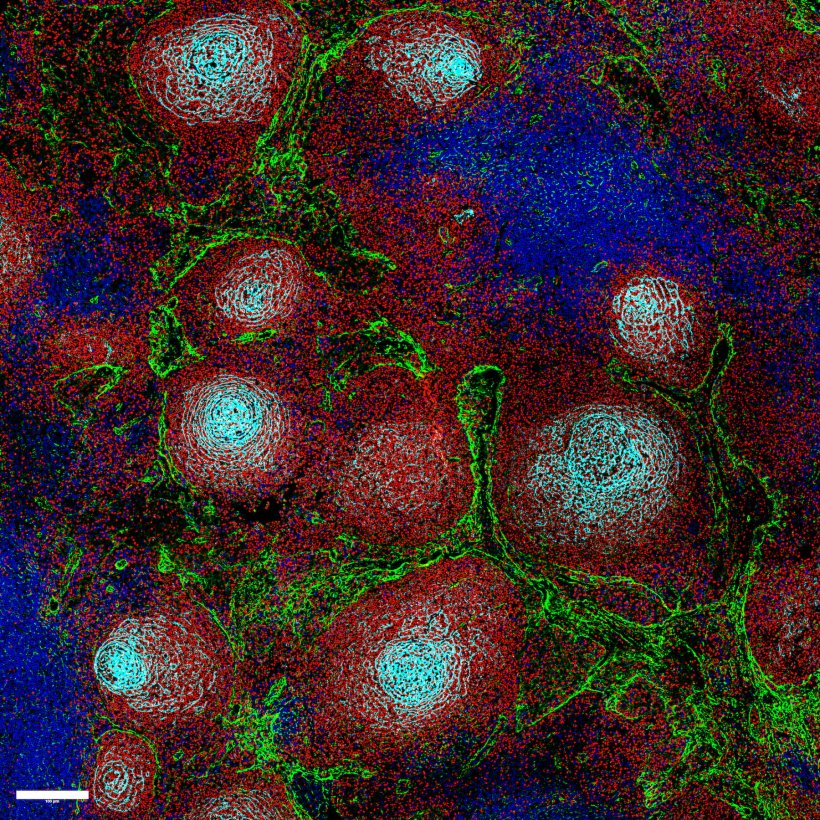
© Marc-Andrea Bärtsch, Felix Czernilofsky (Med-V UKHD)
News • Forschung zu Lymphdrüsenkrebs
Lymphome stiften Chaos im Lymphknoten
Neue Forschung zeigt, warum die Architektur des Lymphknotens bei bösartigen Lymphomen schrittweise abgebaut wird
Diesen Prozess hat ein Team um Simon Haas erstmals mit Einzelzell- und räumlichen Analysen entschlüsselt, berichten sie in „Nature Cancer“.
Lymphknoten sind hochorganisierte Kommandozentralen des Immunsystems. In ihnen verarbeiten Immunzellen Informationen über Krankheitserreger oder entartete Zellen und koordinieren eine gezielte Abwehrreaktion. Diese präzise Zusammenarbeit ermöglicht es dem Körper, Infektionen und Krebs wirksam zu bekämpfen. Entscheidend für den Erfolg ist die räumliche Organisation: Unterschiedliche Immunzelltypen besetzen klar definierte Bereiche im Lymphknoten und übernehmen dort spezialisierte Aufgaben. Diese komplexe Gewebearchitektur bildet die Grundlage einer effektiven Immunantwort.
Wir vermuten, dass der Tumor durch die aktive Zerstörung der Lymphknotenstruktur das lokale Immunsystem schwächt, das ihn eigentlich bekämpfen sollte, und so sein eigenes Wachstum begünstigt
Felix Czernilofsky
Beim Lymphdrüsenkrebs (Lymphom) gerät diese Ordnung jedoch ins Wanken. Bösartig veränderte Immunzellen können die Architektur des Lymphknotens tiefgreifend verändern. Während bei manchen Lymphomformen die räumliche Organisation weitgehend erhalten bleibt, bricht sie – insbesondere bei aggressiven Subtypen – vollständig zusammen. Obwohl Ärzte diese strukturellen Unterschiede seit Jahrzehnten diagnostisch nutzen, war bislang unklar, warum bestimmte Lymphome die Gewebearchitektur zerstören und welche Bedeutung dies für die Krankheitsentwicklung hat.
Ein internationales Forschungsteam hat dieses Rätsel nun gelöst und die Architektur von Lymphknoten bei Patienten mit unterschiedlichen Lymphom-Subtypen detailliert kartiert. An der Forschung federführend beteiligt waren die Forschungsgruppen von:
- Professor Simon Haas (Berlin Institute of Health at Charité (BIH), Max Delbrück Center, Queen Mary University of London)
- Professor Sascha Dietrich (Klinik für Hämatologie, Onkologie und Klinische Immunologie des Universitätsklinikums Düsseldorf)
- Professorin Judith Zaugg (European Molecular Biology Laboratory, Universität Basel)
- PD Dr. Dr. Daniel Hübschmann (Deutsches Krebsforschungszentrum (DKFZ))
Die Ergebnisse eröffnen neue Perspektiven für Biomarker und gezielte Therapien.
Das internationale Team analysierte Lymphknoten mit intakter ebenso wie mit zerstörter Gewebearchitektur und nutzte dafür hochauflösende Einzelzell- und räumliche Analysemethoden. „Diese Technologien ermöglichen es uns, molekulare, zelluläre und räumliche Veränderungen präzise nachzuvollziehen“, sagt Dr. Lea Jopp-Saile, eine der Erstautorinnen der Studie und Wissenschaftlerin in Haas‘ Arbeitsgruppe.
Das Ergebnis der Analyse: Seltene Stromazellen – spezialisierte Stützzellen, die den Lymphknoten wie ein feines Netzwerk durchziehen – sind maßgeblich für die räumliche Organisation der Immunzellen im Lymphknoten verantwortlich. In gesunden Lymphknoten fungieren sie als „Dirigenten“ des Immunsystems, indem sie mithilfe von Botenstoffen die Immunzellen in definierte Bereiche lenken. In besonders aggressiven Lymphomen ist diese Dirigentenfunktion jedoch tiefgreifend gestört.
Beim Versuch, den Tumor zu bekämpfen, produzieren T-Zellen entzündungsfördernde Botenstoffe. Diese Botenstoffe programmieren in den Stromazellen jedoch die Signalproduktion um. Dadurch verlieren die Stromazellen ihre strukturgebende Funktion und die räumliche Organisation des Lymphknotens bricht zusammen. Der Verlust der Architektur ist somit kein passiver Nebeneffekt des Tumorwachstums, sondern wird aktiv durch Entzündungsprozesse in der Tumorumgebung vorangetrieben. Diese Umprogrammierung der Stromazellen geht Analysen großer Patientenkohorten zufolge mit einer deutlich schlechteren Prognose einher. „Wir vermuten, dass der Tumor durch die aktive Zerstörung der Lymphknotenstruktur das lokale Immunsystem schwächt, das ihn eigentlich bekämpfen sollte, und so sein eigenes Wachstum begünstigt“, sagt Dr. Felix Czernilofsky, ebenfalls Erstautor der Studie.

© UKD
„Unsere Ergebnisse deuten darauf hin, dass eine Stabilisierung der Stromazellen oder eine gezielte Modulation entzündlicher Signale ein vielversprechender neuer Therapieansatz sein könnte“, sagt Professor Sascha Dietrich, Klinikdirektor der Klinik für Hämatologie, Onkologie und Klinische Immunologie, Uniklinik Düsseldorf. „Darüber hinaus könnten die identifizierten Mechanismen helfen, neue Biomarker zu entwickeln, um aggressive Krankheitsverläufe frühzeitig zu erkennen.“
Ermöglicht wurde die Studie durch eine internationale Kooperation und eine interdisziplinäre Zusammenarbeit über klassische Fachgrenzen hinweg. Federführend beteiligt waren die Lymphomexperten Dr. Felix Czernilofsky sowie Professor Sascha Dietrich (Universitätskliniken Düsseldorf und Heidelberg), der Experte für Einzelzelltechnologien Professor Simon Haas (Berlin Institute of Health in der Charité und am Max Delbrück Center, Berlin, sowie Queen Mary University of London) sowie die Datenwissenschaftler PD Dr. Dr. Daniel Hübschmann (Deutsches Krebsforschungszentrum, DKFZ, Heidelberg Institute for Stem cell Technology and Experimental Medicine gGmbH, HI-STEM), Dr. Lea Jopp Saile (DKFZ, HI-STEM), Dr. Anna Mathioudaki (European Molecular Biology Laboratory, EMBL, DKFZ) und Professorin Judith Zaugg (EMBL, Universität Basel).
Quelle: Berlin Institute of Health in der Charité
28.03.2026