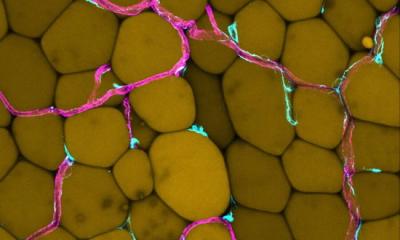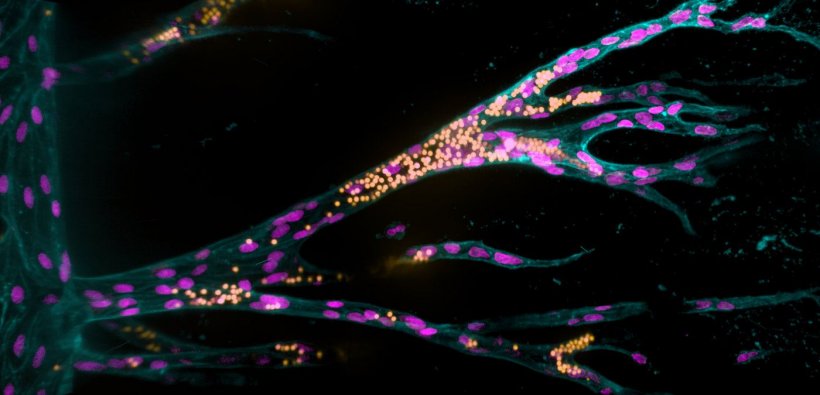
Bildquelle: Liu et al., Nature Communications 2021 (CC BY 4.0)
News • Hydrogel-Gerüst entwickelt
Künstliches Gewebe mit wachsenden Blutgefäßen
Im Labor Gewebe herzustellen, mit denen sich geschädigte Organe heilen oder ersetzen lassen, ist eine der großen Zukunftsvisionen der Medizin. Künstliche Materialien könnten sich als Gewebegerüste eignen, denn anders als natürliches Gewebe bleiben sie im Organismus lange genug stabil, so dass der Körper neue natürliche Strukturen ausbilden kann.
Eine grundlegende Voraussetzung für funktionsfähige Gewebe ist, dass in ihnen Blutgefäße wachsen und sich mit dem Gefäßsystem des Organismus verbinden können, so dass das Gewebe durchblutet und mit Sauerstoff und Nährstoffen versorgt wird. Bisher ist allerdings fast nichts darüber bekannt, welche Materialeigenschaften das Wachstum von Blutgefäßen fördern. Ein Team um die Biomedizin-Ingenieurin Dr. Britta Trappmann vom Max-Planck-Institut für molekulare Biomedizin in Münster hat jetzt ein Zellkultursystem entwickelt, in dem sich zum ersten Mal in einem Gerüst aus künstlichen Materialien ein funktionsfähiges Blutgefäßsystem bildet. Die Studie ist in der Fachzeitschrift „Nature Communications“ erschienen.
Die Endothelzellen bilden untereinander Kontakte, heften sich in dem Kanal an ihre künstliche Gewebeumgebung und formen so nach etwa einem Tag ein Ursprungsblutgefäß
Britta Trappmann
Die Wissenschaftler arbeiteten mit einem speziellen Hydrogel, dessen Eigenschaften sie kontrolliert verändern können, und ließen darin ein Ursprungsblutgefäß aus menschlichen Blutgefäßzellen wachsen. Sie untersuchten, wie die Materialeigenschaften der künstlichen Zellumgebung die Bildung weiterer Blutgefäße beeinflussten, und stimmten diese fein aufeinander ab. Ihre wichtigsten Erkenntnisse: „Das künstliche Gewebematerial muss bestimmte Adhäsionsmoleküle in der Membran von Blutgefäßzellen aktivieren, damit die Zellen in Gruppen aus dem Ursprungsgefäß auswandern und röhrenförmige Strukturen bilden – gleichzeitig muss das Material für die Blutgefäßzellen schnell genug abbaubar sein, damit sie Gefäße in ausreichender Größe formen können“, erklärt Britta Trappmann. Um sich an die natürliche Umgebung von Zellen anzunähern, müssten in weiteren Schritten zahlreiche weitere Biomoleküle und Zellen in das Modellsystem integriert werden, beispielsweise Signalproteine, Immunzellen oder die Blutgefäße stabilisierende Zellen. „Die Wirkung all dieser Faktoren ist in natürlichem Gewebe zudem gekoppelt und von Organ zu Organ unterschiedlich“, ergänzt die Wissenschaftlerin. All das zu verstehen, sei ein Fernziel. Das Wissen könnte man dann nutzen, um implantierbare Gewebe zu entwickeln. Britta Trappmann und ihr Team arbeiteten bei ihren Untersuchungen mit Kollegen an der Universität Münster sowie Arbeitsgruppen aus München und North Carolina zusammen.
Für ihre Untersuchungen bauten die Forschenden auf einem Modellsystem auf, das Britta Trappmann während ihrer Zeit als Postdoktorandin in den USA an der Boston und Harvard University gemeinsam mit Kolleginnen und Kollegen entwickelt hatte. Es besteht aus einem dreidimensionalen Hydrogel auf Zuckerbasis, in das die Wissenschaftler mit einer Akkupunkturnadel zwei Kanäle stechen. Diese haben jeweils einen Durchmesser von 400 Mikrometern und verlaufen im Abstand von etwa einem Millimeter parallel zueinander. In dem einen Kanal säen die Wissenschaftler Endothelzellen aus, die auch in natürlichen Geweben die Blutgefäße auskleiden. „Die Endothelzellen bilden untereinander Kontakte, heften sich in dem Kanal an ihre künstliche Gewebeumgebung und formen so nach etwa einem Tag ein Ursprungsblutgefäß“, erklärt Britta Trappmann. Wenn es soweit ist, schicken die Wissenschaftler durch den zweiten Kanal einen Wachstumsfaktorcocktail – dies sind Moleküle, die auch in natürlichen Geweben das Blutgefäßwachstum vorantreiben – woraufhin die Endothelzellen in das Hydrogel einwandern.
Die Wissenschaftler wollten nun herausfinden, welche Eigenschaften des Hydrogels bestimmen, ob die wandernden Endothelzellen wirklich neue Blutgefäße bilden. Sie untersuchten, welche Rolle die Aktivierung von sogenannten Adhäsionsmolekülen in der Membran der Zellen spielt, durch die sich Zellen an die Umgebung anheften können. Die Forscher reicherten das Gewebegerüst aus Hydrogel zunächst mit unterschiedlichen Mengen von Peptiden an, die einen bestimmten Typ von Adhäsionsmolekülen in der Membran von Endothelzellen aktivieren – die Integrine. Je höher die Konzentration der Peptide war, desto mehr Endothelzellen wanderten in Gruppen durch das Hydrogel. Blockierten die Wissenschaftler die Integrinfunktion, beobachteten sie hingegen, dass die Zellen nur einzeln migrierten. In einem weiteren Schritt untersuchte das Team dies für zwei Integrin-Subtypen. „Wir haben herausgefunden, dass Integrin αvβ3 das entscheidende Adhäsionsmolekül ist, das aktiviert werden muss, damit die Endothelzellen in Gruppen auswandern“, erzählt Britta Trappmann. Die Wissenschaftler zeigten auch, dass die kollektive Zellwanderung wiederum Voraussetzung dafür ist, dass die Endothelzellen im nächsten Schritt – nach einer Kulturzeit von etwa zwei Wochen – Hohlräume formen, die mit dem Ursprungsgefäß verbunden sind.
Zwar bildeten die Blutgefäßzellen nun röhrenförmige Strukturen, diese waren allerdings kleiner als bei natürlichem Gewebe, was sich – so die Hypothese der Wissenschaftler – möglicherweise dadurch erklären ließ, dass das künstliche Hydrogel im Vergleich zu natürlichem Gewebe weniger abbaubar ist und kleinere Poren hat, durch die Zellen hindurchschlüpfen können. Ihre Lösung: Das Hydrogel besteht aus Zuckermolekülketten, die durch bestimmte Moleküle miteinander vernetzt sind. Die Wissenschaftler tauschten diese Vernetzermoleküle aus, so dass die Zellen das Hydrogel durch von ihnen freigesetzte Enzyme schneller spalten und somit schneller migrieren konnten, wodurch sie größere Gefäßstrukturen bildeten.
Quelle: Max-Planck-Institut für molekulare Biomedizin
27.07.2021