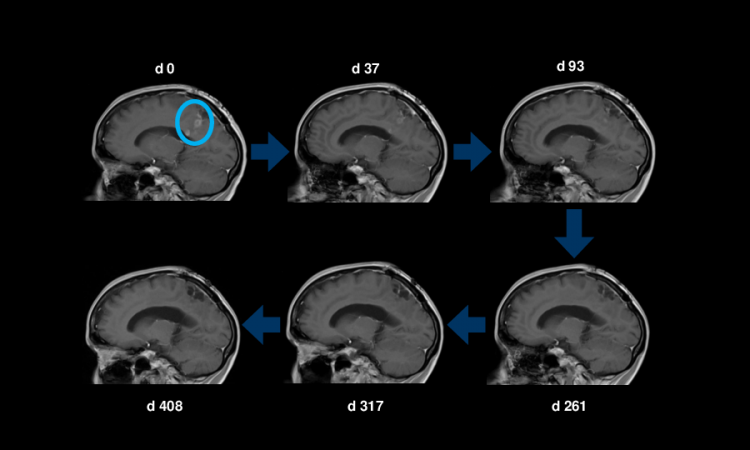
Bildquelle: Universitätsklinikum Heidelberg
News • Meningeom-Forschung
Hirntumoren: bessere Klassifizierung bringt Vorteile für Diagnose und Therapie
Eine internationale Studie mit rund 3000 Patienten bestätigt die Aussagekraft eines neuen Klassifizierungssystems für Meningeome. Es kombiniert Gewebecharakteristika (Histologie) mit molekularen Analysen und verbessert so die Therapieplanung.
Die Forschenden der Neuropathologie (Ärztl. Direktor Prof. Dr. Andreas von Deimling) des Universitätsklinikums Heidelberg (UKHD) und des Deutschen Krebsforschungszentrums (DKFZ) zusammen mit internationalen Kollegen haben die Ergebnisse dieser prospektiven Studie in der Fachzeitschrift Journal of Clinical Oncology veröffentlicht.
In Deutschland erkranken jährlich etwa 7.000 Menschen an einem Tumor des Gehirns oder Rückenmarks. Ein Drittel der Betroffenen leidet an einem Meningeom, das umliegendes Hirngewebe verdrängt und mit Kopfschmerzen und weiteren neurologischen Symptomen in Erscheinung tritt. Meningeome sind die häufigsten Hirntumore bei Erwachsenen und variieren im Krankheitsverlauf von gutartig bis hochaggressiv und tödlich. Eine zuverlässige Klassifizierung bei der Diagnose ist dabei entscheidend für den weiteren Therapieverlauf.
Mit der bisherigen Einteilung rein nach histologischen Kriterien können aggressiv wachsende Meningeome nicht zuverlässig von gutartigen Fällen unterschieden werden
Felix Sahm
Zur Diagnose werden Meningeome derzeit mittels Histologie, d.h. dem Erscheinungsbild ihrer Zellen unter dem Mikroskop, in Grad 1 (gutartig) bis Grad 3 (bösartig) eingestuft. 90 Prozent der Fälle gelten als gutartig und können in der Regel vollständig operativ entfernt werden. Ob der Patient damit geheilt ist oder ob der Tumor schnell nachwächst, ist mit der klassischen histologischen Untersuchung von Gewebeproben – der aktuell gängigen WHO-Einteilung – oft schwer zu entscheiden. „Eine präzise Risikoeinschätzung ist für die Therapie und deren Anpassung im Krankheitsverlauf äußerst wichtig“, sagt PD Dr. Felix Sahm, Geschäftsführender Oberarzt der Neuropathologie des UKHD und Wissenschaftler am DKFZ. Bei Grad 2 und 3 Meningeomen ist derzeit oft eine anschließende Strahlentherapie vorgesehen. „Mit der bisherigen Einteilung rein nach histologischen Kriterien können aggressiv wachsende Meningeome nicht zuverlässig von gutartigen Fällen unterschieden werden“, berichtet der Projektleiter Sahm und Wissenschaftler im Deutschen Konsortium für Translationale Krebsforschung (DKTK). Infolge ungenauer Klassifizierung des Tumors kommt es immer wieder zu Rückfällen bei zu harmlos eingestuften und fälschlicherweise nicht bestrahlten Tumoren. Andererseits werden manche zu aggressiv eingeschätzte Tumore womöglich unnötig bestrahlt.
Die Forschenden entwickelten daher ein neues Klassifizierungssystem auf Basis von histologischen und molekularen Charakteristika, mit dem sich Meningeome wesentlich genauer klassifizieren lassen. Das neue Klassifizierungssystem basiert auf drei Säulen: dem bisherigen WHO-Grading anhand von Gewebemerkmalen, dem Methylierungsstatus des Erbguts und der Kopienzahl-Variationen. Der Methylierungsstatus beschreibt, an welchen Abschnitten der DNA kleine biochemische Gruppen angeheftet sind, und die Kopienzahl-Variationen (CNV, copy-number variations) zeigen das unterschiedlich häufige Auftreten verschiedener DNA-Abschnitte im Genom. Beides spielt eine wichtige Rolle beim Ablesen der Gene und der Produktion zellulärer Bausteine. Die Zusammenschau von klassischen Gewebecharakteristika und dem molekularen Fingerabdruck des Tumors wird Algorithmus-unterstützt in eine Bewertung – den sogenannten Score – verrechnet und gibt Hinweise darauf, wie sich das einzelne Meningeom im Verlauf weiter entwickeln wird. Auf diese Weise lassen sich nun auch erstmals Tumore unterscheiden, die in ihrer DNA-Struktur identisch erscheinen, aber doch einen unterschiedlichen Krankheitsverlauf nehmen.
Die Entwicklung und Aussagekraft des neuen Klassifizierungssystems auf Basis des Methylierungsstatus konnten die Heidelberger Forschenden in den letzten Jahren bereits in retrospektiven, also rückblickenden Analysen an eingelagerten Tumorproben zeigen. In ihrer aktuellen Veröffentlichung verbinden sie die Vorteile der molekularen Analyse mit den mikroskopischen Befunden, und zeigen über einen Untersuchungszeitraum von vier Jahren, dass der Score auch vorausschauend, d.h. prospektiv, mit frisch isolierten Gewebeproben aussagekräftig ist und die Diagnostik sowie Therapieplanung unterstützen kann.
Quelle: Universitätsklinikum Heidelberg
18.10.2021