Bildquelle: Unsplash/Robina Weermeijer
News • Neuer Risikomarker
Fehlerhafte Faltung: Alzheimer bis zu 14 Jahre vor Diagnose erkennen
Der Nachweis einer fehlerhaften Faltung des Proteins Amyloid-β im Blut zeigt bei symptomfreien Menschen, die später tatsächlich Alzheimer entwickelten, ein deutlich erhöhtes Erkrankungsrisiko an – bis zu 14 Jahre vor der klinischen Diagnose der Demenz.
Die Amyloid-β-Faltung erwies sich anderen untersuchten Risikomarkern als überlegen. Dies zeigten Wissenschaftler vom Deutschen Krebsforschungszentrum (DKFZ), von der Ruhr-Universität Bochum (RUB), vom Krebsregister des Saarlands und vom Netzwerk Alternsforschung der Universität Heidelberg.
Die Forscher veröffentlichten ihre Ergebnisse jetzt im Journal Alzheimer & Dementia.
Dieser Artikel könnte Sie auch interessieren

Artikel • Neurodegenerative Erkrankungen
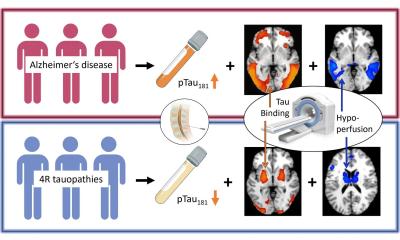
MRT/PET zur Früherkennung von Alzheimer & Co.
Die Gruppe der neurodegenerativen Erkrankungen ist mit einem langsam fortschreitenden Abbau der Hirnsubstanz verbunden. In der Diagnostik kommt zunehmend die Positronen-Emissions-Tomographie (PET) zum Einsatz. Damit können pathologische Proteine aufgespürt werden, etwa die für die Alzheimer-Krankheit typischen Amyloid-Plaques und Tau-Aggregate.
Bis heute gibt es keine wirksame Therapie gegen die Alzheimer-Demenz. Das liegt nach Meinung vieler Experten vor allem daran, dass die Krankheit erst weit nach ihrem eigentlichen biologischen Start klinisch diagnostiziert werden kann – wenn charakteristische Symptome wie etwa Vergesslichkeit auftreten. Die zugrunde liegenden Gehirnschädigungen sind dann aber bereits weit fortgeschritten und irreversibel. „Inzwischen liegen alle Hoffnungen darauf, mit neuen Therapieansätzen in dieser symptomlosen Frühphase der Erkrankung präventiv einzugreifen. Um solche Ansätze in Studien zu prüfen, ist es entscheidend, Menschen zu identifizieren, die ein besonders hohes Risiko haben, Alzheimer zu entwickeln", sagt Hermann Brenner, der im DKFZ die Abteilung Klinische Epidemiologie und Alternsforschung leitet.
Bei der Alzheimer-Krankheit kommt es zu einer fehlerhaften Faltung des Amyloid-β-Proteins, die bereits 15 bis 20 Jahre vor dem Auftreten der ersten Symptome beginnt. Die fehlgefalteten Proteine verklumpen und lagern sich als Amyloid-Plaques im Gehirn ab. Ein von Klaus Gerwert, RUB, entwickeltes Untersuchungsverfahren kann im Blut nachweisen, ob die Amyloid-Proteine abnormal gefaltet sind.
In einer vorangegangenen Arbeit hatten Gerwert und Brenner bereits gezeigt, dass sich die Amyloid-β-Veränderungen im Blut schon viele Jahre vor dem klinischen Ausbruch der Krankheit im Blut feststellen lassen. Sie konnten ebenfalls zeigen, dass der Nachweis von fehlgefaltetem Amyloid im Blut mit der Plaque-Bildung im Gehirn korreliert. Nun wollten die Wissenschaftler prüfen, ob die Analyse von Amyloid-β geeignet ist, das Alzheimer Risiko vorherzusagen und wie sie im Vergleich zu anderen bekannten bzw. vermuteten Risikofaktoren abschneidet. Dazu griffen die Forscher erneut auf Blutproben zurück, die im Rahmen der ESTHER*-Studie gewonnen worden waren. Die von Hermann Brenner geleitete und gemeinsam mit dem Saarländischen Krebsregister durchgeführte Kohortenstudie läuft bereits seit dem Jahr 2000.
In der aktuellen Arbeit berücksichtigten die Forscher die Ausgangs-Blutproben von 150 ESTHER-Teilnehmern, bei denen im Verlauf von 14 Jahren Nachbeobachtungszeit eine Demenz diagnostiziert wurde. Als Kontrollen wurden 620 Teilnehmer ohne bekannte Demenzdiagnose zufällig ausgewählt, die den Erkrankten in Alter, Geschlecht und Bildungsniveau entsprachen. Für die Menschen, die später tatsächlich Alzheimer entwickelten, zeigte die Amyloid-Bestimmung ein gegenüber der Kontrollgruppe bis zu 23-fach erhöhtes Erkrankungsrisiko an – bis zu 14 Jahre vor der Diagnose der Alzheimer-Demenz. Bei anderen Demenzformen, die etwa auf Minderdurchblutung des Gehirns beruhen, lieferte die Untersuchung keine Hinweise auf erhöhte Risiken, sie ist also spezifisch für die Alzheimer Erkrankung.
Mit dem neuen Nachweisverfahren können wir möglicherweise nicht-invasiv und kostengünstig Hochrisikogruppen, die noch keine Symptome zeigen, erkennen
Klaus Gerwert
Die Forscher hatten auch zahlreiche andere mögliche Risikoprädiktoren in ihre Analyse eingeschlossen. Darunter war etwa eine bestimmte Variante des Gens für das Apolipoprotein E (APOE Ɛ4) sowie Vorerkrankungen (Diabetes, Bluthochdruck, Depression) oder Lebensstilfaktoren (Körpergewicht, Bildungsgrad). Mit Ausnahme des APOE4-Status, der für die Menschen, die später tatsächlich Alzheimer entwickelten, ein 2,4-fach erhöhtes Risiko anzeigte, korrelierte keiner der untersuchten Faktoren mit dem Erkrankungsrisiko.
Für die Risikovorhersage spielte es keine wesentliche Rolle, ob zwischen Entnahme der Blutprobe und dem Beginn der klinisch manifesten Demenz 0 bis 8 oder 8 bis 14 Jahre lagen. „Bei dieser Arbeit ging es uns nicht darum, anhand der Amyloid-β-Faltung individuelle Diagnosen zu erstellen. Vielmehr wollten wir prüfen, ob dieser Laborwert für eine Risikostratifizierung größerer Bevölkerungsgruppen geeignet ist. Hier hat sich die Untersuchung auf Fehlfaltung des Amyloid-β den anderen potenziellen Risikomarkern als weitaus überlegen erwiesen", erklärt Hannah Stocker vom DKFZ und vom Netzwerk Alternsforschung der Universität Heidelberg, die Erstautorin der Arbeit.
„Mit dem neuen Nachweisverfahren können wir möglicherweise nicht-invasiv und kostengünstig Hochrisikogruppen, die noch keine Symptome zeigen, erkennen. Bei diesen Personen greifen unter Umständen die Medikamente doch noch, die bislang in klinischen Studien keine Wirkung gezeigt haben", so Klaus Gerwert. „Vielleicht kann der Nachweis von fehlgefaltetem Amyloid-β im Blut damit entscheidend dazu beitragen, ein Medikament gegen Alzheimer zu finden." Um die Eignung des Laborverfahrens zur Ermittlung des Alzheimer-Risikos bei beschwerdefreien Menschen zu prüfen, sind jedoch weitere Studien erforderlich: In größeren Gruppen wollen die Forscher nun die Zuverlässigkeit der Analyse von Amyloid-β-Veränderungen ermitteln: Ist die Blut-Untersuchung auffällig, so muss dies durch ein etabliertes Verfahren zur Frühdiagnose von Alzheimer bestätigt werden, etwa durch eine Untersuchung des Nervenwassers oder durch spezielle Bildgebungsverfahren. Daher steht der Blut-Nachweis von fehlgefaltetem Amyloid-β derzeit noch nicht zur individuellen Risikoeinschätzung zur Verfügung.
Die Untersuchung auf Amyloid-β-Veränderungen beruht auf einer als „Immuno-Infrarot-Sensor" bezeichneten Technologie, mit der das Verhältnis von abnormal und normal gefaltetem Amyloid Beta gemessen wird. Abnormal gefaltetes Protein neigt zur Aggregation in Amyloid Plaques, während die gesunde Struktur dies nicht tut. Die beiden Strukturen absorbieren Infrarotlicht mit unterschiedlicher Frequenz, sodass der Bluttest das Verhältnis von gesundem zu pathologischem Amyloid-β in der Probe bestimmen kann.
* ESTHER: Epidemiologische Studie zu Chancen der Verhütung, Früherkennung und optimierten Therapie chronischer Erkrankungen in der älteren Bevölkerung
Quelle: Deutsches Krebsforschungszentrum (DKFZ)
14.10.2019