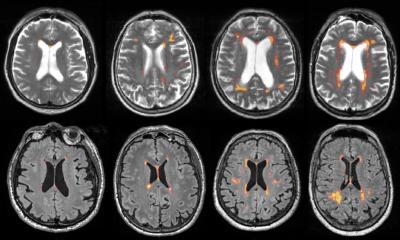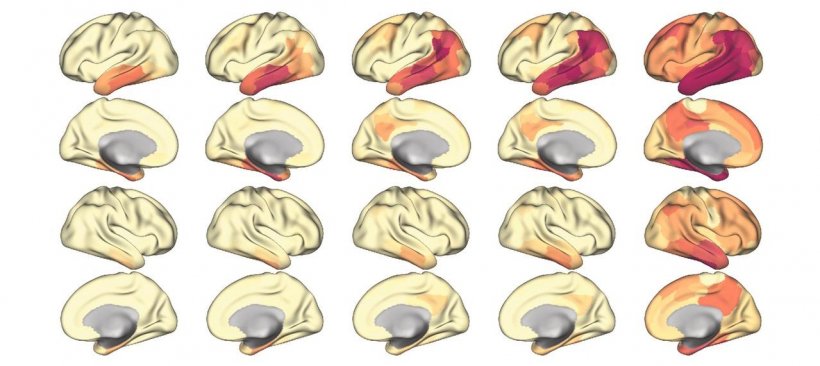
© LMU Klinikum - Dr. Nicolai Franzmeier
News • Demenz-Fortschritt im Blick
Auf dem Weg zur individuellen Alzheimer-Prognose
Während der Alzheimer-Demenz breiten sich fehlgefaltete Tau-Proteine entlang von Nervennetzwerken im Gehirn aus. Forscher am Institut für Schlaganfall- und Demenzforschung des LMU Klinikums ist es nun gelungen, den individuellen Verlauf der Tau-Ausbreitung zu prognostizieren.
Die Alzheimer-Demenz (AD) zählt zu den häufigsten Erkrankungen des zentralen Nervensystems und ist die Hauptursache für Demenz im Alter. Weltweit sollen 44 Millionen Menschen betroffen sein. Im Verlauf reichern sich im Gehirn von Betroffenen die fehlgefalteten Proteine Amyloid-beta und Tau an, was die Nervenzellen und die Kontaktstellen zwischen den Neuronen, die Synapsen, immer weiter zerstört. Die Folge: Gedächtnis- und Orientierungsstörungen, Sprachstörungen, Störungen des Denk- und Urteilsvermögens sowie Veränderungen der Persönlichkeit. Sie machen die Bewältigung des Alltagslebens immer schwieriger.
Forscher des Instituts für Schlaganfall- und Demenzforschung am LMU Klinikum München hatten jüngst nachgewiesen, dass sich die Tau genannten Proteine im Verlauf der Erkrankung vornehmlich entlang miteinander vernetzter Hirnregionen ausbreiten und den Krankheitsverlauf entscheidend mitbestimmen bzw. verschlimmern. Jetzt haben die Wissenschaftler um Arbeitsgruppenleiter Prof. Michael Ewers und Erstautor Dr. Nicolai Franzmeier im Fachblatt „Science Advances“ die Ergebnisse einer Folgestudie veröffentlicht. Kernpunkt: Ihre Methodik lässt sich nutzen, um die Ausbreitung der Tau-Proteine im Gehirn individuell zu prognostizieren.
Dieser Artikel könnte Sie auch interessieren

Artikel • Neurodegenerative Erkrankungen
MRT/PET zur Früherkennung von Alzheimer & Co.
Die Gruppe der neurodegenerativen Erkrankungen ist mit einem langsam fortschreitenden Abbau der Hirnsubstanz verbunden. In der Diagnostik kommt zunehmend die Positronen-Emissions-Tomographie (PET) zum Einsatz. Damit können pathologische Proteine aufgespürt werden, etwa die für die Alzheimer-Krankheit typischen Amyloid-Plaques und Tau-Aggregate.
Die Forscher haben in zwei unabhängigen Stichproben die Gehirne von jeweils 106 und 41 Patienten mit diagnostizierter Alzheimer-Krankheit mit einem ausgefeilten bildgebenden Verfahren untersucht: Die „tau-PET“ Untersuchung ermittelt die Verteilung der krankhaft veränderten Tau-Proteine im Gehirn von lebenden Patienten. Die erhobenen Bilddaten des Gehirns haben die Forscher*innen mit einem Atlas verknüpft, der die Verbindungen einzelner Bereiche des Gehirns darstellt. Darauf basierend ermittelten sie die Hirnregionen, die zum Zeitpunkt des tau-PET am meisten Tau angehäuft hatten. „Das sind die Epizentren der Tau-Pathologie“, erklärt Franzmeier. Jene Hirnregionen, die am stärksten mit diesen Epizentren vernetzt sind, konnten die Forschenden als die Bereiche prognostizieren, in denen sich etwa ein bis zwei Jahre nach der ersten tau-PET Untersuchung mit hoher Wahrscheinlichkeit ebenfalls abnormes Tau anreichert.
Mit unserer Methode können wir gezielt vorhersagen, wo im Gehirn ein Medikament für die Beseitigung der Tau-Pathologie tatsächlich wirken sollte
Michael Ewers
Mit dieser Methodik, so das Ergebnis der Studie, lässt sich grundsätzlich vorhersagen, wie sich die Tau-Proteine im Gehirn ausbreiten werden. „Und das kann individuell sehr unterschiedlich sein“, betont Ewers. Diese Erkenntnis ist fundamental, denn sie erweitert die gängige Lehrmeinung. Basierend auf Gewebeuntersuchungen von Gehirnen verstorbener Alzheimer-Patienten gingen Experten bislang davon aus, dass sich der Erkrankungsprozess relativ stereotyp bei den meisten Patienten über die immer gleichen Hirnregionen weiter verbreitet. „Aber nach unseren Daten ist die Variabilität viel größer als angenommen“, sagt Franzmeier. Beispiel: Bei Patienten mit frühem Tau in der rechten Hirnhälfte hat sich Tau am ehesten entlang Verbindungen in der rechten Hirnhälfte ausgebreitet. Umgekehrt sieht es bei Leuten mit Tau in der linken Hirnhälfte aus. Was das für die Patienten klinisch bedeutet, welche Symptomatik sie also bei fortschreitender Erkrankung entwickeln, wollen die Forscher demnächst erkunden.
Franzmeier betont, dass das neue Modell „die bisherigen Vorhersage-Verfahren der Tau-Ausbreitung übertrifft, da es eine individualisierte und patienten-zentrierte Prognose vornimmt.“ Noch allerdings ist es nicht so präzise, dass Ärzte es kurzfristig im klinischen Alltag nutzen könnten. „Dafür muss das Verfahren noch weiter validiert werden“, erklärt Ewers. Allerdings wäre eine Anwendung der Methode in der klinischen Medikamentenforschung sofort möglich. Hintergrund: Derzeit entwickeln Pharmafirmen Wirkstoffe, die die Ausbreitung des Tau-Proteins blockieren sollen. „Mit unserer Methode können wir gezielt vorhersagen, wo im Gehirn ein Medikament für die Beseitigung der Tau-Pathologie tatsächlich wirken sollte“, sagt Michael Ewers. Damit ließe sich besser ermitteln, ob ein Wirkstoff wirkt oder nicht.
Quelle: LMU Universität München
30.11.2020