Bildquelle: Leijie Jia/Leibniz-HKI
News • Infektionsbiologie
Apergillose: Wie Pilzsporen Lungenzellen "kidnappen"
Der krankheitserregende Pilz Aspergillus fumigatus entgeht seiner Vernichtung in Oberflächenzellen der menschlichen Lunge, indem er ein menschliches Protein bindet. Dadurch nistet er sich in abgegrenzten Bereichen – den Phagosomen – in den Lungenzellen ein.
So verhindert der Pilz, dass Zellprozesse in Gang gesetzt werden, die ihn abtöten würden. Forschende des Leibniz-Instituts für Naturstoff-Forschung und Infektionsbiologie (Leibniz-HKI) haben damit einen möglichen neuen Angriffspunkt gegen die Pilzinfektion entdeckt. Sie stellen ihre Erkenntnisse im Fachjournal Cell Host & Microbe vor.
Aspergillus fumigatus ist ein Schimmelpilz, der weltweit in der Umwelt vorkommt. Für Menschen mit einem geschwächten Immunsystem kann er zu einer ernsten Gefahr werden: Laut Schätzungen erkranken jedes Jahr mehr als 300.000 Menschen weltweit an einer Invasiven Aspergillose, also einer Infektion mit einem Schimmelpilz der Gattung Aspergillus. 40 bis 90 Prozent der Patienten versterben daran. Forschende am Leibniz-HKI haben nun entdeckt, dass Pilzsporen die Oberflächenzellen der Lunge davon abhalten können, sie zu töten. „Die sogenannten Epithelzellen unserer Lunge sind die wichtigste Barriere gegen Pilzsporen und andere potentielle Pathogene aus der Luft“, erklärt Axel Brakhage, Direktor des Leibniz-HKI und Professor an der Friedrich-Schiller-Universität Jena. Sie halten einen Großteil der Sporen ab, die wir tagtäglich einatmen.
Wir wollten wissen, welche der pilzlichen Oberflächenproteine an menschliche Zellen binden und somit an der Infektion beteiligt sein könnten
Leijei Jia
Anders als Immunzellen sind Lungenepithelzellen zwar nicht auf das Töten von Krankheitserregern spezialisiert, aber trotzdem dazu in der Lage: Die Zellen umschließen Fremdkörper und bilden damit ein sogenanntes Phagosom, ein von einer Membran umschlossenes Kompartiment innerhalb der Zelle. Anschließend wird eine Vielzahl von Zellprozessen in Gang gesetzt, bei denen das Phagosom reift und die Eindringlinge schließlich mit stark reaktiven Substanzen zersetzt werden. Dass Pilzsporen diesen Mechanismus umdirigieren können, entdeckten die Forschenden, als sie sich deren Oberflächenstrukturen genauer ansahen. „Wir wollten wissen, welche der pilzlichen Oberflächenproteine an menschliche Zellen binden und somit an der Infektion beteiligt sein könnten“ erklärt Leijei Jia, Erstautor der Studie.
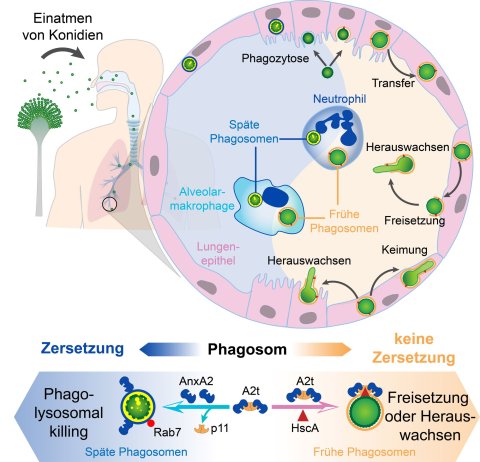
Bildquelle: Leijie Jia/Leibniz-HKI
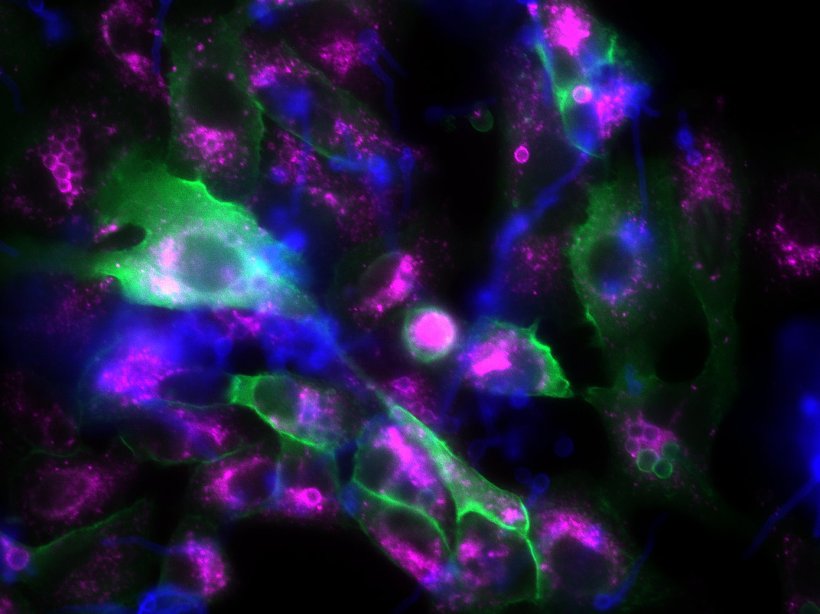
Dabei fanden sie ein menschliches Protein – p11 – das offenbar von einem pilzlichen Protein gebunden wird. „Wenn wir das Pilzprotein ausschalten, das an p11 bindet, finden wir die Pilzsporen in den ‚reifen‘ Phagosomen, das heißt sie werden zersetzt. Wenn wir das menschliche p11 ausschalten, ebenso“, sagt Jia. „Wenn das Pilzprotein und p11 jedoch intakt sind, bleiben die Phagosomen ‚unreif‘.“ Dann umschließen die Epithelzellen der Lunge zwar die Pilzsporen, vernichten sie aber nicht. Das konnten Jia und seine Kollegen am Leibniz-HKI auch unter dem Mikroskop beobachten: In den unreifen Phagosomen keimten die Sporen und bildeten Pilzfäden, sogenannte Hyphen. Manche der Sporen wurden auch wieder aus der Zelle heraus oder in eine Nachbarzelle transportiert, sodass der Pilz sich verbreiten kann.
Die Experimente konnten die Forschenden anschließend auch mit Immunzellen bestätigen. Das heißt, die Pilzsporen können nicht nur Phagosomen in den Lungenzellen umdirigieren, sondern auch in verschiedenen Immunzellen.
Die klinische Bedeutung ihrer Entdeckung untersuchte das Team aus Jena gemeinsam mit Medizinern aus Portugal, die DNA-Daten von Empfängern und Spendern einer Stammzelltransplantation lieferten. „Nach Transplantationen sind Patienten besonders anfällig für Pilzinfektionen, weil das Immunsystem heruntergefahren wird“, erklärt Axel Brakhage. Gut ein Viertel der etwa 500 Empfänger von Stammzelltransplantationen entwickelte in den Monaten nach der Transplantation eine lebensbedrohende Invasive Aspergillose.
Auf dem p11-Gen der transplantierten Stammzellen fanden die Forschenden tatsächlich einen kleinen Unterschied. „Patienten mit einer bestimmten Mutation hatten in der Stichprobe eine geringere Wahrscheinlichkeit, an Invasiver Aspergillose zu erkranken. Dieses Ergebnis hilft, die stärker gefährdeten Patienten besonders intensiv zu beobachten“, so Jia. Sowohl das Pilzprotein, das an p11 bindet, als auch das menschliche Protein selbst könnten zudem mögliche Angriffspunkte für eine Therapie der Pilzinfektion sein.
Die Arbeit wurde durch die Deutsche Forschungsgemeinschaft (DFG) unter anderem im Rahmen des Exzellenzclusters Balance of the Microverse und der Sonderforschungsbereiche FungiNet (Transregio) und PolyTarget gefördert. Weitere Unterstützung erhielt die Arbeit durch die Leibniz-Gemeinschaft, die Fundação para a Ciência e a Tecnologia, durch die EU im Rahmen von Horizon 2020, durch die „la Caixa“-Stiftung und durch das Gilead Research Scholars Program.
Quelle: Leibniz-Institut für Naturstoff-Forschung und Infektionsbiologie
09.03.2023