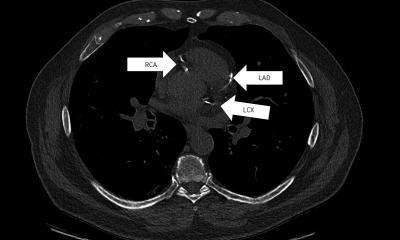
Interview • Tumor oder nicht?
Detektivarbeit beim Lungenrundherd
Dank moderner Techniken wie der HRCT mit ihren 1 - 2mm Schichten werden Rundherde immer früher entdeckt. Nahezu jedes zweite CT weist einen auffälligen Befund in der Lunge auf.

Doch welcher Befund ist harmlos und welcher muss beobachtet und kontrolliert werden? Prof. Cornelia Schaefer-Prokop gibt Tipps zur morphologischen Befundung und berichtet über neue wissenschaftliche Ansätze.
Ist der Lungenrundherd schwer zu diagnostizieren?
In der Tat ist der Lungenrundherd einer der häufigsten – oft inzidentellen – Befunde. Die normale Thorax-Aufnahme weist nur eine relativ limitierte Sensitivität gegenüber Rundherden oder allgemein fokalen Verdichtungen auf. Das ist auch der Grund, warum wir im Röntgenbild nur selten ein Bronchialkarzinom mit einer Größe von ein bis zwei Zentimetern erkennen. Im CT dagegen können wir bei einer Schichtdicke von inzwischen nur einem Millimeter auch den kleinsten Rundherd in der Lunge sehen. Als Radiologen sind wir daher in mehrfacher Hinsicht diagnostisch gefordert: Wir müssen eine Aussage darüber treffen, ob es sich um einen besorgniserregenden Befund handelt, der weiter kontrolliert und behandelt werden muss und wir müssen diese Diagnose aufgrund der deutlich besseren Technik bei einer steigenden Anzahl von Patienten durchführen.
Dabei helfen die Fleischner-Kriterien?
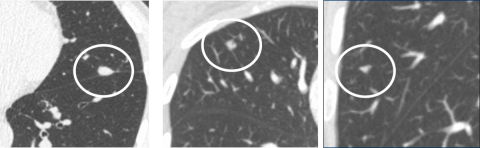
Die Fleischner-Kriterien wurden erstmals 2005 publiziert und bezogen sich zunächst ausschließlich auf solide Rundherde. Im Jahr 2013 wurden diese Kriterien dann um die sub-soliden Rundherde erweitert. Subsolide Herde bestehen zum Teil aus einer milchglasartigen und zum Teil aus einer soliden Komponente. Die ersten Fleischner-Kriterien waren insofern ein Novum, weil erstmals zwischen zwei Risikogruppen – Rauchern und Nicht-Rauchern – unterschieden wurde. Dabei wurden Richtlinien aufgestellt, in welchen Zeitabständen je nach Gruppe die CT-Untersuchungen wiederholt werden sollten. Inzwischen sind diese Kriterien allerdings nicht mehr adäquat, weil sie nicht an die Häufigkeit des Rundherdbefundes angepasst sind. Denn seinerzeit haben wir noch mit dickeren CT-Schichten gearbeitet, heute sehen wir jedoch kleine und kleinste Rundherde. In Folge dessen fielen hochgerechnet abertausende von CTs an, um Rundherde zu kontrollieren – eine Aufgabe, die weder medizinisch noch finanziell zu bewerkstelligen ist.
Darüber hinaus haben wir aus den großen Screening-Studien wie dem amerikanischen National Lung Screening Trial (NLST) mit mehr als 50.000 Patienten oder der NELSON Studie als der größten europäischer Screeningstudie viel über die Rundherdmorphologie gelernt. Wenden wir diese neuartigen morphologischen Kriterien an, können wir den CT-Befund viel besser danach beurteilen, welches Risiko für eine Malignität besteht. Beispielsweise sind die kleinen intrapulmonalen Lymphknoten mit ihrer spezifischen Morphologie unbedenklich und nicht mit Metastasen zu verwechseln, während die Struktur anderer Rundherde den Verdacht auf ein primäres Lungenkarzinom aufkommen lässt.
Nach welchen Kriterien kann dann unterschieden werden?
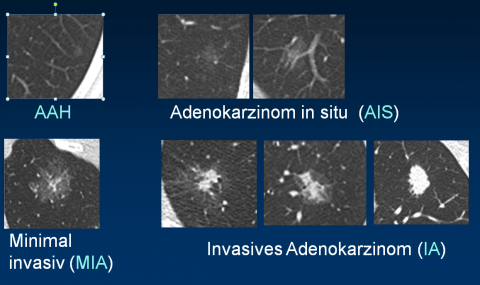
Aus den Screening-Studien wissen wir, dass die häufig auftretenden soliden Rundherde in der Regel ein deutlich geringeres Malignitäts-Risiko aufweisen als nicht-solide. Während von hunderten solider Rundherde nur wenige bösartig sind, liegt das Risiko bei den nicht-soliden Vertretern bei gut 30 Prozent. Neben der Fleischner-Society haben auch noch andere Fachgesellschaften Kriterien entwickelt. Am bekanntesten sind sicherlich die Lung-RADS des American College of Radiology (ACR), die aus Merkmalen wie Struktur, Durchmesser, Volumen und Wachstum eine Risikoabschätzung ableiten.
Noch liegt in der Interpretation eines Befundes sehr viel Subjektivität: Je nach Erfahrung und Einschätzung kommen zehn Radiologen manchmal zu ebenso vielen unterschiedlichen Ergebnissen. Das große Thema in der Forschung – und auch in meinen Arbeiten – ist daher die Entwicklung einer standardisierten Analyse per Computer, mit der Rundherde automatisch detektiert, quantifiziert und mit einem Risikofaktor versehen werden können. Danach kann auf objektivierter und automatisierter Grundlage festgelegt werden, welche Rundherde in welchen Zeitabständen kontrolliert werden müssen.
Dieses Verfahren wird sicherlich in den nächsten Jahren kommen. Der Radiologe muss sich dann nicht mehr jeden einzelnen Befund anschauen; ein Teil der radiologischen Arbeit wird durch Computerprogramme erledigt. Derzeit warten alle darauf, dass die Ergebnisse der größten europäischen Screening-Studie – der Nelson -Studie veröffentlicht werden, nicht nur weil sie den Einsatz des Lungenscreenings in Europa entscheidend beeinflussen werden, sondern auch weil positive Ergebnisse die Entwicklung derartiger computer-basierter Analysen weiter voranbringen würden.
Lässt sich damit das Problem der falsch-positiven Befunde in den Griff bekommen?
Erfahrungsgemäß zeigt jedes zweite CT einen Rundherd und es ist sinnvoller, zwischen unbedenklichen und risikobehafteten Rundherden zu diskriminieren als jahrelang falsch-positive Befunde zu überprüfen. Das haben wir gelernt, weil wir über Jahre viele Patienten systematisch kontrolliert haben. In anderen Worten, selbst wenn in Europa kein flächendeckendes Screening eingeführt wird, können wir künftig ein komplexes Krankheitsbild wie den Lungenrundherd viel besser befunden.
Profil:
Prof. Dr. Cornelia Schaefer-Prokop arbeitet seit 2009 als Radiologin am Meander Medical Centre, Amersfoort (Niederlande) und darüber hinaus als Wissenschaftlerin am Department of Radiology and Nuclear Medicine am Radboud University Medical Center in Njimegen. Zuvor war sie in Hannover (1993-1998), am AKH Wien (1998-2004) und AMC Amsterdam (2005-2009) tätig. Ihre Forschungsschwerpunkte liegen in der digitalen Radiographie, Computer-Aided Detection und Klassifikation und der Diagnostik interstitieller Lungenerkrankungen. Sie ist Mitherausgeberin von „European Radiology“, „Journal of Thorac Imgaing“ sowie „Insights into Imaging“ und Mitglied der Fleischner Gesellschaft.
15.01.2016