Jacobs University leitet Verbundprojekt TRANSLOCATION
EU-Offensive gegen multiresistente Krankheitskeime
Multiple Antibiotika-Resistenz von Bakterien ist eine der größten Gesundheitsbedrohungen unserer Zeit. Um die Entwicklung neuer Antibiotika voranzutreiben, startet nun als Teil der von der EU-Kommission ins Leben gerufenen Innovative Medicine Initiative (IMI) das Projekt TRANSLOCATION, an dem sich unter akademischer Leitung der Jacobs University 25 Partner aus Industrie und Wissenschaft beteiligen

Copyright: Jacobs University
Copyright: Jacobs University
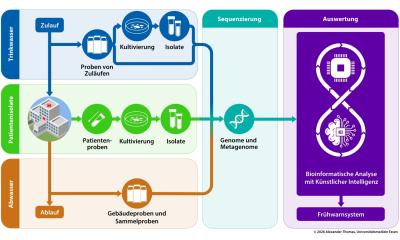
Forschungsfokus des mit 29,3 Mio. Euro budgetierten und zunächst auf fünf Jahre angelegten Projekts sind die molekularbiologischen Prozesse des Antibiotika-Transports durch die Bakterienzellwände und bakterielle Resistenzmechanismen. Außerdem soll ein neues Datenbanksystem für größtmögliche Informationstransparenz und Effizienz sorgen.
Die Resistenz vieler bakterieller Krankheitserreger gegen Antibiotika stellt weltweit eine ernsthafte Bedrohung für die Gesundheit von Mensch und Tier dar, die von der Weltgesundheitsorganisation WHO als „besorgniserregender öffentlicher Gesundheitsnotstand mit bislang unabsehbarer Tragweite“ bezeichnet wird. Allein in der EU sterben jährlich 25.000 Menschen an Infektionen mit multiresistenten Bakterien; die geschätzten Behandlungs- und Sozialfolgekosten belaufen sich auf 1,5 Mrd. Euro im Jahr. Außerdem entstehen und verbreiten sich ständig neue resistente Krankheitserreger, so dass vor allem Klinikärzten zunehmend effektive Behandlungsmöglichkeiten für bakterielle Infektionen ausgehen.
Trotz der gebotenen Dringlichkeit wurden in den vergangenen 30 Jahren nur zwei neue Antibiotika-Klassen bis zur Anwendungsreife gebracht. Zum einen sind die vorgeschriebenen klinischen Tests für neue Antibiotika sehr teuer; zum andern dürfen neue antibiotische Medikamente nicht auf dem freien Markt gehandelt, sondern nur in Notfällen zur Behandlung besonders problematischer Infektionen verwendet werden, um neuen Resistenzen vorzubeugen. Aus Rentabilitätsgründen sind daher nur noch wenige Pharmaunternehmen in diesem Feld aktiv. Darüber hinaus bestehen in der Forschung zahlreiche Wissenslücken auf molekularbiologischer Ebene in Bezug auf die genaue Wirkweise von Antibiotika und den Resistenzaufbau der Bakterien.
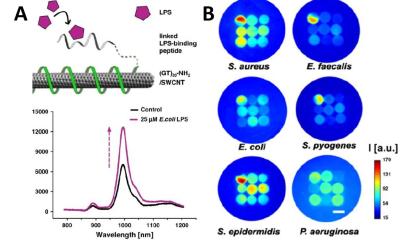
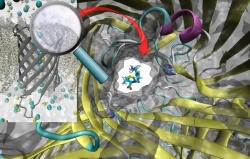
Hier liegt der wissenschaftliche Fokus des Projektes TRANSLOCATION: In einer breiten, Disziplinen-übergreifend angelegten Forschungsallianz wollen führende Wissenschaftler aus Mikrobiologie, Strukturbiologie sowie experimenteller und computergestützter Biophysik untersuchen, wie antibiotisch wirksame Substanzen mittels hochspezialisierter Transportproteine, sogenannter Porine, durch bakterielle Zellwände hindurch in das Zellinnere gelangen. Hierzu wollen die Forscher zunächst in einem umfangreichen Screening die entsprechenden Porine identifizieren, um dann ihre Struktur und Funktionsweise im Detail zu analysieren. Unter anderem sollen neu entwickelte Methoden ermöglichen, den Transport einzelner Wirkstoffmoleküle durch die Zellwände zu untersuchen. Darüber hinaus will das Forschungskonsortium die Mechanismen identifizieren, mit denen Bakterien bestimmte antibiotische Moleküle als schädlich erkennen und aus ihrem Zellinneren ausstoßen, bevor sie wirken können.
Im Zentrum der Untersuchung stehen die klinisch relevanten Organismen Escherischia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa sowie Acinetobacter baumannii, sogenannte gram-negative Bakterien, die wegen ihrer doppelten Zellmembran eine besonders effiziente Barriere für viele antibiotische Substanzen besitzen und in Krankenhäusern als Antibiotika-resistente Krankheitserreger weit verbreitet sind.
Die gewonnenen Erkenntnissen sollen dann in einem nächsten Schritt im Rahmen von TRANSLOCATION als Basis für gezieltes Wirkstoffdesign dienen: Ziel ist die Identifizierung von Substanzklassen bzw. gezielte Entwicklung von Molekülen, die besonders gut von den Krankheitserregern aufgenommen werden, im Inneren der Zellen jedoch als antibiotische Zellgifte unerkannt bleiben, bis sie ihre Wirkung entfalten konnten.
Der zweite Schlüsselaspekt von TRANSLOCATION ist die systematische Auswertung bisheriger Erfahrungen in der antibakteriellen Forschung. Um die Entwicklung anwendungsreifer antibiotischer Medikamente mit größtmöglicher Effizienz und Schnelligkeit voranzutreiben und dafür ein möglichst breites Wissens- und Kompetenzspektrum zu erschließen, werden sowohl ein neuartiges institutionsübergreifendes Datenmanagementsystem als auch ein spezielles Geschäftsmodell entwickelt, die einen umfassenden Datenaustausch von bislang beispielloser Transparenz ermöglichen sollen. Das TRANSLOCATION-Projektteam wird die Freigabe und Analyse von umfangreichen, zurzeit noch vertraulichen Datenbeständen koordinieren. Bereitgestellt werden diese Informationen in erster Linie von den Unternehmen der European Federation of Pharmaceutical Industries (EFPIA),, die sich an TRANSLOCATION beteiligen. Zusätzlich wird das TRANSLOCATION-Projektteam die Veröffentlichung aller neuen Erkenntnisse koordinierend unterstützen.
„Mit TRANSLOCATION werden erstmals in enger Zusammenarbeit mit den Forschungslabors weltweit operierender Pharmaunternehmen zahlreiche Forschungsfragen zusammengefasst und ganzheitlich betrachtet, die bislang getrennt von vielen einzelnen Forschergruppen bearbeitet wurden. So entstehen Synergien, die uns ein umfassendes Verständnis der Wirkweise von Antibiotika, dem Zustandekommen der gefährlichen Multiresistenzen und hoffentlich bald auch der molekularbiologischen ‚Tricks‘ erlauben, mit denen wir die Resistenzmechanismen aushebeln können“, sagt Mathias Winterhalter, Professor of Biophysics an der Jacobs University und wissenschaftlicher Manager von TRANSLOCATION.
Auch die neue Form des Datenaustausches sowie die breit angelegte Zusammenarbeit, die neben Forschungsinstitutionen und großen Pharmakonzernen auch kleine und mittelständische Unternehmen einschließt, sind für Winterhalter unverzichtbare Vorteile des TRANSLOCATION-Konzepts: „Die fortschreitende Ausbreitung multiresistenter Bakterien ist eine tickende Zeitbombe, so dass Antibiotika-Forschung und Entwicklung in einem dramatischen Wettlauf mit der Zeit stattfinden müssen. Einen öffentlichen Gesundheitsnotstand von dem Ausmaß, wie er sich im Moment abzeichnet, können wir nur verhindern, wenn alle Wissenschaftler im Bereich der antibakteriellen Forschung zusammenarbeiten – ohne dass sie durch Partikularinteressen oder organisatorische Reibungsverluste behindert werden! Die angestrebte Informationstransparenz von TRANSLOCATION hat daher echten Vorbildcharakter.“
TRANSLOCATION ist eines von derzeit drei Projekten des Programms „New Drugs for Bad Bugs“ (ND4BB) der von der Europäischen Kommission ins Leben gerufenen und als Public-Private Partnership organisierten Initiative für innovative Medikamente IMI (Innovative Medicines Inititiative). Die Gesamtkoordination von TRANSLOCATION liegt bei dem britischen Pharmakonzern GlaxoSmithKline. Die Jacobs University, die sich zusätzlich zu dem übergreifenden wissenschaftlichen Management auch in der Forschung für TRANSLOCATION engagiert, erhält 3,8 Mio. Euro. Beteiligte Jacobs-Wissenschaftler neben Mathias Winterhalter sind Roland Benz, Professor of Biotechnology und Experte für die Messung des Substanztransports durch Porine, Ulrich Kleinekathöfer, Professor of Theoretical Physics und Experte für die atomare Modellierung des Transports durch Membranproteine, Nikolai Kuhnert, Professor of Chemistry und Experte für den massenspektrometrischen Nachweis der Antibiotikaaufnahme durch die Bakterien, Georgi Muskhelishvili, Professor of Genetics und Experte für die Genregulation von bakteriellen Stressreaktionen, sowie Helge Weingart, University Lecturer in Life Sciences und Spezialist für Efflux-Pumpen, welche häufig an Antibiotika-Resistenzen beteiligt sind.
TRANSLOCATION-Projektpartner:
Universitäten, Forschungseinrichtungen, öffentliche Einrichtungen und Non-Profit-Organisationen
• Assistance Publique - Hôpitaux de Paris, Frankreich
• Centre National de la Recherche Scientifique, Frankreich
• Société Civile Synchrotron SOLEIL, Frankreich
• Fundacio Centre de Recerca en Salut International de Barcelona, Spanien
• Jacobs University Bremen, Deutschland
• Johann Wolfgang Goethe Universität, Frankfurt am Main, Deutschland
• University of St Andrews, Großbritannien
• Universita degli Studi di Cagliari, Italien
• Universität Basel, Schweiz
• Universitätsklinikum Freiburg, Deutschland
• Université d'Aix-Marseille, Frankreich
• Université de Genève, Schweiz
• University College Dublin, Irland
• University of Newcastle upon Tyne, Großbritannien
Pharmaunternehmen der European Federation of Pharmaceutical Industries (EFPIA):
• AstraZeneca AB, Schweden
• Basilea Pharmaceutica AG, Schweiz
• GlaxoSmithKline Research and Development Ltd, Großbritannien
• Janssen Infectious Diseases – Diagnostics BVBA, Belgien
• Sanofi-Aventis Research and Development, Frankreich
Unternehmen außerhalb von EFPIA
• Bruker Daltonik GmbH, Deutschland
• European Screening Port GmbH, Deutschland
• Ionovation GmbH, Deutschland
• Nanion Technologies GmbH, Deutschland
• Nanospot GmbH, Deutschland
• Yelen, Frankreich
14.02.2013