Bild Laurette: © privat, Bild Gilsbach: © UKHD
News • Tool beeinflusst Genaktivität
Genschere ohne Schere: CRISPRi ebnet Weg für bessere Herzforschung
Ein innovatives Werkzeug zur gezielten Veränderung der Genaktivität in Herzmuskelzellen könnte sich als Standardmethode für die Erforschung von Herz-Kreislauf-Erkrankungen etablieren.
Dr. Patrick Laurette und seine Kollegen des Deutschen Zentrums für Herz-Kreislauf-Forschung (DZHK) unter der Leitung von Prof. Ralf Gilsbach haben erfolgreich die Aktivität einzelner Gene in Herzmuskelzellen von Mäusen mittels des CRISPRi-Systems reduziert. Diese Technologie ermöglicht es, die Genexpression vorübergehend zu unterdrücken, ohne das Erbgut zu verändern. Sie umgeht damit potenzielle Risiken, die mit direkten Eingriffen in das Erbgut verbunden sind.
Die Wissenschaftler stellen ihre Erkenntnisse im Fachjournal Circulation Research vor.
CRISPRi basiert auf dem CRISPR-Cas-System und beinhaltet eine Genschere ohne Schneidefunktion, eine sogenannte „dead CAS“ (dCAS), die mit einer KRAB Repressordomäne fusioniert wurde. Durch die Verwendung eines molekularen Führers, einer guide RNA, kann dCas9 spezifisch an DNA-Sequenzen binden. Damit wird die Zielregion im Genom epigenetisch stillgelegt und ein Gen kann dann nicht mehr so gut abgelesen werden. Diese Blockade wird „epigenetisches Silencing“ genannt.
Ich bin überzeugt, dass dieser Ansatz eine translationale Bedeutung hat, auch wenn schwer vorherzusagen ist, wie schnell die Entwicklung hier weitergehen wird
Ralf Gilsbach
Um das CRISPRi-System in Herzmuskelzellen von Mäusen einzubringen, nutzten die Forscher Adeno-assoziierte Viren (AAV), die sich nicht in das Erbgut integrieren. Eine Herausforderung bestand darin, das gesamte System in die begrenzte genomische Kapazität der AAVs zu verpacken. Dies gelang den Forschern durch die Verwendung einer besonders kleinen dCAS. Andere virale Vektoren haben diesbezüglich zwar mehr Kapazität, sind aber nicht in der Lage, Herzmuskelzellen effizient zu erreichen oder können in das Genom integrieren.
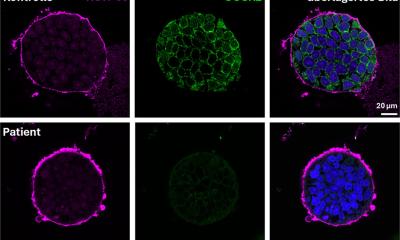
Wie gut das epigenetische Silencing mit dem AAV-CRISPRi-System in Herzzellen funktioniert, konnten Dr. Patrick Laurette und seine Kollegen des Universitätsklinikums Heidelberg für mehrere Gene und Enhancer nachweisen. Die Aktivität einiger Gene sank um bis zu 95%. Enhancer sind regulatorische Elemente, die Genexpression aus entfernten genomischen Distanzen feinregulieren können. „Die Komplexität des Säugerorganismus entsteht durch etwa eine Million regulatorischer Elemente. Allein in Herzmuskelzellen gibt es zwischen fünfzig- und hunderttausend dieser Enhancer“, so Prof. Ralf Gilsbach. Diese regulatorischen Elemente haben er und seine Kollegen nun im Visier, wenn sie mithilfe ihrer neuen Methode Erkrankungen wie Herzschwäche oder Herzrhythmusstörungen beeinflussen wollen.
Gilsbach betont die translationale Bedeutung dieses Ansatzes, der es ermöglicht, die Genexpression in vivo gezielt zu beeinflussen, ohne die DNA-Sequenz zu verändern. Zudem ist die Methode titrierbar, lässt sich also regulieren, und ihre Wirkung kann wieder rückgängig gemacht werden. Im Vergleich zu anderen Methoden wie dem Knock-out-Verfahren, bei dem Gene zerstört werden, bietet das AAV-CRISPRi-System eine präzisere Nachahmung der natürlichen Regulationsmechanismen in Zellen.
Methodisch optimiert und weiterentwickelt, könnte das Verfahren langfristig auch für die Therapie beim Menschen genutzt werden. „Ich bin überzeugt, dass dieser Ansatz eine translationale Bedeutung hat, auch wenn schwer vorherzusagen ist, wie schnell die Entwicklung hier weitergehen wird“, so Gilsbach. Es gibt bereits zahlreiche Firmen, die Adeno-assoziierte Viren und insbesondere CRISPR für Therapien andenken. Sie arbeiten unter anderem daran, unerwünschte Antikörper-Reaktionen zu vermeiden. Denn Menschen haben Antikörper gegen AAV und häufig auch gegen das aus Bakterien stammende CRISPR Protein.
Quelle: Deutsches Zentrum für Herz-Kreislauf-Forschung
16.05.2024