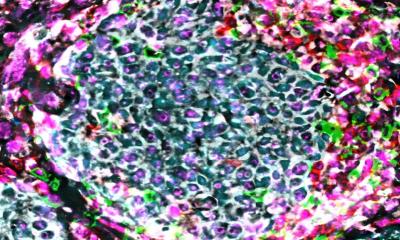
Der zelluläre Müllbeutel
Bei der Autophagozytose, dem Prozess der Abfallverwertung in den Zellen werden molekularen Müllbeutel hergestellt. Wie jetzt in Nature Communications berichtet, haben Wissenschaftler vom Max-Plack-Institut für Biochemie in Martinsried einen molekularen Klebstoff entdeckt, der das Ausgangsmaterial für die Müllbeutel, kleinen Fettbläschen, zusammenklebt.
Die Autophagozytose hilft Krebszellen eine Chemotherapiebehandlung zu überleben. Deshalb könnte ein den Wissenschaftlern bekannter Hemmstoff für den molekularen Kleber die Grundlage für eine neue Krebstherapie sein.
Autophagozytose ist ein wichtiger Prozess der zellulären Abfallverwertung. Dieser liefert ungewünschtes oder geschädigtes Material aus dem Zellplasma an das Lysosom, die Recyclinganlage der Zellen. Dafür werden besondere Müllbeutel, sogenannte Autophagosomen hergestellt, die den Abfall erkennen, einschließen und an die Recyclinganlage weiterleiten. Für die Herstellung dieser speziellen Müllbeutel sind zwei Eiweißkomponenten notwendig. Eines ist Atg9, ein Membraneiweiß, das in kleinen Vesikeln, eine Art Fettbläschen, eingelagert ist, die das Ausgangsmaterial für den Autophagosom-Müllbeutel bilden. Die zweite Komponente ist der Atg1-Kinasekomplex, ein großer Eiweißkomplex, der aus fünf Untereinheiten besteht. Die Wissenschaftler haben jetzt herausgefunden, wie die beiden Komponenten an der Herstellung des Autophagosoms beteiligt sind.
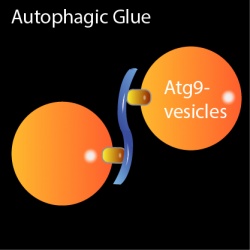
Die Wissenschaftler haben das Ausgangsmaterial für die Müllbeutel, die künstliche Atg9-Vesikel im Reagenzglas hergestellt. “Durch die Zugabe vom Atg1-Kinasekomplexes konnten wir zeigen, dass ein Atg1-Kinasekomplex zwei Atg9-Moleküle bindet und somit wie eine Art Klammer funktioniert und zwei Atg9-Vesikel miteinander verknüpft“ erklärt Yijian Rao aus dem Team von Thomas Wollert, Leiter der Abteilung Molekulare Membran- und Organell-Biologie.
Wenn kein Müll vorhanden ist, können zwei Untereinheiten des Atg1-Kinasekomplexes die Atg9-Bindungsstelle blockieren und so das Verknüpfen der Vesikel verhindern. Dann können keine Autophagosom-Müllbeutel entstehen. „Das heißt, das Verknüpfen der Membranen und die Herstellung des Müllbeutels wird durch die verschiedenen Untereinheiten der Atg1-Kinase kontrolliert“, erklärt Rao weiter.
Entscheidend für eine spätere medizinische Anwendung der Forschungsergebnisse ist ein kleines Peptid mit therapeutischem Potential. Die Wissenschaftler konnten zeigen, dass ein bestimmtes Peptid den Atg1-Kinasekompex in Hefezellen hemmt. Da Atg1 und Atg9 sowohl in Hefezellen als auch in menschlichen Zellen vorkommt, gehen die Wissenschaftler davon aus, dass ein ähnlicher Wirkstoff die Autophagozytose in menschlichen Zellen hemmen kann. Krebszellen nutzen die Autophagozytose, um eine Chemotherapiebehandlung zu überleben. Heutige Krebsmedikamente verursachen die Schädigung der Krebszellen, damit sie sterben. Leider werden bei dieser Behandlung nicht nur Krebszellen, sondern auch gesunde Zellen von den Medikamenten geschädigt.
Eine Möglichkeit, die Krebszellen empfindlicher zu machen, ist die Hemmung ihrer Autophagozytose. „Der Hemmstoff des Autophagozytose-Klebstoffes verhindert die Herstellung der Müllbeutel und stoppt die Autophagozytose sehr spezifisch. Dieses Peptid könnte die Grundlage für die Entwicklung eines Antikrebsmedikamentes sein oder die Effektivität eines heutigen Chemotherapie-medikamentes verbessern“, fasst Rao zusammen.
Quelle: Max-Planck-Institut für Biochemie
15.01.2016