Artikel • Symbiose zwischen Mensch und Bakterien
Das Mikrobiom: Eine Herausforderung für die Labormedizin
Der Mensch lebt in Symbiose mit einer Vielzahl von Mikroorganismen, die sowohl in seiner Umgebung, wie auch auf und in seinem Körper zu finden sind. Welch wichtige Funktion sie beim Menschen haben, wurde bis vor wenigen Jahren unterschätzt.
Bericht: Sandra Theison
Die mit Abstand meisten Bakterien des Mikrobioms befinden sich im Gastrointestinaltrakt und hier insbesondere im Dickdarm. Die Anzahl der dort befindlichen Bakterien übersteigt die Gesamtanzahl der menschlichen Körperzellen um den Faktor zehn, die Anzahl ihrer Gene die Summe der humanen Gene sogar um den Faktor 100. Mit 10-30% ist nur ein kleiner Teil kultivierbar. Beim Menschen gehören die meisten Bakterien des gastrointestinalen Mikrobioms zu den vier Stämmen Firmicutes, Bacteroidetes, Proteobacteria und Actinobacteria.
Im klinischen Alltag ist die bakterielle Identifikation zudem essentiell um zu unterscheiden, ob es sich bei einer Bakterienart um einen der bakteriellen Kolonisatoren oder um einen ursächlichen Infektionserreger handelt. Hierzu wird seit vielen Jahren bereits auf die Sequenzierung der 16S-rRNA zurückgegriffen, besonders wenn die phänotypischen Identifikationsmetoden Schwierigkeiten bereitet.
Das bakterielle 16S-rRNA Gen codiert für die 30S Untereinheit des prokaryotischen 70S Ribosoms und ist daher in der Erbinformation aller Bakterien enthalten. Es unterscheidet sich zudem von seinem eukaryotischen Pendant, dem 18S-rRNA Gen, sodass eine präzise Unterscheidung der bakteriellen DNA von der humanen möglich ist. Bekannt geworden ist die Gensequenz dieser Untereinheit, da sie sich in der Evolutionsbiologie als das Instrument zur Stammbaumanalyse etabliert hat.
Das 16S-rRNA-Gen besitzt eine Gesamtlänge von ca. 1.500 Basenpaaren und lässt sich in mehrere konservierte und neun weniger konservierte Abschnitte (V1-V9) unterteilen. Da die gering konservierten Abschnitte nur einen kleinen Effekt auf die Formation der 30S Untereinheit haben, sind diese Bereiche sehr variabel und spezifisch für einzelne bakterielle Spezies. Diese Regionen können somit als taxonomische Marker genutzt werden. Bei einer PCR-Reaktion können Primer an die bekannten konservierten Abschnitte binden und die variablen Regionen selektiv amplifizieren. Die anschließende Sequenzierung dieser DNA-Abschnitte erfolgt normalerweise durch Pyrosequenzierung (siehe Kasten unten).
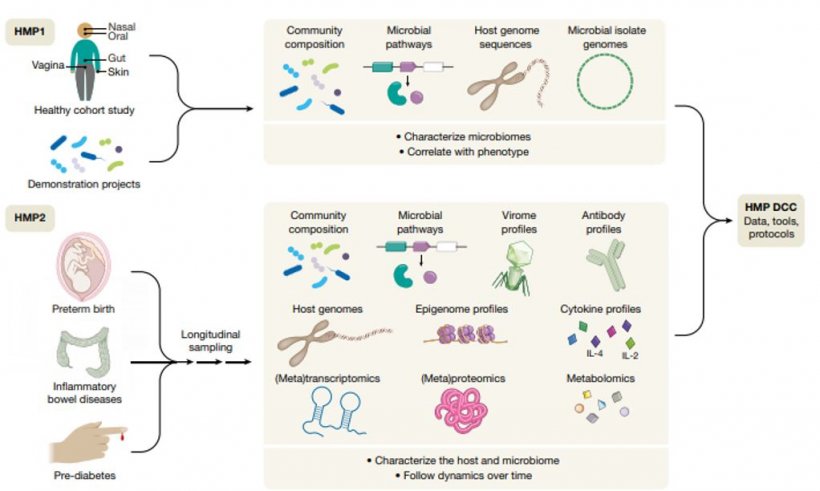
Das Humane Mikrobiom Projekt
Das Humane Mikrobiom Projekt (HMP) ist eines der größten biologischen Projekte aller Zeiten. Ziel des HMP ist es, alle Mikroorganismen, die den Menschen besiedeln, zu katalogisieren und die Einflüsse auf den gesunden als auch den kranken Menschen zu untersuchen. Das HMP wurde 2008 vom National Institute of Health (NIH) gestartet. Die Analyse setzt den Schwerpunkt auf die fünf Körperstellen Haut, Nase, Mund, Gastrointestinaltrakt und Vagina des gesunden Menschen. 2013 wurde das HMP1 mit über 14 TB Daten von 300 Personen abgeschlossen.
Die zweite Phase des HMP, das Integrative HMP (HMP2), startete 2014. Das HMP2 generiert Datenbanken, die die Interaktion des menschlichen Wirts mit dem Mikrobiom untersuchen. Hierbei wird der Fokus auf die drei Themen Schwangerschaft und Frühgeburt, Chronisch Entzündliche Darmerkrankungen sowie den Ausbruch von Diabetes Typ 2 gelegt. Beispielhaft ist im Folgenden die Vorgehensweise bei der Frühgeburt dargelegt. Bei Frühgeburten gibt es signifikante Unterschiede hinsichtlich ihrer Häufigkeit. So ist zum Beispiel in den USA die Wahrscheinlichkeit einer Frühgeburt bei Frauen mit afroamerikanischen Wurzeln sehr viel höher als bei Frauen anderer Volksgruppen.
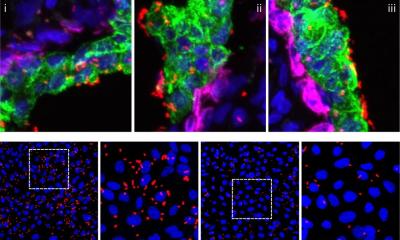
Analysen der 16S-rRNA sowie weitere Untersuchungen an 45 Früh- und 90 Normalgebärenden wurden in der beschriebenen Studie durchgeführt. Es wurde bereits bei einer ersten Auswahl bemerkt, dass der Anteil afroamerikanischer Frauen bei Frühgeburten höher ist. Bei der Analyse des vaginalen Mikrobioms stellte sich heraus, dass Frühgebärende eine niedrigere Konzentration eines Lactobacillusstamms und von 13 weiteren Bakterienstämmen eine höhere Konzentration aufweisen. Die Bakterien, die mit den Frühgeburten in Verbindung gebracht werden, korrelieren mit proinflammatorischen Cytokinen im Vaginalsekret. Diese Erkenntnisse zeigen neue Möglichkeiten in der Risikobewertung von Frühgeburten auf.
Ausblick
Ansatzpunkte für weiterführende Untersuchungen könnten an dieser Stelle die Katalogisierung des Mikrobioms in Hinsicht auf sein Proteom und Metabolom sein sowie deren Wechselwirkung mit den Proteinen und Stoffwechselprodukten des Menschen.
Pyrosequenzierung
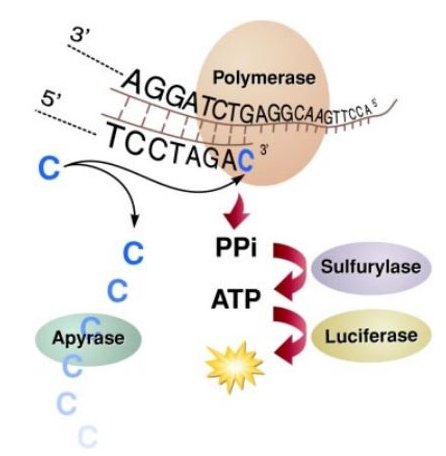
Wird von der DNA-Polymerase ein komplementäres Nukleodtid in den zu synthetisierenden Strang eingebaut, wird Pyrophosphat (PPi) freigesetzt. Das Enzym ATP-Sulfurylase wandelt dieses zu Adenosintriphosphat um, welches wiederum die Luziferase-Reaktion auslöst. Dadurch wird Luziferin in Oxyluziferin umgewandelt. Daraus resultiert dann ein charakteristisches Lichtsignal, dessen Stärke proportional zum verbrauchten Adenosintriphosphat ist. Überschüssige Nukleotide werden danach durch die Apyrase abgebaut. Da die Nukleotide einzeln in wiederkehrender Reihenfolge der Polymerase zur Verfügung gestellt werden, kann aus dem zeitlichen Muster der Lichtsignale die Sequenz des DNA-Stranges ermittelt werden.
13.08.2020