Artikel • Bestrahlungsplanung in Echtzeit, MRT mit Sauerstoff
Das innovative Arsenal der medizinischen Physik
MR-Linac, X-Kern-MRT, PET-CT: Prof. Mark Ladd, Präsident der Deutschen Gesellschaft für Medizinische Physik (DGMP) über die aktuellen Themen im Bereich der medizinischen Physik.

Für die Planung einer Strahlentherapie ist eine vorhergehende Bildgebung unerlässlich – schließlich muss man wissen, wo genau der Tumor liegt, um die ionisierende Strahlung zielgenau zu platzieren. „Derzeit erleben wir, wie die Bildgebung zunehmend auch während der eigentlichen Therapie zum Einsatz kommt“, berichtet Prof. Dr. sc. techn. Mark Ladd, Leiter der Abteilung für Medizinische Physik in der Radiologie am Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg anlässlich der 51. Jahrestagung der Deutschen Gesellschaft für Medizinische Physik (DGMP), deren Präsident er ist. Möglich macht dies ein System namens MR-Linac (Magnetic Resonance Linear Accelerator), das einen Linearbeschleuniger mit einem Magnetresonanztomographen kombiniert. „Dabei kann man in Echtzeit sehen, wie sich der Tumor mit der Atmung bewegt“, sagt Ladd, der im Interview mit Healthcare in Europe über die aktuellen Trends in der medizinischen Physik spricht.
Bestrahlungsplanung und -korrektur in Echtzeit
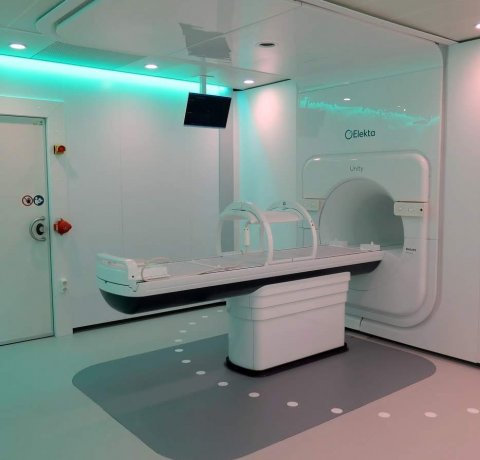
Bildquelle: Daniela Thorwarth / Uniklinik Tübingen
Mit dem MR-Linac lässt sich durch die kontinuierliche MR-Bildgebung während der Bestrahlung nicht nur die Atembewegung nachverfolgen und die Bestrahlung dahingehend anpassen, sondern auch die veränderte Lage eines Tumors oder eine Größenveränderung des Krebsgeschwürs während des mehrwöchigen Therapieverlaufes erfassen. „Mittelfristiges Ziel ist es, die Kollimatoren in Echtzeit zu steuern, um alle Veränderungen gegenüber der ursprünglichen Therapieplanung während Bestrahlung zu kompensieren. Wir sprechen davon, die Therapieplanung in Echtzeit anzupassen“, bekräftigt Ladd. Kann der Tumor zielgenauer angesteuert werden, so würde dies den präzisen Einsatz höherer Strahlendosen ermöglichen. „Dann müssten Patienten nicht 30 Mal zur Bestrahlung kommen, sondern vielleicht nur fünfmal“, erklärt der Heidelberger Wissenschaftler. Am DKFZ wird derzeit in einem Forschungsprojekt nach einem neuen Ansatz gefahndet, um Kollimatoren mit der dazu notwendigen Geschwindigkeit zu justieren.
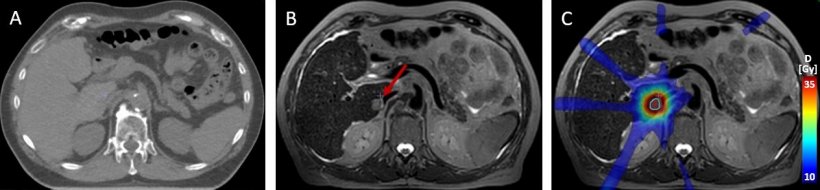
Bildquelle: Daniela Thorwarth / Uniklinik Tübingen
Eine noch exaktere Erkennung des Bragg-Peaks – also jenes Punktes, an dem die Energieabgabe des Strahles ihren Höhepunkt erreicht und dann abrupt abfällt – ist Thema eines weiteren Forschungsgebietes in der Strahlentherapie mit Protonen. Weil noch immer eine gewisse Unsicherheit herrscht, wo exakt der Bragg-Peak im Körper endet, wird ein vergleichsweise breiter Sicherheitsabstand um den Tumor festgelegt, damit möglichst das gesamte Tumorgewebe bestrahlt wird. „Mit der aktuellen Technik ist dieser Sicherheitssaum so groß, dass die Vorteile, die man von der Protonentherapie erwartet, nicht in vollem Umfang realisiert werden können“, bedauert Ladd. Daher wird versucht, verschiedene Methoden zu entwickeln, um in vivo den Bragg-Peak zu eruieren. Eine davon stützt sich auf die Detektion sekundärer Gammastrahlung, die von dem Protonenstrahl im Körper ausgelöst wird.
Schärfere Einblicke – die Photon-Counting-CT
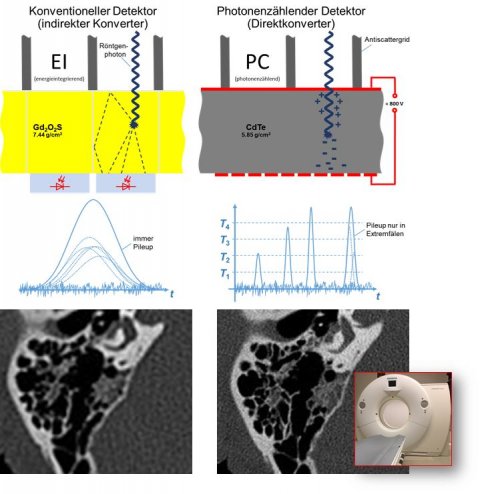
Bildquelle: DKFZ/Universitätsklinikum Heidelberg
Auch in der Radiologie gibt es bemerkenswerte aktuelle Entwicklungen. Eine davon ist die Photon-Counting-CT. Am DKFZ steht einer von weltweit insgesamt drei Prototypen, die sich durch ihren speziellen Detektor auszeichnen: Ein photonenzählender Detektor besteht aus einem Halbleitermaterial, das in der Lage ist, Röntgenstrahlen direkt in elektrische Signalimpulse umzuwandeln, was ihn besonders effizient macht. „Ich hoffe, dass diese Technologie irgendwann den Weg in die klinische Routine schafft“, bemerkt Ladd.
Die Kosten der photonenzählenden Detektoren seien zwar hoch, dafür aber ermöglichen sie eine bessere Auflösung und Bildgebung mit deutlich niedrigeren Kontrastmitteldosen. „Auch in Hinblick auf die aktuellen Diskussionen um Kontrastmittel ist Photon Counting ein vielversprechender Ansatz“, so Ladd.
Die MRT mit neuen Elementen und großer Feldstärke
Ein anderer aktueller Trend auf dem Gebiet der medizinischen Physik ist die X-Kern-MRT. Während bei der herkömmlichen MRT der Spin der Atomkerne des Wasserstoffs gemessen wird, ermittelt die X-Kern-MRT das magnetische Moment von Isotopen anderer Kerne, beispielsweise Natrium-23 (Na-23), Sauerstoff-17 (O-17), Kalium-39 (K-39) oder Chlor-35 (Cl-35). Das Problem: diese Isotope sind relativ selten – zum Beispiel liegen nur etwa 0,04 Prozent allen Sauerstoffes in Gestalt von O-17 vor. Am DKFZ läuft derzeit ein Forschungsprojekt, in dessen Zuge die Patienten während der Untersuchung mit O-17 angereichertes Gas inhalieren, das so ins Blut gelangt. Sobald der Sauerstoff in den Mitochondrien der Zellen ankommt und dort ins Wasser umgewandelt wird, kann er sichtbar gemacht werden. „Auf diese Weise kann man eine sehr genaue Messung des lokalen Sauerstoffstoffwechsels im Gehirn – aber auch in allen anderen Teilen des Körpers – durchführen“, erklärt Ladd. Gerade erforscht wird, ob dadurch nach einem Schlaganfall anhand regionaler Unterschiede im Stoffwechsel ermittelt werden, welche Areale sich erholen werden und welche nicht.
Dieser Artikel könnte Sie auch interessieren

News • Bildgebung mit Sauerstoff
X-Kern-MRT blickt in den Tumorstoffwechsel
Bei der Magnetresonanztomographie (MRT) wird gewöhnlich das mit dem Spin verbundene magnetische Moment der Atomkerne des Wasserstoffs gemessen. Wissenschaftler vom Deutschen Krebsforschungszentrum untersuchen allerdings den Spin anderer Kerne für die Bildgebung. „Die X-Kern-Bildgebung hat sehr großes Potenzial für die MRT-Bildgebung, da X-Kerne in vielen physiologischen Prozessen eine…
Für die Darstellung der Verteilung von O-17 und anderer Isotope mittels MRT ist eine Feldstärke von 7 Tesla fast unabdingbar. Doch auch darüber hinaus ist die 7-T-MRT eines der aktuell bedeutendsten Entwicklungsfelder in der medizinischen Physik. Seit 2017 sind die ersten Systeme für klinische Untersuchungen zugelassen, zunächst nur für Kopfscans und die kleinen Gelenke. Der Vorteil von 7-T-MRT liegt nicht nur in der höheren Auflösung. „Es gibt eine gegenseitige Abhängigkeit von Empfindlichkeit und Zeit“, erläutert Ladd: „Mit einer Feldstärke von 1,5T kann fast alles untersucht werden, was auch mit 7T untersucht wird, aber nicht in derselben Zeit.“ 3T-Geräte werden in vielen Fällen dazu genutzt, dieselben Untersuchungen schneller als bei 1,5T durchzuführen. Bei 7T hingegen werde der Gewinn in der Regel in eine höhere räumliche Auflösung, also mehr Detailgenauigkeit, investiert. „Es ist vergleichbar mit dem Unterschied zwischen Standard- und HD-Auflösung beim Fernsehen: Man erkennt plötzlich Dinge, die vorher nicht zu sehen waren“, sagt Ladd. Die sogenannten Schwalbenschwanzzeichen in den Basalganglien etwa, deren Fehlen ein Hinweis auf eine Parkinson-Erkrankung ist, sind bei einer Feldstärke von 3T bestenfalls zu erahnen, während sie mit 7T eindeutig sichtbar sind.
Gradientenspulen – die Grenzen der Physik ausloten
Ganzkörper-PET-CTs könnten neue Möglichkeiten in der Bildgebung, die bislang aufgrund zu hoher Strahlenbelastung ausgeschlossen waren, und auch neue Möglichkeiten bei der Darstellung von Therapieverläufen eröffnen
Mark Ladd
Generell ist in der MRT-Bildgebung ein Trend zu stärkeren Gradienten-Feldern zu beobachten, führt Ladd eine weitere aktuelle Entwicklung an. Je schneller der Gradient, desto größer allerdings die Gefahr der Stimulation peripherer Nerven: Dieser Umstand setzte bislang dem Einsatz stärkerer Gradienten-Felder eine Grenze. GE Healthcare hat inzwischen ein neues 3T-System nur für den Kopf entwickelt, das schnellere Gradienten gestattet, weil bei Kopfuntersuchungen die Probleme mit der Nervenstimulation geringer ausfallen. Ersten Forschungsgruppen wiederum ist es gelungen, die Nervenstimulation von Gradientenspulen im Vorfeld zu simulieren. Bislang wurde die Stärke der Nervenstimulation bei bereits fertig entwickelten Gradientenspulen gemessen und anschließend die Obergrenze für die Leistung der Spule festgesetzt. Mittlerweile lässt sich das am Computer vorhersagen, so dass die Spule bereits während der Entwicklung entsprechend optimiert werden kann. „Wir werden in den nächsten Jahren Gradientensysteme sehen, die deutlich stärker sind“, resümiert Ladd.
PET-CT und der 2-Meter-Detektor
Zu guter Letzt wurde im Bereich PET-CT der erste Ganzkörpertomograph entwickelt. Das chinesische Unternehmen United Imaging hat dazu einen Detektor von sage und schreibe zwei Meter Länge entwickelt. Siemens hingegen arbeitet an einem Gerät, das durch die Kombination von vier herkömmlichen Detektoren eine PET-CT-Untersuchung über eine Länge von immerhin etwas über einem Meter möglich macht. „Ganzkörper-PET-CTs könnten neue Möglichkeiten in der Bildgebung, die bislang aufgrund zu hoher Strahlenbelastung ausgeschlossen waren, und auch neue Möglichkeiten bei der Darstellung von Therapieverläufen eröffnen“, erklärt Ladd.
Profil:
Prof. Dr. sc. techn. Mark Ladd ist Leiter der Abteilung für Medizinische Physik in der Radiologie am Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg und Präsident der Deutschen Gesellschaft für Medizinische Physik (DGMP). Seine Forschungsschwerpunkte liegen im Bereich der Magnetresonanztomographie (MRT), insbesondere in der Einführung und Weiterentwicklung neuer Methoden bei sehr hohen Magnetfeldern und bei der Anwendung der MRT in der bildgeführten Strahlentherapie. Nach dem Studium der Elektrotechnik an der University of Michigan in Ann Arbor und der Stanford University in Kalifornien promovierte er 1998 an der ETH in Zürich im Rahmen einer Forschungskooperation zwischen dem Universitätsspital Zürich und GE. Als Professor für Biomedizinische Bildgebung am Universitätsklinikum Essen vertiefte er ab 2004 seine Forschungsinteressen im Bereich der Ultrahochfeld-MRT, bevor er 2013 nach Heidelberg wechselte.
24.09.2020





