© Karin Kaiser / MHH
News • Gerinnungsstörung
Auszeichnung für "Gen-Transporter" gegen Hämophilie A
Hämophilie A ist eine erblich bedingte Störung der Blutgerinnung. In Deutschland sind etwa 4.000 Menschen betroffen. Bei ihnen ist der sogenannte Gerinnungsfaktor VIII (FVIII) gestört oder fehlt ganz. Bei Verletzungen gerinnt das Blut dann langsamer, was zu chronischen Gelenkschäden oder akut lebensbedrohlichen Situationen führen kann.
Eine bereits verfügbare Gentherapie hilft nur bestimmten Patienten, die keine Antikörper gegen den viralen Vektor bilden, der als Genfähre eine intakte Kopie des FVIII-Gens in den Körper einschleusen soll. Dr. Simon Krooss, Wissenschaftler an der Klinik für Gastroenterologie, Hepatologie und Endokrinologie der Medizinischen Hochschule Hannover (MHH), hat eine Idee für ein neues Gentransportmittel, das unerkannt am Immunsystem vorbeikommt. Dafür wurde der Biologe und angehende Arzt jetzt mit dem „Bayer Hemophilia Award“ in der Kategorie Grundlagenforschung ausgezeichnet. Die Fördersumme beträgt rund 60.000 Euro.
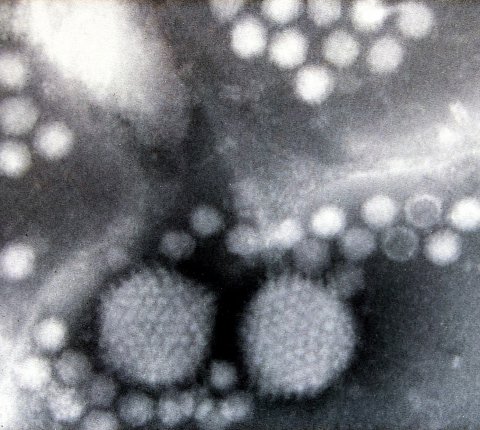
Bildquelle: Graham Beards, AAVs by electron microscopy, CC BY-SA 4.0
Bislang wird Hämophilie A mit der bereits etablierten AAV-Gentherapie behandelt. Dabei wird die Proteinhülle des Adeno-assoziierten Virus (AAV) mit einer funktionstüchtigen Kopie des FVIII-Gens ausgestattet. AAV schleust als viraler Vektor die FVIII-Kopie in Leberzellen ein, die dann das entsprechende Protein – den Gerinnungsfaktor VIII – bilden können. AAV-Vektoren werden als häufig als Genfähren verwendet, da sie selbst keine Krankheiten auslösen und sich ihr Erbgut nur selten unspezifisch in das Genom der Wirtszelle einbaut. Weil unser Immunsystem das eigentlich harmlose Virus meist aber als fremd erkennt, kann es jedoch Antikörper gegen die Genfähre bilden und so den gewünschten Behandlungserfolg verhindern. Das Forschungsteam um Dr. Simon Krooss möchte daher ein neues Transportmittel entwickeln, das die Immunabwehr nicht auf den Plan ruft. Dafür will er die neue Lipid-Nanopartikeltechnologie nutzen.
Nanopartikel sind deutlich kleiner als 100 Nanometer, also kleiner als 100 Millionstel Millimeter. Zum Vergleich: Ein menschliches Haar ist etwa 70.000 Nanometer dick. Die winzigen Teilchen werden problemlos in Körperzellen aufgenommen und eignen sich dadurch gut als Transportmittel. „Diese Partikel können das FVIII-Gen verpacken und in die Leber transportieren“, sagt Dr. Krooss. Weil sie eine ähnliche Struktur aufweisen wie Fetttröpfchen aus dem natürlichen Fettstoffwechsel, erkennt das Immunsystem sie nicht als fremd. „Somit könnten alle Patientinnen und Patienten damit behandelt werden, unabhängig von vorher gebildeten Antikörpern“, erklärt der Biomediziner. Der Wissenschaftler hofft, langfristig mit einer oder zumindest wenigen Injektionen einen dauerhaften Therapieerfolg zu erzielen. Der Förderpreis gibt ihm nun die Möglichkeit, seinen Forschungsansatz weiter zu verfolgen und eine erfolgversprechende Alternative zur AAV-Gentherapie anzubieten.
Quelle: Medizinische Hochschule Hannover
02.10.2021