News • Molekulare Mechanismen
Der Schlüssel zur Arterienbildung
Die Arteriogenese ist ein elementares Ereignis – nicht nur während der Entwicklung, sondern auch im Erwachsenenleben. Viele kardiovaskuläre Krankheiten könnten überwunden werden, wenn die Bildung neuer Arterien angeregt werden könnte. Wissenschaftler um Ralf Adams des Max-Planck-Instituts für molekulare Biomedizin haben einen genetischen Ansatz in Mäusen entwickelt, um die molekularen Mechanismen des Arterienwachstums aufzudecken.
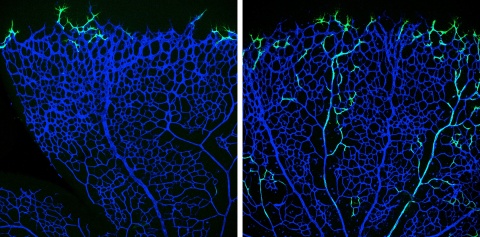
Zusammen mit Tilman Borggrefe der Justus-Liebig-Universität Gießen fanden sie heraus, dass der Rezeptor Notch in diesem Prozess essenziell ist. Dies könnte dabei helfen, neue therapeutische Ansätze zu identifizieren, die die Bildung neuer Arterien anregen.
Die Arterienbildung ist enorm wichtig, denn nur dieser Gefäßtyp kann genügend Blut in beeinträchtigte Gewebe transportieren. Wie das vaskuläre Netzwerk aufgebaut ist, ist noch nicht ausreichend gut erforscht – noch weniger ist bekannt, wie die Arteriogenese in therapeutischen Ansätzen stimuliert werden könnte. Die Max Planck Wissenschaftler haben nun die Angiogenese – die Bildung neuer Blutgefäße aus einem bestehenden Kapillarnetzwerk – im Gefäßnetzwerk der Retina von neugeborenen Mäusen untersucht.
Rezeptoren und Liganden einflussreich
„Die so genannten Leitzellen tasten im wachsenden Gefäßnetzwerk ihre Umgebung ab und weisen den nachfolgenden Endothelzellen die richtige Richtung“, sagt Mara Pitulescu, Erstautorin der Studie und Wissenschaftlerin in der Abteilung von Ralf Adams. Leitzellen werden gefolgt von so genannten Stalk-Zellen (to stalk, engl.: verfolgen), welche einen proliferativeren Charakter haben. Direkt hinter den Leit- und Stalk-Zellen sind die Blutgefäße zunächst in einem unausgereiften Plexus arrangiert, von dem aus Arterien, Venen und die verbindenden Kapillaren gebildet werden. Mittels Signalmolekülen interagieren Endothelzellen in diesem Netzwerk andauernd mit benachbarten Zellen und ihrer Umgebung. Diese Interaktionen basieren auf Rezeptoren, die sich auf der Oberfläche von Endothelzellen befinden und auf Liganden, die an die Rezeptoren binden. Vor allem der Notch-Rezeptor und sein Ligand Dll4 sind, neben anderen Rezeptoren und Liganden, für die Angiogenese wichtig.
Um die genauen Mechanismen der Arterienbildung in Mäusen zu studieren, verwendete das Team um Ralf Adams einen eleganten genetischen Ansatz in Mäusen, bei dem nur die Leitzellen und deren Abkömmlinge markiert werden und über die Zeit verfolgt werden können. „Erstaunlicherweise fanden wir heraus, dass die Abkömmlinge der Leitzellen entgegen der allgemeinen Wachstumsrichtung des Plexus migrieren und sich innerhalb einiger Tage in Arterien integrieren“, sagt Pitulescu. Die Wissenschaftler konnten den Notch-Ligand Dll4 in Leitzellen gezielt inaktivieren und beobachten, wie sich das Gefäßnetzwerk ausbreitete.
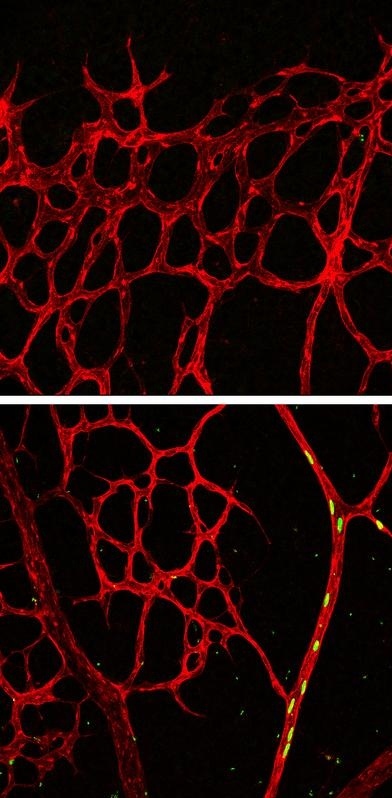
Interessanterweise ist Dll4 nicht erforderlich, um Leitzellen in ihrer Position am Rande des wachsenden Gefäßbettes zu halten. „Vielmehr fanden wir heraus, dass CXCR4, ein für Zellmigration wichtiger Chemokin-Rezeptor, für die Erhaltung der Leitzellen notwendig ist“, sagt Pitulescu. Die Experimente verdeutlichten allerdings die Rolle von Dll4: „Wenn Dll4 nicht vorhanden ist und der Notch-Rezeptor dadurch nicht aktiviert wird, verschlechtert sich die Rückwärts-Migration der Leitzellen“, sagt Pitulescu.
Notch reguliert die Arterienbildung
„Dies ist die erste Studie in Mäusen, in der gezeigt wird, dass die direkte Verbindung zwischen Sprossung und Arterienbildung gleichermaßen von Notch reguliert wird“, sagt Ralf Adams, der auch Professor der Medizinischen Fakultät der Westfälischen Wilhelms-Universität Münster und Mitglied des Exzellenzclusters „Cells in Motion“ ist. „Diese Ergebnisse sind von großer Bedeutung für das Verständnis des arteriellen Wachstums“, sagt Tilman Borggrefe, der mit seinem Team die biochemischen Analysen der Studie durchführte. „Dies könnte die Grundlage für einen neuen therapeutischen Ansatz sein, in dem bei Bedarf an Arterienbildung die Angiogenese über Notch kontrolliert werden könnte“, sagt Borggrefe.
Quelle: Max-Planck-Institut für molekulare Biomedizin
19.07.2017