News • Wirkstoffe gegen Hirnerkrankungen
Smarte Biomarker sollen neue Medikamente gegen Alzheimer & Co. finden
Mit der Technologieplattform "i3D-Markers" wollen Dr. Hayder Amin und Dr. Caghan Kizil vom DZNE-Standort Dresden die Entwicklung von Medikamenten gegen Hirnerkrankungen beschleunigen. Dafür verbinden sie hochdichte Mikroelektroden-Arrays und dreidimensionale Netzwerke menschlicher Nervenzellen zu einem Messsystem.
Bildquelle: DZNE / Amin Lab
Auf dieses werden zu prüfende Substanzen getropft und mittels künstlicher Intelligenz die Reaktion der Nervenzellen ermittelt. Mit ihrem Verfahren wollen die DZNE-Wissenschaftler die Auswahl aussichtsreicher Wirkstoffkandidaten für klinische Studien optimieren und dazu beitragen, Sackgassen in der Entwicklungspipeline zu vermeiden. Die Validierung dieses Ansatzes wird mit 820.000 Euro aus dem „Helmholtz-Validierungsfonds“ und mit Mitteln des DZNE finanziert, so dass sich das Gesamtbudget auf rund 1,2 Millionen Euro beläuft. Ziel der Forscher ist es, die neue Technologie für den industriellen Einsatz fit zu machen.
Die Entwicklung von Medikamenten ist kostspielig und von Rückschlägen gekennzeichnet. „In den letzten Jahren sind die meisten neuen Wirkstoffe gegen Hirnerkrankungen in Studien am Menschen gescheitert. Ein Grund dafür sind die ineffizienten In-vitro-Tests für neurologische Erkrankungen – vor allem während der frühen Phase der Medikamentenentwicklung, also vor Beginn klinischer Studien“, sagt Alzheimer-Forscher Dr. Caghan Kizil, der sich mit der Entwicklung experimenteller Krankheitsmodelle befasst. Sein Dresdner Kollege, Dr. Hayder Amin, meint: „Die bestehende Methodik hat ein grundsätzliches Manko. Das menschliche Gehirn ist enorm komplex und kann von den derzeit im Labor verwendeten Methoden nicht angemessen modelliert werden. Diese sind zu vereinfachend, um den wahren Effekt eines Wirkstoffes auf neuronale Netzwerke erkennen zu können. Insbesondere zweidimensionale Zellkulturen und herkömmliche Methoden der Datenerhebung können die komplizierten elektrophysiologischen und zellulären Eigenschaften des Gehirns nicht erfassen.“ Amin, der über umfangreiche Expertise in der Neurowissenschaft, Neurotechnologie und der Untersuchung der Dynamik von Nervenzellen mittels computergestützter Verfahren verfügt, ergänzt: „Es gibt daher einen dringenden Bedarf an Werkzeugen, die die Entwicklung neuer Medikamente besser unterstützen.“
Die Dresdner Forscher gehen dieses Problem mit ihrer Technologieplattform „i3D-Markers“ an. Sie könnte eine entscheidende Frage im Zuge der Entwicklung von Medikamenten beantworten: „Wie würde sich ein bestimmter Arzneistoff-Kandidat auf die Netzwerke des menschlichen Gehirns auswirken: gut oder schlecht?“. Die Erfahrung zeigt, dass diese Frage vor klinischen Studien am Menschen schwer zu beantworten ist. „Tatsächlich scheitern viele Wirkstoffkandidaten, die im Labor oder Tierversuch medizinisches Potenzial zeigen, in klinischen Studien aufgrund unerwünschter Wirkungen auf das menschliche Gehirn“, so Amin. Die DZNE-Wissenschaftler sind zuversichtlich, dass i3D-Markers neue Impulse geben kann. „Unser Ziel ist es, zu validieren, dass unsere Technologie besser als derzeitige Methoden vorhersagen kann, ob ein experimenteller Wirkstoff die beabsichtigte Wirkung auf den Menschen haben wird. Das wird hoffentlich helfen, den Weg zu neuen Medikamenten zu beschleunigen, Sackgassen in der Medikamentenentwicklung zu vermeiden und Entwicklungskosten zu senken“, sagt Kizil.
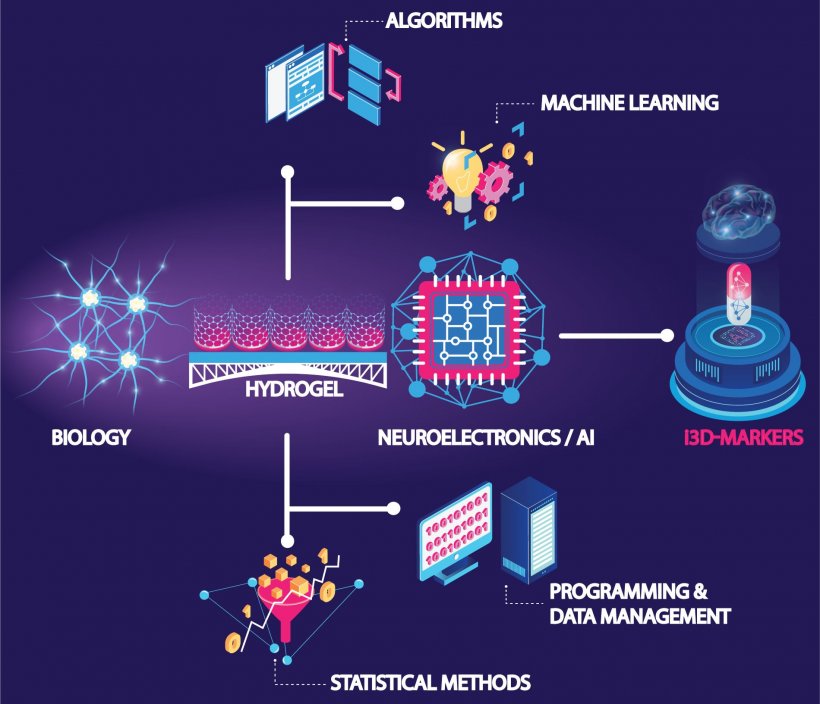
Bildquelle: DZNE / Amin Lab
Das Konzept der Dresdner Forscher verschmilzt Neuroelektronik mit einer innovativen Zellkulturmethode. „i3D-Markers nutzt neuronale Zellkulturen, die mit einem Mikrochip gekoppelt sind. Das heißt, wir züchten Nervenzellen auf elektronischen Bauteilen, die dicht angeordnete Mikroelektroden beinhalten. Dabei bilden die Nervenzellen ein dreidimensionales Geflecht, wie es im Gehirn vorkommt. Dieser Aufbau ermöglicht es uns, die elektrische Aktivität von Tausenden von Nervenzellen gleichzeitig mit hoher räumlicher und zeitlicher Auflösung zu erfassen“, erklärt Amin. „Diese Anordnung von vielen winzig kleinen Sensoren gibt uns Einblicke in die Dynamik dieses sehr komplexen Netzwerks aus menschlichen Nervenzellen. Wir werden High-Content-Daten in noch nie dagewesener Detailtiefe und Einzelzellauflösung erhalten.“ Ein zu testender Wirkstoff wird in definierter Konzentration auf die Nervenzellen getropft. „Dann beginnt man mit der Aufzeichnung elektrophysiologischer Daten, die von unserem Array von Sensoren erfasst werden“, sagt Kizil.
Durch künstliche Intelligenz und spezielle mathematische Ansätze wollen wir sogenannte funktionelle Biomarker entwickeln, die auf der Aktivität des neuronalen Netzwerks beruhen
Hayder Amin
Obwohl das Netzwerk aus mehr als hunderttausend Nervenzellen bestehen wird, würde diese Zellkultur einschließlich des Mikrochips auf eine Fläche passen, die zehnmal kleiner ist als eine 2-Eurocent-Münze. Die Informationen über die neuronale Aktivität werden allerdings komplex sein, da sie von Tausenden von Mikrokontaktsensoren stammen. Für die Analyse werden die Wissenschaftler daher Methoden der künstlichen Intelligenz einsetzen. Solche Algorithmen identifizieren und extrahieren Muster aus komplexen, mehrdimensionalen Daten. „Durch künstliche Intelligenz und spezielle mathematische Ansätze wollen wir sogenannte funktionelle Biomarker entwickeln, die auf der Aktivität des neuronalen Netzwerks beruhen. Diese Biomarker werden uns mitteilen, ob es dem Netzwerk gut geht oder nicht und ob ein bestimmter Wirkstoff diesen Zustand beeinflusst. Das wird uns helfen, vielversprechende Wirkstoffe zu identifizieren“, sagt Amin.
Die DZNE-Wissenschaftler starten nicht bei null: Vorherige Studien haben gezeigt, dass die verschiedenen Technologien, die in diesem Projekt enthalten sind, tatsächlich erfolgreich zusammengeführt werden können. Auf dieser Grundlage zielt der nun beginnende Validierungsprozess darauf ab, eine Technologieplattform zu entwickeln, die schließlich bis zur Marktreife gebracht werden kann. Ein Gremium aus wissenschaftlichen Beratern wird an dem Projekt beteiligt sein, ebenso wie mehrere Doktoranden und Postdocs. Darüber hinaus werden sich Industriepartner aus den Bereichen Mikrotechnik und Arzneimittelherstellung mit Sachleistungen beteiligen. „Wir haben das Ziel, innerhalb der nächsten zwei Jahre einen voll funktionsfähigen Prototyp zu bauen und zu testen“, sagt Amin. „Wenn die Technologie für die Routineanwendung bereit ist, würden wir zunächst einen Inhouse-Service für externe Kunden anbieten. Das könnten Forschungseinrichtungen und Pharmaunternehmen sein. Langfristig streben wir die Gründung eines Start-ups an.“
Quelle: Deutsches Zentrum für Neurodegenerative Erkrankungen
27.06.2021