News • Hanta im Haushalt
Krank durch Frühjahrsputz?
Wer beim Frühjahrsputz Staub einatmet, setzt sich in manchen Gebieten Deutschlands einem erhöhten Infektionsrisiko durch Hanta-Viren aus. Diese finden sich unter anderem in Staub, der mit den Ausscheidungen infizierter Rötelmäuse kontaminiert ist. Wissenschaftler der Goethe-Universität und des Senckenberg Biodiversität und Klima Forschungszentrums haben die Entwicklung von Hanta-Infektionen in Deutschland nun anhand von Langzeitdatenreihen untersucht und festgestellt: Erhöhte Gefahr droht im Frühsommer und in waldreichen Gebieten sowie nach „fetten Jahren“ für die Rötelmaus.
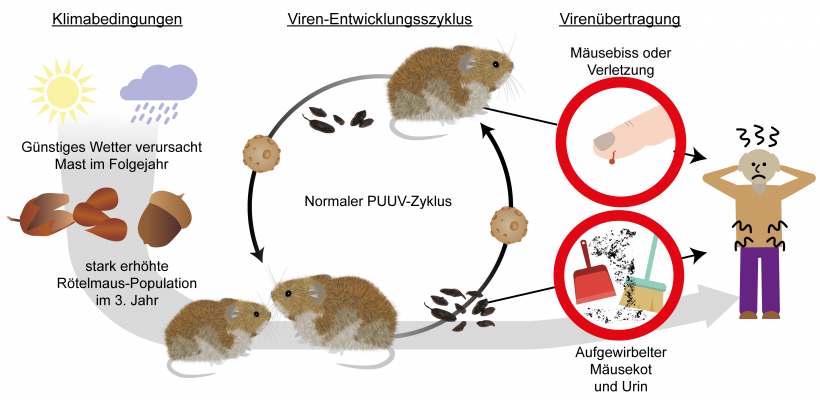
Hanta-Viren erregten erstmals Anfang der 1950er öffentliches und wissenschaftliches Interesse, als zahlreiche amerikanische Soldaten sich in Korea mit dem damals unbekannten Erreger infizierten und an hämorrhagischem Fieber erkrankten. Dies ist vor allem wegen der erhöhten Blutungsneigung gefährlich, die zu akutem Nierenversagen führen kann. In Deutschland wurden Infektionen mit Hanta-Viren Mitte der 1980er Jahre bekannt. In den meisten Fällen ist das durch die Rötelmaus (Myodes glareolus) übertragene Puumala-Virus (PUUV) die Ursache. Die Maus selbst erkrankt nicht, kann den Erreger aber zum Beispiel durch einen Biss auf den Menschen übertragen. Auch durch Kot, Urin oder erregerhaltige Aerosole, die beispielsweise während Reinigungsarbeiten in der Land- und Forstwirtschaft aufgewirbelt und eingeatmet werden, kann es zur Infektion kommen.

Belastbare Daten über die Häufigkeit der Hanta-Virus-Infektionen sind in Deutschland seit der Einführung der Meldepflicht im Jahr 2001 verfügbar. Besonders viele Puumala-Virus-Infektionen treten in Baden-Württemberg und angrenzenden Gebieten in Bayern und Nordrhein-Westfalen auf. In Nordostdeutschland gibt es dagegen wenige PUUV-Virus-Fälle. In großen Städten und Ballungsgebieten (Berlin, Stuttgart, Bonn) ist die Zahl der PUUV-Infektionen pro 100.000 Einwohner tendenziell höher als in ländlichen Gebieten. Während die räumlichen Muster über die letzten 15 Jahre ähnlich geblieben sind, gab es starke zeitliche Schwankungen: So war die Zahl der gemeldeten PUUV-Infektionen in den Jahren 2007, 2010 und 2012 besonders hoch.
Die Gruppe von Prof. Sven Klimpel von Institut für Ökologie, Evolution und Diversität der Goethe-Universität hat diese Daten zusammen mit Kollegen des Senckenberg Biodiversität und Klima Forschungszentrum untersucht, um räumliche, zeitliche und saisonale Muster für das Auftreten der Infektion zu identifizieren. Wie die Wissenschaftler in der aktuellen Ausgabe von „PeerJ“ mitteilen, gelten als wichtige Faktoren für die Rötelmausdichte die Landnutzung (insbesondere der Waldanteil), klimatische Faktoren (kalte Winter) und das Nahrungsangebot. Jahre, in denen Buche, Eiche und Kastanie besonders viele Früchte produzieren (Mastjahre), bedeuten ein reiches Nahrungsangebot für den Krankheitsüberträger. Das führt oft zu einem starken Anstieg der Populationsdichte und damit zu mehr infizierten Rötelmäusen, was letztlich auch das Infektionsrisiko für den Menschen erhöht. Tatsächlich gingen den infektionsreichen Jahren 2007, 2010 und 2012 jeweils Mastjahre voraus. Allerdings folgte auf das Mastjahr 2014 nur ein Jahr mit leicht erhöhter Anzahl an humanen Puumala-Virus Infektionen. Entscheidend für das Auftreten von Mastjahren sind wiederum klimatische Bedingungen in den Vorjahren und der zeitliche Abstand zum vorhergehenden Mastjahr.
Aufgrund der komplexen Zusammenhänge und der Vielzahl an Faktoren, die Einfluss auf die Zahl der Puumala-Virus-Infektionen haben, ist es derzeit noch schwierig, ein zuverlässiges Vorhersage-Modell zu erstellen. Anhand von Korrelationsanalysen konnte die Gruppe aber ein höheres Risiko für waldreiche Gebiete ableiten sowie für den Frühsommer und für Jahre, die auf ein Mastjahr folgen. „Durch den Klimawandel, der häufigere Mastjahre und mildere Winter mit sich bringt, könnte die Zahl der Puumala-Virus-Infektionen künftig ansteigen“, prognostiziert Klimpel.
Quelle: Goethe-Universität Frankfurt am Main
06.02.2018