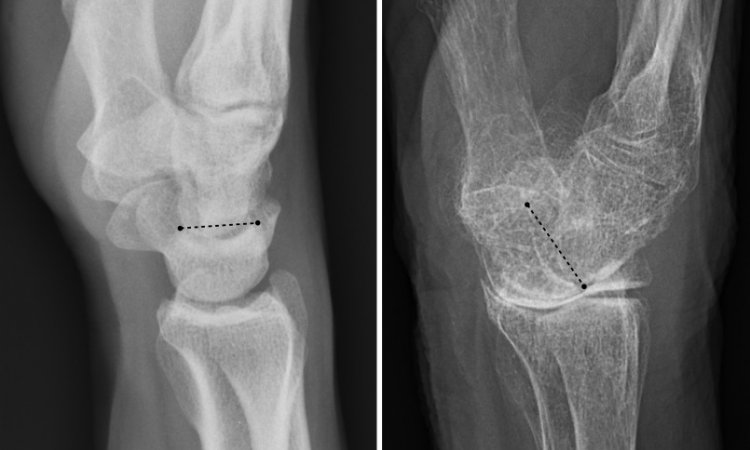
Bildquelle: ShakataGaNai, XrayOITypeV-Kid, bearbeitet, CC BY-SA 2.5
News • Osteogenesis imperfecta
Glasknochenkrankheit: neuer Behandlung auf der Spur
Extrem brüchig wie Glas sind die Knochen bei Menschen mit der genetisch bedingten Erkrankung Osteogenesis imperfecta (OI). Von der „Glasknochenkrankheit“ sind besonders Kinder, aber auch Erwachsene betroffen.
Man kennt zwar bereits verschiedene Gene, in denen Veränderungen zu einer gestörten Knochenbildung und zur Entstehung der Glasknochenkrankheit führen können. Dennoch bleibt bei einigen Patienten der ursächliche Gendefekt bislang ungeklärt.
Unter Federführung der Arbeitsgruppe um Prof. Dr. Bernd Wollnik, Direktor des Instituts für Humangenetik der Universitätsmedizin Göttingen (UMG), entdeckten Wissenschaftler aus Deutschland, Brasilien, Portugal, England und der Schweiz nun ein weiteres Gen, das bei der Entstehung der Glasknochenkrankheit eine Rolle spielt. Wenn das Gen MESD mutiert oder verändert ist, kann sich dies offenbar auf den WNT-Signalweg auswirken, der auch für Knochenwachstum und -stärke wichtig ist. Diese neuen Erkenntnisse eröffnen nach Ansicht der Forscher für eine mögliche Behandlung neue Perspektiven. Wirkstoffe, die den WNT-Signalweg aktivieren, könnten sich als Therapie für bestimmte Patienten eignen. Die Forschungsergebnisse wurden im Fachjournal „American Journal of Human Genetics“veröffentlicht.
MESD wurde bislang noch mit keiner Erkrankung beim Menschen in Verbindung gebracht, aber wir wussten, dass es für den WNT-Signalweg wichtig ist
Bernd Wollnik
Eine Heilung der Glasknochenkrankheit ist bislang nicht möglich. Die Behandlung stützt sich auf die operative Behandlung, Physiotherapie und die medikamentöse Gabe von Bisphosphonaten. Bei den Patienten der aktuellen Studie zeigte ein Behandlungsversuch mit Bisphosphonaten jedoch keinen Erfolg. Für Prof. Wollnik eröffnen sich durch die Studienergebnisse auch im Hinblick auf die Behandlung solcher Patienten neue Perspektiven: „Unsere Zellexperimente liefern uns einen Hinweis auf einen möglichen neuen Behandlungsansatz: Wirkstoffe, die den WNT-Signalweg aktivieren, könnten sich demnach eventuell als Therapie für bestimmte Patienten eignen. Ein derartiges Medikament gibt es bereits und wird bei Patienten mit altersbedingter Osteoporose eingesetzt, um die Knochenbildung und -masse zu steigern“.
Bei fünf Patienten mit fortschreitenden Verformungen des Skeletts, bei denen bereits im Mutterleib oder vor dem zweiten Lebensjahr zahlreiche Knochenbrüche aufgetreten waren, fanden die Forscher Mutationen in einem neuen Gen: MESD. „Bei allen führten wir eine Exomsequenzierung durch. Wir analysierten gleichzeitig alle kodierenden Bereiche aller 19.000 Gene der menschlichen Erbinformation. Zuvor hatten wir ausgeschlossen, dass Veränderungen in einem der für die Glasknochenkrankheit bereits bekannten Gene in Frage kamen. Stattdessen trugen alle betroffenen Kinder jeweils eine Mutation in beiden Kopien des MESD-Gens. MESD wurde bislang noch mit keiner Erkrankung beim Menschen in Verbindung gebracht, aber wir wussten, dass es für den WNT-Signalweg wichtig ist. Damit hatten wir einen sehr viel versprechenden Kandidaten", sagt Wollnik.
Der WNT-Signalweg ist ein Zusammenspiel aus verschiedenen Molekülen, die u.a. die Embryonalentwicklung, die Zelldifferenzierung und die Zellteilung regulieren. Das vom MESD-Gen kodierte Protein agiert dabei nicht direkt im WNT-Signalweg. Als so genanntes „Chaperon“ sorgt es indirekt über bestimmte Domänen in seiner Struktur dafür, dass spezifische WNT-Rezeptormoleküle, LRP5 und LRP6, die für ihre korrekte Funktion erforderliche Proteinfaltung einnehmen und in der Zelle vom Endoplasmatischen Retikulum zur Zellmembran gelangen.
Dieser Artikel könnte Sie auch interessieren
News • Wichtiges Protein
Wie Chaperone die Krebsabwehr in Gang halten
Über Leben und Tod einer Zelle entscheidet das Anti-Tumor-Protein p53: Erkennt es Schäden im Erbgut, treibt es die Zelle in den Selbstmord. Eine neue Forschungsarbeit an der Technischen Universität München (TUM) zeigt, dass diese körpereigene Krebsabwehr nur funktioniert, wenn bestimmte Proteine, die Chaperone, dies zulassen.
In Experimenten mit unterschiedlichen Zellmodellen untersuchten die Forscher, wie sich die gefundenen Mutationen auf Zellebene auswirken. Dabei zeigte sich, dass diese aufgrund ihrer spezifischen Lage innerhalb des Proteins zwar die Funktion von MESD herabsetzen, sie aber nicht komplett ausschalten. Dass der WNT-Signalweg eine Rolle für Knochenwachstum und -stärke spielt, war bereits belegt. Auch die Arbeitsgruppe um Prof. Wollnik hatte schon vor einigen Jahren nachgewiesen, dass mit WNT1 ein Baustein dieses Signalwegs für die Knochenbildung und die Funktion von Knochenzellen bedeutsam ist.
Quelle: Universitätsmedizin Göttingen (UMG)
27.10.2019