Artikel • Herz-Mapping
Kardiale MRT: messen statt sehen
In der Vergangenheit eine Domäne der CT, ist die kardiale MRT als Schnittbildverfahren auf dem Weg, ihren Stellenwert im Rahmen der Stufendiagnostik kontinuierlich auszubauen.
„Die MRT des Herzens bietet eine sehr gute zeitliche und räumliche Auflösung und erlaubt darüber hinaus eine spezifische Gewebecharakterisierung. Sie ermöglicht zudem eine präzise Beurteilung der Morphologie des Herzens, der herznahen Gefäße sowie der Wandbewegung des Herzens“, sagt Professor Dr. Ulrich Kramer, Leitender Oberarzt der Abteilung Diagnostische und Interventionelle Radiologie an der Universität Tübingen.
In welchen Bereichen hat die kardiale MRT Vorzüge im Vergleich zu anderen Modalitäten?
Insbesondere in den Bereichen Kardiomyopathie und Myokarditis gewinnt die MRT zunehmend an Bedeutung, weil wir mit ihr nicht-invasiv eine Gewebecharakterisierung vornehmen können. Das heißt, wir können bildgebend sehr schonend nachweisen, ob es strukturelle oder entzündliche Veränderungen, eine Fibrosierung oder auch Texturstörungen des Myokards gibt. Wir können also bildmorphologisch zeigen, ob die Struktur des Herzens hochauffällig ist.
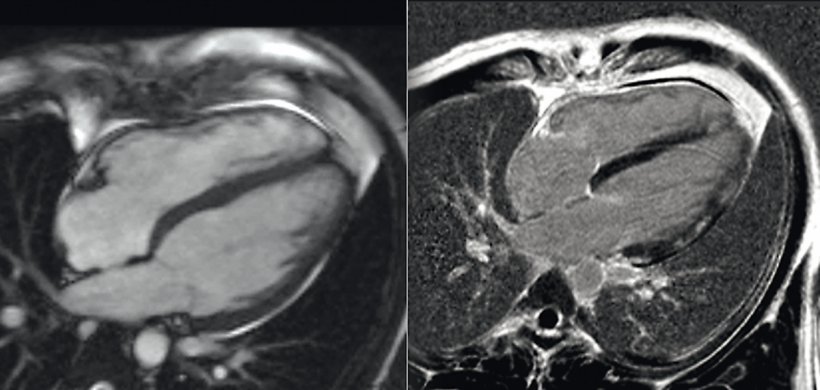
29-jähriger Patient mit subjektiv angegebener Abgeschlagenheit sowie echokardiographisch reduzierter Ventrikelfunktion (EF 45%). Noch normal großer linker Ventrikel (enddiastolisches Volumen 130 ml) mit nachgewiesener regionaler Wandbewegungsstörung der lateralen Wandsegmente (nicht dargestellt) sowie Nachweis eines fleckförmigen, teils mittmyokardialen, teils epikardialen Late Gadolinium Enhancements, welches charakteristisch für eine Myokarditis ist.
Klinisch ist der Formenkreis der nicht-ischämischen Herzerkrankungen bisweilen schlecht zu differenzieren. Insbesondere die Unterscheidung zwischen einer entzündlich bedingten Myokarditis und einer primären Kardiomyopathie stellt eine gewisse Herausforderung dar, da sich die klinischen Symptome kaum unterscheiden. Hier zeigt sich die Stärke der kardialen MRT, da sie eine Differenzierung zwischen ischämischen und nicht-ischämischen Herzerkrankungen zuverlässig ermöglicht.
Natürlich kann dies im Einzelfall keine Myokardbiopsie ersetzen, die MRT gibt aber wichtige Hinweise, ob der Patient eine entzündliche Erkrankung wie beispielsweise eine Myokarditis hat. Auch in der Abklärung ischämischer Herzerkrankungen kommt der Darstellung von Narbengewebe bzw. fibrotisch umgebautem Herzmuskelgewebe eine besondere Bedeutung zu. So gilt es, nach einem Herzinfarkt um das eigentliche Infarktareal noch genug gesundes, jedoch schlecht durchblutetes Herzmuskelgewebe nachzuweisen. Denn nur dann hat eine erfolgreiche Therapie (Revaskularisierung) mittels Bypass oder Stent Aussicht auf eine resultierende Funktionsverbesserung der geschädigten Herzmuskelabschnitte. Die Abklärung einer Ischämie bzw. der Vitalität des Herzmuskels ist daher seit vielen Jahren eine Domäne der kardialen MRT.
Und wo sehen Sie die Limitationen der kardialen MRT?
Kommt bei ohnehin kritisch kranken Patienten im MRT noch die Aufregung und/oder eine Platzangst hinzu, wird der Patient möglicherweise tachykard oder entwickelt Herz-Rhythmus-Störungen.
Professor Dr. Ulrich Kramer
Die Koronargefäße weisen teilweise nur einen Durchmesser von unter einem Millimeter auf und bewegen sich sehr schnell im Takt des Herzschlags. Eine direkte Darstellung der Herzkranzgefäße stellt hohe Anforderungen an örtliches und zeitliches Auflösungsvermögen und ist damit -methodisch bedingt - im MRT limitiert; die direkte Darstellung der Herzkranzgefäße ist somit Aufgabe der kardialen CT.
Auch die Patientenkonstitution stellt eine Herausforderung dar. Kommt bei ohnehin kritisch kranken Patienten im MRT noch die Aufregung und/oder eine Platzangst hinzu, wird der Patient möglicherweise tachykard oder entwickelt Herz-Rhythmus-Störungen. Oder er ist in Folge von Begleiterkrankungen nicht in der Lage, ausreichend lange die Luft anzuhalten. Dies alles sind Faktoren, die das Prozedere stören, da wir neben der herzeigenen Bewegung auch die atemmodulierten Bewegungen des Zwerchfells ‚einfrieren‘ müssen, um adäquat scharfe Bilder zu generieren.
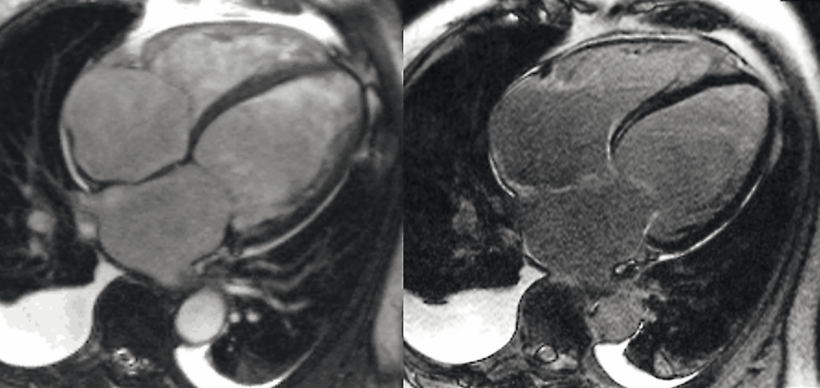
55-jähriger Patient mit DCM. Neben einem beidseitigen Pleuraerguss (rechts mehr als links) erkennt man eine globale Dilatation beider Herzkammern mit typischer Konfiguration und einem linksventrikulären enddiastolischen Diameter (LVEDD) über 5,5 cm, einem enddiastolischen Volumen von 240 ml und einem mittmyokardialen linearen Late Gadolinium Enhancement des basalen Ventrikelseptums. Nebenbefundlich ließen sich zusätzlich eine begleitende Trikuspidal- und Mitralklappen-insuffizienz infolge der globalen Dilatation nachweisen.
Welche zukünftigen Einsatzmöglichkeiten wird die MRT des Herzens haben?
Die Möglichkeiten der kardialen MRT sind noch lange nicht ausgeschöpft. Neuerdings entfernen wir uns von der reinen Diagnostik und gehen eher in Richtung Therapiekontrolle, Prognoseabschätzung und Risikostratifizierung. Nach einer Pulmonalvenenisolation haben wir beispielsweise die Möglichkeit, den Therapieeffekt zu visualisieren. Bei der Ablation werden künstliche Narbenareale gesetzt, um die Erregungsleitungsstörungen zu unterbrechen, ein Prozess, den wir visualisieren können. Das ist zwar herausfordernd, kann aber dazu beitragen, dass der Interventionist bildmorphologisch veranschaulicht bekommt, in welchen Regionen Ablationen durchgeführt worden sind und ob sie erfolgreich verlaufen sind oder nicht.
Auf dem Weg von der wissenschaftlichen Forschung hin zur klinischen Routine bewegen wir uns auch mit sogenannten Mapping-Techniken, die die Gewebecharakterisierung weiter verfeinern. Denn Methoden zur Bestimmung der T1- und T2-Relaxationszeiten des Herzmuskels ermöglichen es, Fibrosen und Ödeme in den einzelnen Regionen des Myokardgewebes nicht nur qualitativ, sondern zukünftig auch quantitativ auszuwerten. Bisher haben wir unsere Erkenntnisse auf die rein visuelle Bildanalyse gestützt und konnten Aussagen darüber treffen, ob gesundes oder infarziertes Gewebe vorliegt. Diese Art der Schwarz/Weiß-Aussage hilft aber beispielsweise nicht bei nicht-ischämischen Herzerkrankungen. Denn da muss die globale, aber eher diffuse Schädigung des Herzmuskels beurteilt werden – das wiederum entzieht sich der rein visuellen Analyse.
Wie funktionieren Mapping-Techniken bei der kardialen MRT?
Das sind spannende Perspektiven, die bislang jedoch noch nicht flächendeckend zur Verfügung stehen.
Professor Dr. Ulrich Kramer
Ein Beispiel: Narbengewebe nimmt in der konventionellen Bildgebung mehr Kontrastmittel auf als normales Gewebe. Das heißt, dank vermehrter Kontrastmittelaufnahme kann Narbengewebe gut differenziert werden. Bei einer diffusen Schädigung, wie beispielsweise einer hypertrophen oder dilatativen Kardiomyopathie, erhalte ich mit den konventionellen Methoden dagegen irgendeinen nicht näher bestimmbaren Grauwert. Schädigungen, die diffus sind, können im Herzen somit visuell nicht korrekt erfasst werden. Die neuen ‚Mapping-Techniken‘ bieten hier Möglichkeiten, die T1-Relaxationszeiten quantitativ zu erfassen. Damit sind wir dann auch in der Lage, einen diffus geschädigten Herzmuskel als solchen zu erkennen, ohne ihn visuell als krankhaft zu bewerten.
Mit dieser Methode können wir einen objektivierbaren Befund präsentieren und im Sinne einer Verlaufskontrolle einen möglichen Therapieeffekt korrelieren. Das sind spannende Perspektiven, die bislang jedoch noch nicht flächendeckend zur Verfügung stehen.

Profil:
Professor Dr. Ulrich Kramer promovierte 1999 zum Thema „Magnetresonanztomographische Untersuchungen zur Morphologie, Funktion und zum Kontrastierungsverhalten des normalen menschlichen Myokards” an der Universität Tübingen. Dort legte er 2009 seine Habilitation zum Thema “Kardiale MR-Funktionsdiagnostik - Analyse technischer Parameter und klinische Anwendungen” ab. Von Januar 2013 bis März 2016 war Kramer Stellvertretender Ärztlicher Direktor am Institut für Diagnostische und Interventionelle Radiologie der Universität Tübingen. Seit April 2016 ist er Leitender Oberarzt der Abteilung Diagnostische und Interventionelle Radiologie an der Universität Tübingen.
03.02.2017