Bildquelle: Astrid Eckert/TUM
News • Einsatz zwischen den Zellen
Mikroroboter eröffnet Chancen für Krebsbehandlung und Wundheilung
Eine Forschendengruppe der Technischen Universität München (TUM) hat weltweit erstmals einen Mikroroboter entwickelt, der im Zellverbund navigieren und einzelne Zellen gezielt stimulieren kann.
Die Professorin für Nano- und Mikrorobotik Berna Özkale Edelmann sieht darin das Potenzial, neue Behandlungsmethoden für den Menschen zu finden. Die Wissenschaftler stellen im Fachjournal Advanced Healthcare Materials die neue Technik vor.
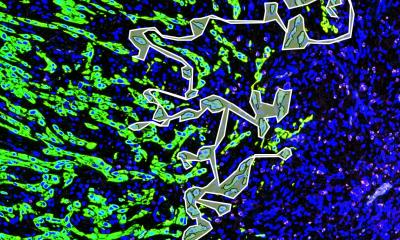
Sie sind rund, halb so dick wie ein Haar, enthalten Goldstäbchen und fluoreszierenden Farbstoff, sind umgeben von einem Biomaterial, das aus Algen gewonnen wird und können sich – angetrieben von Laserlicht – zwischen Zellen bewegen: Die winzigen Roboter sind eine Erfindung von Prof. Berna Özkale Edelmann. Genauer gesagt hat die Bioingenieurin und Leiterin des Microrobotic Bioengineering Labs mit ihrem Forschendenteam eine technologische Plattform entwickelt, mit der beliebig viele dieser Vehikel hergestellt werden können. Eingesetzt werden sie aktuell außerhalb des menschlichen Körpers, in vitro.

Bildquelle: Astrid Eckert/TUM
Die „TACSI-Microrobots“ unterscheiden sich von klassischen humanoiden Robotern oder Roboterarmen in Fabrikhallen. Denn das gesamte System erfordert ein Mikroskop für die Vergrößerung der Mikrowelten, einen Computer sowie einen Laser als Antriebswerkzeug für die etwa 30 Mikrometer großen Mikroroboter, die von einem Menschen gesteuert werden. Das Besondere: Die Roboter können nicht nur erwärmt werden, sie zeigen auch ständig ihre Temperatur an. Das ist wichtig, denn sie sollen sich nicht nur zu einzelnen Zellen hinbewegen, sondern lokal einzelne Zellen oder Zellverbünde erwärmen.
TACSI ist ein Kürzel und steht für „Thermally Activated Cell-Signal Imaging“. Einfach gesagt ist das ein bildbasiertes System, das in der Lage ist, Zellen zu erwärmen und dadurch zu aktivieren. „Wir haben zum ersten Mal weltweit ein System entwickelt, mit dem sich nicht nur Mikroroboter durch Zellverbände navigieren lassen, sondern Zellen auch gezielt, über Veränderungen der Temperatur, stimulieren lassen“, sagt Prof. Özkale Edelmann.
Die Basis für die Produktion von Mikrorobotern ist ein so genannter mikrofluider Chip, auf dem der Fabrikationsprozess abgebildet ist. Auf dem Chip wird von links durch einen Kanal Biomaterial zugeführt, dann von oben und unten über weitere 15 bis maximal 60 Mikrometer dicke Kanäle ein Öl mit spezifischen Komponenten zugegeben, bevor rechts dann fertige Mikroroboter herauskommen. Im Falle des TACSI-Mikroroboter werden folgende Bestandteile hinzugegeben:
- Ein fluoreszierender Farbstoff: Hier wurde das orange Rhodamin-B verwendet, das mehr und mehr seine Farbintensität verliert, je höher die Temperatur ist. So wird der Mikroroboter zum Thermometer für den Betrachter.
Bildquelle: Astrid Eckert/TUM
- Gold-Nanoteilchen: Die 25 mal 90 Nanometer kleinen Edelmetallzylinder haben die Eigenschaft, sich durch die Bestrahlung mit Laserlicht sehr schnell aufwärmen (und auch wieder abkühlen) zu können. Es dauert gerade einmal wenige Millisekunden, um den Roboter um fünf Grad zu erhitzen. Die Nanoteilchen können auf bis zu 60°C erwärmt werden. Durch den automatischen Temperaturausgleich der Nanoteilchen (Konvektion genannt) setzt sich der Roboter in Bewegung, mit einer Höchstgeschwindigkeit von 65 Mikrometer pro Sekunde.
„Bis zu 10.000 Mikroroboter können so in einem Produktionslauf hergestellt werden“, erläutert Wissenschaftler Philipp Harder aus dem Forschendenteam.

Bildquelle: Astrid Eckert/TUM
Um Vorgänge in der Zelle zu beeinflussen, reichen manchmal leichte Veränderungen der Temperatur aus. „Bei einer Verletzung an der Haut, etwa durch einen Schnitt, steigt die Körpertemperatur leicht an, wodurch das Immunsystem aktiviert wird“, erläutert Özkale Edelmann, die mehr darüber erfahren will, ob diese „thermische Stimulation“ für die Wundheilung eingesetzt werden kann. Auch in Hinsicht auf Krebszellen ist noch nicht ausreichend erforscht, ob sie durch Anregung aggressiver werden oder nicht. Aktuelle Studien zeigen, dass bei hohen Temperaturen (60°C) Krebszellen absterben und dass Arrhythmien im Herzen und Depressionen behandelt werden können.
Forschungen im Team von Prof. Özkale Edelmann an Zellen der Niere haben gezeigt, dass sich die Mechanismen der Ionenkanäle in Zellen beeinflussen lassen. Dafür navigierten die Forschenden mit den TACSI-Microrobots an die Zelle heran. „Über den Infrarotlaser haben wir die Temperatur erhöht und über die Intensität von Rhodamin-B die Temperatur bestimmt“, erläutert Wissenschaftler Harder. Und es zeigte sich, dass sich die Ionenkanäle der Zellen bei bestimmten Temperaturen öffneten und beispielsweise Calcium in die Zelle hineinließen. „Wir haben an diesem konkreten Beispiel gezeigt, dass Wärme konkrete Änderungen in der Zelle bewirkt, und zwar schon bei leichten Temperaturerhöhungen“, sagt Özkale Edelmann, die sich nun neue therapeutische Ansätze durch weitere Forschungen erhofft – etwa indem Wirkstoffe in die Zelle geschleust werden können.
Quelle: Technische Universität München
08.09.2023