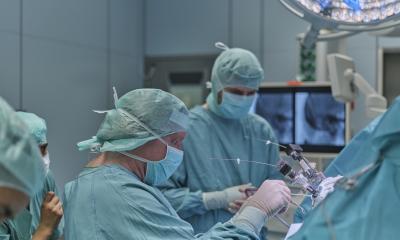
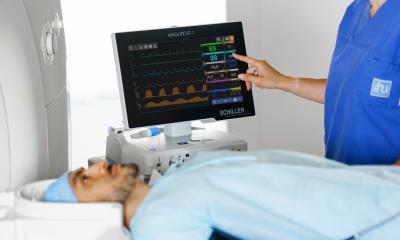
Quelle: BVMed
Artikel • Jahres-Pressekonferenz BVMed
Digitale Bestandsplattform soll Lieferengpässe während Pandemien vermeiden
Zu Beginn der Corona-Pandemie kam es zu Lieferengpässen bei Medizinprodukten und Pharmazeutika. Um diese in zukünftigen Krisensituationen zu vermeiden, möchte der Bundesverband Medizintechnologie (BVMed) eine digitale Bestandsplattform etablieren. Erste Gespräche mit dem Bundesgesundheitsministerium haben dazu bereits stattgefunden. Dr. Meinrad Lugan, BVMed-Vorstandsvorsitzender, hätte sich diesen Schritt jedoch schon viel früher gewünscht. Im Rahmen der digitalen Jahres-Pressekonferenz des deutschen MedTech-Verbandes kritisierte er: „Hätte die Bundesregierung unsere Expertise rechtzeitig einbezogen, hätte es nicht zu derartigen Engpässen kommen müssen. Aus unserer Sicht mangelt es an einer ausreichenden Wertschätzung der Branche in der Politik und der Öffentlichkeit.“
Report: Sonja Buske

Quelle: BVMed
Bei mehr als 80 Prozent aller kritischen Produkte gab es laut Lugan gar keinen Mangel, sondern ein Verteilungsproblem: „Spontane und multiple Bestellungen führten zu Lieferengpässen. Eine digitale Bestandsplattform versorgungskritischer Medizinprodukte wäre hier die Lösung.“ Aktuell gebe es für Deutschland allerdings keine Versorgungsengpässe. Produkte wie Handschuhe oder Masken werden zwar zum Teil zu höheren Preisen gehandelt, doch sei das vor allem für Länder ein Problem, die finanziell schlechter dastehen als Deutschland.
Die deutsche Medizintechnik ist auf dem Weltmarkt sehr erfolgreich. Die Exportquote lag nach eigenen Angaben im Jahr 2019 bei rund 65 Prozent, der Inlandsumsatz bei über 33 Milliarden Euro. Auch in Krisenzeiten müsse der weltweite freie Warenverkehr sichergestellt und globale Lieferketten dürften nicht durch staatliche Eingriffe unterbrochen werden, betonte Lugan.
Neue Kennzeichnung für britischen Markt
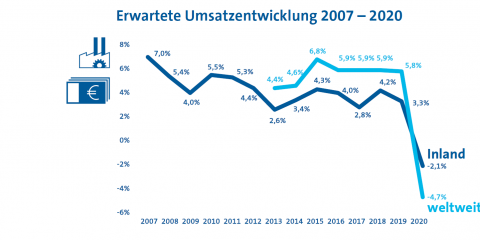
Sorge bereitet dem Vorstandsvorsitzenden die neue UKCA-Kennzeichnung (UK Conformity Assessed), die ab dem 1. Januar 2021 das CE-Zeichen auf dem britischen Markt als Folge des Brexits ersetzen wird. Alle Medizinprodukte müssen dann in Großbritannien neu registriert werden. „Kleinere Firmen werden sich diese Doppelbelastung nicht leisten können und als Folge den britischen Markt aufgeben“, so Lugan. Die Lage der Medizintechnik-Branche gut sechs Monate nach dem Lockdown war auch Thema der Herbstumfrage des BVMed. 118 Mitgliedsunternehmen insbesondere aus Deutschland und den USA haben sich an der Umfrage beteiligt. „56 Prozent der befragten Unternehmen gehen von einem Umsatzrückgang in diesem Jahr aus. Bei einem Drittel der Unternehmen sind die Umsatzrückgänge sogar im zweistelligen Bereich“, erläuterte der BVMed-Geschäftsführer Dr. Marc-Pierre Möll. Dies zeige, wie dramatisch die MedTech-Branche von der Verschiebung elektiver Eingriffe und den rückläufigen Arztbesuchen betroffen sei. Der Mehrbedarf an medizinischer Schutzausrüstung und Hygieneprodukten könne das nicht kompensieren.
Trotz der finanziellen Einbußen wollen die Unternehmen ihr sehr gut ausgebildetes Personal halten, wie die Umfrageergebnisse ebenfalls zeigen. Möglich wird dies unter anderem durch die Anmeldung von Kurzarbeit, wovon 38 Prozent der Unternehmen Gebrauch gemacht haben.
EU-Medizinprodukte-Verordnung sorgt für Probleme

Quelle: BVMed
Die größte Sorge bereitet den Mitgliedsunternehmen die neue EU-Medizinprodukte-Verordnung (MDR). Hunderttausende vorhandene Medizinprodukte müssen neu zertifiziert sowie die Zertifizierungsstellen für Medizinprodukte in der gesamten EU neu benannt werden. Der Prozess der Neuzertifizierung dauert in der Regel für jedes Produkt mindestens sechs Monate. Gleichzeitig muss eine Zertifizierung des Qualitätsmanagementsystems des jeweiligen Herstellers erfolgen. „56 Prozent der Unternehmen fordern eine vereinfachte Neuzertifizierung für bewährte Bestandsprodukte“, fasst Möll zusammen. „Wir benötigen pragmatische Lösungen, damit alle Produkte nach der EU-Medizinprodukte-Verordnung zertifiziert und Anwendern und Patienten zur Verfügung gestellt werden können.“
Auf nationaler Ebene setzt sich der Verband für einen schnellen Innovationszugang für moderne Medizintechnologien ein, insbesondere für digitale Gesundheitsanwendungen. Möll: „Wir wollen abgestimmte Maßnahmen gegen offensichtliche Defizite in der Versorgung, beispielsweise bei Diabetes, Adipositas oder Herz-Kreislauf-Erkrankungen.“
29.10.2020