News • Tumorzellen unter der Lupe
Aggressiver Krebs: neuer Mechanismus entdeckt
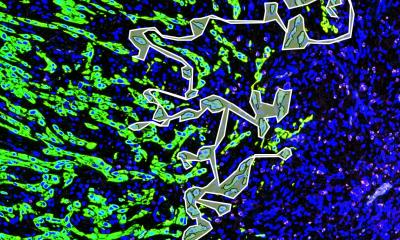
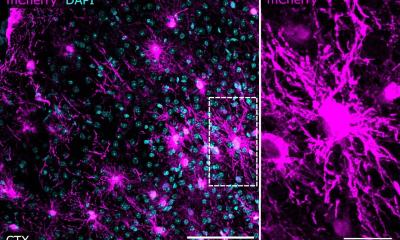
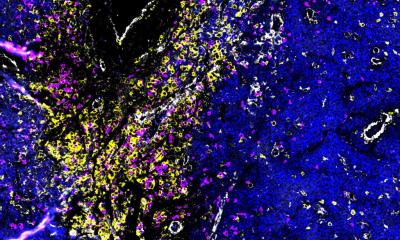
Wissenschaftler des Universitätsklinikums Carl Gustav Carus Dresden im Nationalen Centrum für Tumorerkrankungen Dresden (NCT/UCC) haben gemeinsam mit einem internationalen Forscherteam in Laborversuchen einen bislang unbekannten Überlebensmechanismus im Zellkern besonders aggressiver Tumorzellen entschlüsselt.
Eine wichtige Rolle hierbei spielt das proteinspaltende Enzym Caspase 8, das sich ausschließlich bei aggressiven Krebszellen im Zellkern anreichert. Ließe sich das Enzym an dieser Stelle chemisch hemmen, wäre es denkbar, verschiedene Krebserkrankungen auch in fortgeschrittenen Stadien wirkungsvoll zu bekämpfen.
Die Aufdeckung des Mechanismus bietet daher einen vielversprechenden Ansatz für die Entwicklung neuer zielgerichteter Therapien. Neben dem schwarzen Hautkrebs (malignes Melanom) und Prostatatumoren konnte der entsprechende Mechanismus für weitere Tumorarten, darunter Bauchspeicheldrüsenkrebs, Blasenkrebs, Brustkrebs, Darmkrebs, Eierstockkrebs, Hodenkrebs, Lungenkrebs, Nierenkrebs und Tumoren des Hirns nahegelegt werden. Die Ergebnisse der Untersuchung sind jetzt auf der Website des Fachmagazins „Molecular Cell“ veröffentlicht worden.
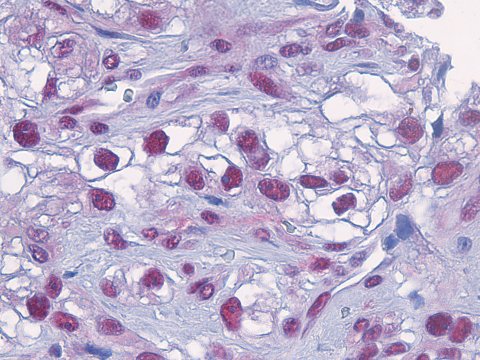
Bildquelle: Institute of Pharmacology University of Bern
Tumorzellen vermehren sich meist besonders schnell und setzen dabei Kontrollmechanismen außer Kraft, mit denen der Körper die Teilung kranker Zellen zu verhindern sucht. Häufig spielen hierbei Mutationen des im Zellkern enthaltenen Proteins p53 eine Rolle, das eine wichtige Kontrollfunktion im Zellzyklus ausübt. Gerade in besonders aggressiven Krebszellen, die bei metastasierenden Tumorerkrankungen wie dem malignen Melanom eine wichtige Rolle spielen, liegt p53 allerdings zumeist in seiner funktionsfähigen Normalform vor. Trotzdem kann es seiner Wächterfunktion offensichtlich nicht nachkommen. Verantwortlich hierfür ist ein bislang unbekannter Mechanismus, der bewirkt, dass der p53-Spiegel im Kern besonders aggressiver Krebszellen zu gering ist, um geschädigte Krebszellen in den programmierten Zelltod – eine Art Selbstmordprogramm der Zelle – zu treiben.
Eine wichtige Rolle in diesem Mechanismus spielt das Enzym Caspase 8, das normalerweise nur im Zytoplasma – der den Zellkern umgebenden Grundsubstanz der Zelle – vorkommt, sich bei aggressiven Krebszellen jedoch im Zellkern anreichert. „Wir konnten erstmals zeigen, dass Caspase 8 im Zellkern ein spezielles Protein – USP28 – spaltet, das dafür verantwortlich ist, den p53-Spiegel in Krebszellen mit erhöhter DNA-Schädigung anzureichern. In der Folge wird p53 zu stark abgebaut und kann seine Kontrollfunktion nicht mehr ausüben. Zellen mit geschädigter DNA werden dann nicht mehr in den programmierten Zelltod getrieben, sondern stattdessen der Zellteilung zugeführt“, erklärt Prof. Dagmar Kulms, Leiterin des Bereichs „Experimentelle Dermatologie“ des NCT/UCC. „Wie wirkungsvoll dieser Mechanismus ist, zeigen die schlechten Überlebensraten von Patienten, bei denen sich eine Anreicherung von Caspase 8 im Zellkern von Tumorzellen nachweisen lässt. Gerade diese Zellen finden sich oft auch gehäuft in der restlichen Tumormasse, die sich bei vielen aggressiven Krebserkrankungen der zunächst erfolgreichen Behandlung entzieht“, sagt Dr. Mads Daugaard vom Vancouver Prostate Centre (Kanada).
Der Mechanismus spielt in einer Vielzahl von Krebsarten eine Rolle. Daher sind unsere Ergebnisse von besonders großer klinischer Relevanz
Stefan Beissert
Die Wissenschaftler konnten den Mechanismus im Labor anhand zahlreicher Zelllinien sowie Patientengewebe für das maligne Melanom und Prostatakrebs belegen. Zum gleichen Ergebnis führten Untersuchungen an Zelllinien weiterer Tumorarten, darunter Bauchspeicheldrüsenkrebs, Blasenkrebs, Brustkrebs, Darmkrebs, Eierstockkrebs, Hodenkrebs, Lungenkrebs, Nierenkrebs und Tumoren des Hirns.
Besonders vielversprechend ist, dass Caspase 8 nur bei besonders aggressiven Krebszellen im Zellkern vorkommt und dort das Protein USP28 spaltet. Ließe sich die Interaktion von Caspase 8 und USP28 mit einem chemischen Wirkstoff hemmen, könnten die aggressiven Tumorzellen künftig sehr gezielt bekämpft werden. „Dies könnte im Idealfall dazu führen, dass bei metastasierten Krebserkrankungen, bei denen heutige Tumortherapien versagen, möglicherweise das Wachstum und die Ausbreitung gestoppt werden könnten. Der Mechanismus spielt in einer Vielzahl von Krebsarten eine Rolle. Daher sind unsere Ergebnisse von besonders großer klinischer Relevanz“, sagt Prof. Stefan Beissert, Direktor der Klinik für Dermatologie des Universitätsklinikums Dresden. Gemeinsam mit spezialisierten Chemikern wollen die Wissenschaftler künftig an einem entsprechenden Wirkstoff forschen.
Quelle: Nationales Centrum für Tumorerkrankungen Dresden (NCT/UCC)
23.01.2020