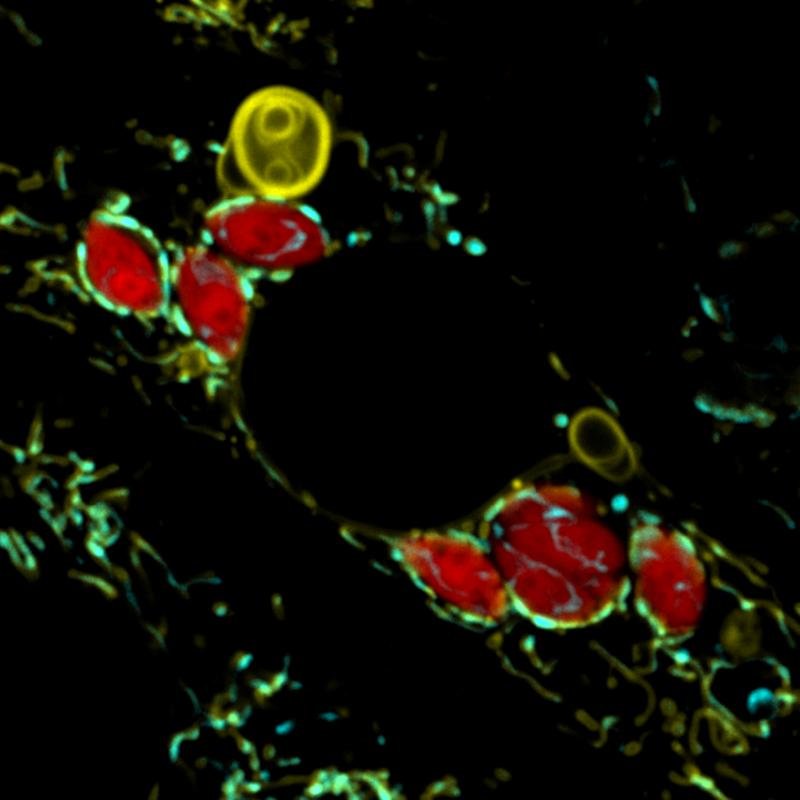
Quelle: © MPI für Biologie des Alterns/ Xianhe Li
News • Feindliche Übernahme
Krankheitserreger kapern Mitochondrien des Wirts
Mitochondrien sind bekannt dafür, Energie für unsere Zellen zu liefern, aber sie spielen auch eine wichtige Rolle bei der Abwehr von Krankheitserregern. Sie können Immunreaktionen auslösen und Krankheitserregern die Nährstoffe entziehen, die diese für ihr Wachstum benötigen. Ein Forschungsteam vom Max-Planck-Institut für Biologie des Alterns hat nun gezeigt, dass Krankheitserreger die mitochondrialen Abwehrmechanismen ausschalten können, indem sie eine normale zelluläre Reaktion auf Stress aushebeln.
Um zu überleben, müssen Krankheitserreger nicht nur die Abwehrmechanismen des Wirts ausschalten, sondern auch, wenn sie in die Zelle eingedrungen sind, Nährstoffe von ihrem Wirt beziehen. Eine dieser Abwehrmechanismen kommt von den Mitochondrien des Wirts, die den Erregern die benötigten Nährstoffe entziehen und so ihr Wachstum einschränken. "Wir wollten wissen, wie sich das Verhalten der Mitochondrien sonst noch verändert, wenn Mitochondrien und Krankheitserreger in der Zelle aufeinandertreffen. Da die äußere Membran dieser Organellen der erste Kontaktpunkt mit den Eindringlingen ist, haben wir uns diese genauer angeschaut", erklärt Lena Pernas, Forschungsgruppenleiterin am Max-Planck-Institut für Biologie des Alterns.
Mitochondrien stoßen ihre "Haut" ab
Die Forschenden infizierten Zellen mit dem menschlichen Parasiten Toxoplasma gondii und beobachteten live unter dem Mikroskop, was mit der äußeren Membran der Mitochondrien passiert. "Wir sahen, dass Mitochondrien, die mit dem Parasiten in Kontakt kamen, große Strukturen von ihrer äußeren Membran ablösten. Das war für uns sehr rätselhaft. Warum sollten Mitochondrien das abstoßen, was im Grunde das Bindeglied zwischen ihnen und dem Rest der Zelle ist?", sagt Xianhe Li, Erstautor der Studie.
Aber wie bringt der Parasit die Mitochondrien dazu, dies zu tun? Das Forschungsteam konnte zeigen, dass der Erreger über ein Protein verfügt, das ein mitochondriales Wirtsprotein nachahmt. Es bindet an einen Rezeptor auf der äußeren Membran der Mitochondrien, um Zugang zu der Maschinerie zu erhalten, die dafür sorgt, dass Proteine in Mitochondrien importiert werden. "Auf diese Weise kapert der Parasit eine normale Reaktion des Wirts auf mitochondrialen Stress. Dies führt zu einer Entwaffnung der Mitochondrien", so Pernas. "Andere Forschende haben gezeigt, dass ein Protein des SARS-CoV-2-Virus ebenfalls an diesen Transportrezeptor bindet. Dies deutet darauf hin, dass der Rezeptor eine wichtige Rolle bei der Interaktion zwischen Wirt und Krankheitserreger spielt. Es sind jedoch weitere Untersuchungen erforderlich, um seine Rolle bei verschiedenen Infektionen besser zu verstehen.“
Die Studie wurde in Science veröffentlicht.
Quelle: Max-Planck-Institut für Biologie des Alterns
17.01.2022