News • Forschung
Gen-Reparatur: Schafft ein neuer Ansatz, woran CRISPR scheitert?
Der große Hype um die sogenannte "Genschere" CRISPR/Cas ist mittlerweile einer gewissen Ernüchterung gewichen, denn bei der praktischen Anwendung der DNA-Reparatur gibt es unerwartete Hürden. Forscher aus Heidelberg haben jetzt einen neuen Ansatz entdeckt, der diesen Makel beheben könnte.
Mit der molekulargenetischen Methode CRISPR/Cas können Brüche in der DNA-Doppelhelix und damit zufällige Mutationen in jedem Zielgen ausgelöst werden. Die exakte Reparatur eines Gens mithilfe einer Reparaturkopie war bislang äußerst aufwändig, doch nun haben Forscher der Universität Heidelberg eine Lösung gefunden: Mit einem neuen Ansatz haben sie die Grundlage geschaffen, um auf einfache Weise die Reparaturkopie eines defekten Gens in die DNA einzuschleusen. Wie der Entwicklungsbiologe Prof. Dr. Joachim Wittbrodt erläutert, ist mit diesem effizienten Verfahren die präzise Geneditierung in der Grundlagenforschung möglich, und eine Anwendung im therapeutischen Bereich rückt damit ein großes Stück näher. Die Forschungsergebnisse wurden in „eLife“ veröffentlicht.
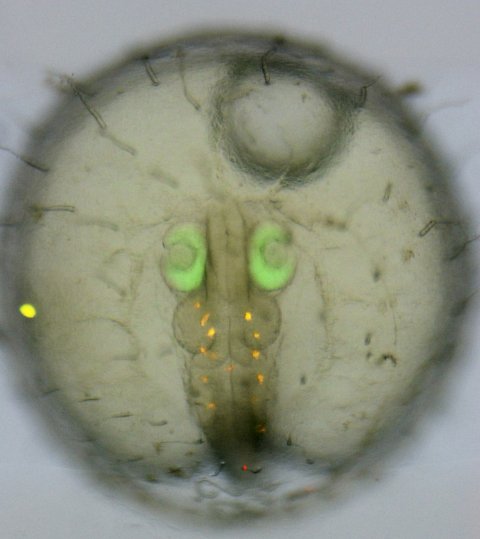
Bei der Geneditierung muss zunächst im Genom punktgenau die Stelle gefunden und angesteuert werden, bei der eine Genmutation ausgelöst werden soll. Dazu wird eine „Sonde“ konstruiert. Sie besteht aus RNA-Abschnitten, die der DNA-Abfolge der jeweiligen Zielsequenz entspricht. Diese „Sonde“ dockt an der gewünschten Stelle der DNA an, um dort den Doppelstrang mit der molekularen „Schere“ CRISPR/Cas zu durchschneiden. Anschließend tritt das zelleigene Reparatursystem in Aktion. Bei der Reparatur dieser künstlich hergestellten Bruchstellen können einzelne DNA-Bausteine verloren gehen. Auf diese Weise kommt es in ausgesuchten Zielgenen zu Veränderungen, die jedoch dem Zufall überlassen sind. In praktisch jedem untersuchten Organismus konnte diese Methode erfolgreich angewendet werden, wie Prof. Wittbrodt vom Centre for Organismal Studies der Universität Heidelberg erläutert.
Eine Utopie blieb bislang jedoch das routinemäßige präzise Editieren, das zu genau definierten Modifikationen beliebiger Gene führt. Nach den Worten von Dr. Arturo Gutierrez liegt dies ausgerechnet am zelleigenen Reparatursystem, das die Brüche im DNA-Doppelstrang rasch wieder schließt. Während dieser Mechanismus mit der Bezeichnung „Non-Homologous End Joining“ (NHEJ) für das effiziente Erzeugen zufälliger Genveränderungen kein Problem darstellt, konkurriert NHEJ mit einem zweiten, hoch präzise arbeitenden Reparaturverfahren namens „Homology Directed Repair“ (HDR). Wie beim Einsetzen eines Ersatzteils müssen hierbei beide Enden perfekt passen, damit HDR das defekte Gen durch die korrekte Reparaturkopie ersetzen kann. „Unglücklicherweise verbindet NHEJ diese in die Zellen eingebrachten Kopien in große zusammenhängende Ketten und macht sie damit unbrauchbar“, so Tinatini Tavhelidse.
Dieses kostengünstige Verfahren erlaubt nun eine effiziente Reparatur von Genen, indem es das passgenaue Einsetzen einer einzelnen Reparaturkopie ermöglicht
Thomas Thumberger
Das Team von Prof. Wittbrodt hat jetzt am japanischen Reisfisch Medaka einen neuen Ansatz entwickelt und überprüft, der die präzise Genreparatur mit hoher Effizienz ermöglicht und damit eine Grundvoraussetzung für die Anwendung in der Genchirurgie darstellt. Dabei folgten die Heidelberger Wissenschaftler einer einfachen Idee: Anstatt pharmakologische Wirkstoffe mit starken Nebenwirkungen zu verwenden, um die ungewollten Effekte des NHEJ abzuschwächen, veränderten sie die Reparaturkopie derart, dass sie nicht „angegriffen“ und damit unbrauchbar gemacht werden kann. Die beiden Enden der Kopie werden durch Biotin – ein Vitamin B – blockiert, um das „Non-Homologous End Joining“ zu verhindern. „Dieses kostengünstige Verfahren erlaubt nun eine effiziente Reparatur von Genen, indem es das passgenaue Einsetzen einer einzelnen Reparaturkopie ermöglicht“, betont Dr. Thomas Thumberger.
Quelle: Universität Heidelberg
30.08.2018