© MedUni-Wien / LBI Trauma
Artikel • Natürliches Biomaterial "CartiScaff"
Die Kunst der Knorpelregeneration
Mit Knorpelmatrix aus natürlichem Biomaterial haben Wiener Forscher Gelenkknorpel dazu gebracht, wieder zu regenerieren.
Bericht: Michael Krassnitzer
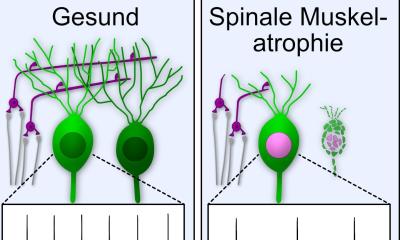
Gelenkknorpel kann unter normalen Umständen nur in äußerst geringem Ausmaß von selbst regenerieren. Die Knorpelmatrix, das Gerüst des Knorpelgewebes, beherbergt nur sehr wenige Zellen und diese befinden sich meist tief im inneren der Matrix. Außerdem ist Gelenkknorpel extrem isoliert: In der direkten Umgebung gibt es keine regenerativen Zellen, die in den Defekt einwandern und diesen reparieren könnten; es gibt auch keine Blutgefäße, über die regenerative Zellen an den Knorpel gelangen könnten. Aus diesem Grund verfolgen Forscher weltweit verschiedene experimentelle Ansätze, bei denen Biomaterial in das Gelenk eingebracht wird, um damit eine Knorpelregeneration herbeizuführen.

Foto © MedUni Wien/feelimage
Einer Forschungsgruppe der Medizinischen Universität Wien (Universitätsklinik für Orthopädie und Unfallchirurgie) ist es nun in präklinischen Studien gelungen, mit Knorpelmatrix als Biomaterial eine erstaunlich gute Regeneration von Gelenkknorpel zu erreichen. Die verwendete Matrix stammt von operativ versorgten Patienten, die ihr Einverständnis zur wissenschaftlichen Untersuchung ihres Gewebes gegeben haben. Abgesehen davon, dass alle von Spendern stammenden Knorpelzellen aus der Matrix entfernt werden, handelt es sich um natürliches Knorpelgewebe aus Kollagen-II-Fasern und Glykosaminoglykanen. Dieses „CartiScaff“ genannte Material wird an die defekte Stelle im Gelenk eingebracht, um dort eine optimale Umgebung für Knorpel- oder Stammzellen zu schaffen.
Die Forscher veröffentlichten ihre Arbeit jetzt im Lancet-Journal EBioMedicine.
„Die Kunst dabei ist es, die körpereigenen Zellen in das Gewebe hineinzubekommen“, erklärt Priv.-Doz. Dr. Sylvia Nürnberger, die das Projekt leitet: „Knorpelzellen sind nämlich essentiell für den Erhalt des Knorpels.“ Knorpelzellen bauen Kollagen II auf und müssen auf unterschiedliche Belastungen reagieren; Knorpelmatrix ohne Zellen würde im Laufe der Zeit dem Verschleiß um Opfer fallen. „Knorpelzellen halten den Knorpel instand. Sie sind sozusagen die Hausmeister des Knorpels“, vergleicht die Wissenschaftlerin.
Laser schafft Eingangstore für Helferzellen
Aufgrund der Ähnlichkeit des Biomaterials mit natürlichem Knorpel ist es dazu geeignet, als Teil des Regeneratgewebes im Defekt zu verbleiben, oder aber abgebaut und von neuer Matrix ersetzt zu werden
Sylvia Nürnberger
Um die Zellen in die Matrix hineinzubekommen, wird diese mit einem feinen Laser perforiert, der ansonsten zur Korrektur von Fehlstellungen im Ohr oder bei Linsenkorrekturen im Auge eingesetzt wird. In geringstem Abstand werden kontrolliert und standardisiert feine Einkerbungen gesetzt. Auf diese Weise werden auch tiefere Geweberegionen für regenerative Zellen zugänglich. Diese können auf drei Arten an die Matrix gebracht werden: Entweder wird ein Loch bis zum Knochenmark gebohrt, durch das Stammzellen in den Defekt einströmen oder es wird zugleich mit der Matrix vom Beckenkamm stammendes Knochenmark in das Gelenk eingebracht; die Stammzellen entwickeln sich dann zu Knorpelzellen. Die dritte Variante: die Matrix wird bereits vor der Implantation mit Stamm- oder Knorpelzellen besiedelt.
© MedUni-Wien / LBI Trauma
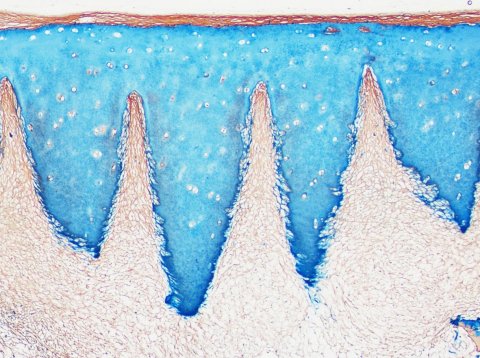
Die mit dem Laser produzierten Einkerbungen bieten einen weiteren Vorteil: Sie verschaffen dem Knorpelgewebe eine gewisse Flexibilität, so dass es sich den Rundungen des Gelenkknochens besser anpassen kann – vergleichbar mit der Beweglichkeit einer Ziehharmonika, wie Nürnberger erläutert. „Das Knorpelgewebe, das sich in diesen Einschnitten bildet, ist für ein regeneriertes Gewebe von erstaunlich guter Qualität“, resümiert die Forscherin: Die Kollagen-II-Fasern sind vertikal zum Knochen ausgerichtet, auch die Oberfläche wird vom Implantat/Biomaterial gebildet und entspricht daher der Struktur von natürlichem Knorpel. „Aufgrund der Ähnlichkeit des Biomaterials mit natürlichem Knorpel ist es dazu geeignet, als Teil des Regeneratgewebes im Defekt zu verbleiben, oder aber abgebaut und von neuer Matrix ersetzt zu werden“, erklärt Nürnberger: „Folgestudien werden darüber Auskunft geben, wie sich die Implantate über einen längeren Zeitraum entwickeln.“
Profil:
Priv.-Doz. Dr.rer.nat Sylvia Nürnberger ist Biologin und Leiterin der Arbeitsgruppe für experimentelle Knorpelregeneration im Forschungslabor der Abteilung für Unfallchirurgie an der Medizinischen Universität Wien und ist an den Aktivitäten des Österreichischen Clusters für Geweberegeneration beteiligt. Der besondere Schwerpunkt ihrer Arbeit liegt auf Biomaterialien und alternativen Zelltherapien. Sie entwickelte und patentierte Biomaterialien auf der Basis natürlicher Ressourcen und konzentrierte sich insbesondere auf die translationale Forschung, mit dem Ziel grundlegende Kenntnisse und Entwicklungen bis in den klinischen Bereich umzusetzen und sie der medizinischen Infrastruktur und den Patienten zugänglich zu machen.
16.02.2021