News • Potentielles Mittel gegen Coronavirus
Deutschland genehmigt erste klinische Prüfung von COVID-19-Impfstoff
Das Paul-Ehrlich-Institut, Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel, hat die erste klinische Prüfung eines Impfstoffs gegen COVID-19 in Deutschland genehmigt.
Bildquelle: U.S. Department of Health and Human Services - National Institutes of Health (NIH)
Die Genehmigung ist das Ergebnis einer sorgfältigen Bewertung des potenziellen Nutzen-Risiko-Profils des Impfstoffkandidaten. Durch eine intensive wissenschaftliche Beratung des Arzneimittelentwicklers BioNTech im Vorfeld konnte das Paul-Ehrlich-Institut das Verfahren in vier Tagen abschließen. Die Erprobung von Impfstoffkandidaten am Menschen ist ein wichtiger Meilenstein auf dem Weg zu sicheren und wirksamen Impfstoffen gegen COVID-19 für die Bevölkerung in Deutschland und darüber hinaus.
Die Bereitstellung zugelassener sicherer und wirksamer COVID-19-Impfstoffe ist ein zentrales Ziel der Bekämpfung des grassierenden neuen SARS-Coronavirus-2 (SARS-CoV-2). Erste klinische Prüfungen haben das Ziel, die generelle Verträglichkeit von Impfstoffkandidaten und ihre Fähigkeit zu ermitteln, eine spezifische Immunantwort gegen den Erreger zu erzeugen. Das für die Genehmigung klinischer Prüfungen sowie die Bewertung und Zulassung von Impfstoffen in Deutschland zuständige Paul-Ehrlich-Institut unterstützt die COVID-19-Impfstoffentwicklung mit höchster Priorität. Mit seiner frühen und umfassenden wissenschaftlichen Beratung wird erreicht, dass die Impfstoffentwicklung zielgerichtet beschleunigt wird und trotzdem die notwendigen wissenschaftlichen Anforderungen erfüllt werden. Denn das Paul-Ehrlich-Institut betrachtet es als eine seiner zentralen Aufgaben, die klinische Entwicklung von COVID-19-Impfstoffen zur Prävention und von biomedizinischen Arzneimitteln zur Therapie regulatorisch zu unterstützen, um eine zeitnahe Verfügbarkeit dieser Arzneimittel zu ermöglichen. Dabei wird darauf geachtet, dass die erforderliche Sorgfalt nicht beeinträchtigt wird.
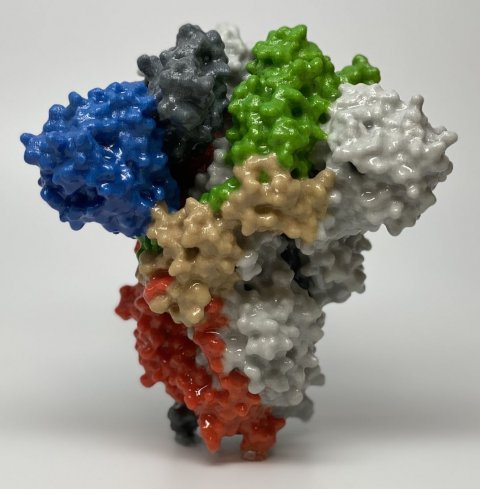
Bildquelle: U.S. Department of Health and Human Services - National Institutes of Health (NIH)
Bei dem Impfstoffkandidaten des Mainzer Biotechnologieunternehmens BioNTech handelt es sich um einen sogenannten RNA-Impfstoff, der die genetische Information für den Bau des sogenannten Spikeproteins des CoV-2 oder Teilen davon in Form der Ribonukleinsäure (RNA) enthält. Im genehmigten ersten Teil der klinischen Prüfung werden 200 gesunde Probanden im Alter von 18 bis 55 Jahren mit jeweils einer von mehreren gering modifizierten Impfstoffvarianten geimpft. Nach einer Wartezeit zur Beobachtung der Geimpften werden im zweiten Teil der klinischen Prüfung weitere Probanden der gleichen Altersspanne geimpft. Der zusätzliche Einschluss von Probanden mit erhöhtem Infektionsrisiko oder mit erhöhtem Risiko für einen schweren Verlauf einer COVID-19-Erkrankung ist im zweiten Teil der klinischen Prüfung vorgesehen, für die vorab weitere Studiendaten eingereicht werden müssen.
In dem genehmigten Teil der klinischen Prüfung werden verschiedene Varianten des RNA-Impfstoffkandidaten geprüft. Neben der Verträglichkeit wird die Fähigkeit zur Erzeugung einer Immunantwort auf SARS-CoV-2 nach Gabe einer bestimmten RNA-Menge (Dosis) untersucht (erste Dosisfindung). Dabei werden unterschiedliche RNA-Typen und unterschiedliche Längen und Modifikationen des Spikeproteins getestet sowie der Einfluss einer zweiten Impfung geprüft. Weltweit ist dies erst die vierte genehmigte Prüfung von präventiven, spezifischen COVID-19-Impfstoffkandidaten am Menschen. Angesichts der schwerwiegenden Folgen der COVID-19-Pandemie ist dies ein bedeutender Schritt, um einen wirksamen und sicheren COVID-19-Impfstoff möglichst zeitnah in Deutschland zu entwickeln und möglichst weltweit verfügbar zu machen.
Das Paul-Ehrlich-Institut geht nach derzeitigem Erkenntnisstand davon aus, dass weitere klinische Prüfungen von COVID-19-Impfstoffkandidaten in Deutschland in den nächsten Monaten beginnen werden. Für die Bekämpfung der Pandemie werden mehrere Impfstoffprodukte notwendig sein, um eine ausreichende Versorgung sicherzustellen.
Quelle: Paul-Ehrlich-Institut
22.04.2020