News • Pathogenes Wachstum bremsen
Alzheimer, Parkinson & Co. bei den Fibrillen packen
Bei einer Reihe von Erkrankungen stehen miteinander verklebte Eiweißbausteine, sogenannte Fibrillen, als Verursacher in dringendem Verdacht. Ein Team von Biophysikern der Heinrich-Heine-Universität Düsseldorf (HHU) und des Forschungszentrums Jülich hat sich damit beschäftigt, wie das Wachstum dieser pathogenen Fibrillen gehemmt werden kann.
In einer Online-Veröffentlichung von Chemical Science beschreiben sie ein spezielles Molekül, welches die Enden der Fibrillen verkleben kann.
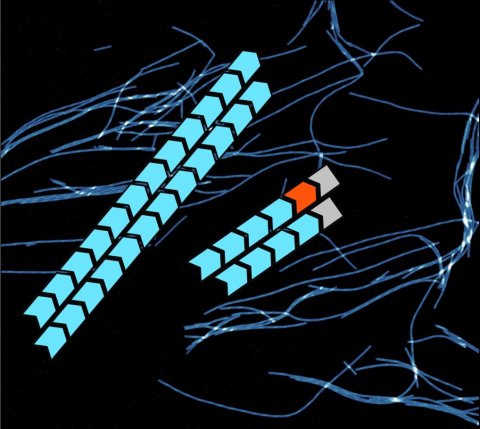
© HHU / Emil Agerschou
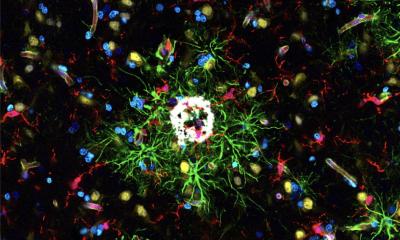
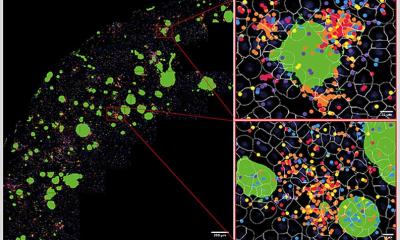
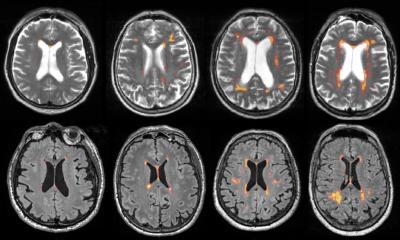
Sogenannte Amyloidfibrillen sind die Bausteine von Proteinplaques, die bei vielen, insbesondere neurodegenerativen Erkrankungen gefunden werden. Sie gelten als Ursache zum Beispiel für Parkinson, die Lewy-Body- oder die Alzheimer-Demenz, aber auch Diabetes. Bei Parkinson und der Lewy-Body-Demenz entstehen diese Fibrillen, wenn mehrere einzelne körpereigene Proteine des Typs α-Synuclein – sogenannte Monomere – miteinander verkleben.
Ein Ansatzpunkt für die Entwicklung von Therapeutika ist, die Enden der Fibrillen zu blockieren, so dass dort keine weiteren Monomere mehr angebaut werden können. Bereits in früheren Arbeiten sind Kandidaten für Moleküle gefunden worden, die dies erreichen können. Die Arbeitsgruppe um Jun.-Prof. Dr. Wolfgang Hoyer vom Institut für Physikalische Biologie der HHU hat untersucht, wie diese Inhibitor-Moleküle funktionieren. Sie untersuchten dazu eine Variante des α-Synuclein, die eine Art Knick im Molekül aufweist und die bereits in einer früheren Publikation beschrieben wurde. In ihrer neuen Studie zeigte das Forschungsteam, dass dieser spezielle Inhibitor sich so fest an das Ende von Fibrillen anlagert, dass keine weiteren α-Synuclein-Monomere dort angebaut werden können. Zusätzlich umlagern einige zusätzliche dieser Monomere das so präparierte Fibrillenende und blockieren damit komplett das weitere Wachstum.
Darüber hinaus konnte dieser Vorgang auch mathematisch beschrieben werden, und zwar mit einem Modell, das für die Inhibition von Enzymen entwickelt worden ist (Michaelis-Menten-Modell). Bei der Anwendung spielt das Ende der Fibrille die Rolle des Enzyms, das einzubauende Monomer diejenige des Substrats, welches das Enzym normalerweise verändert. „Während das α-Synuclein-Monomer im Körper eine biologische Funktion hat, ist die Fibrille für uns nutzlos, sogar schädlich“, so Prof. Hoyer, und weiter: „Kann man durch den Einbau des Inhibitors an eine Fibrille deren weiteres Wachstum verhindern, so hemmt man nicht nur ihre toxische Wirkung, sondern fördert auch die normale Funktion des α-Synuclein-Monomers, welches ansonsten dem Körper verloren ginge.“
Die Forschungen zeigen einen Weg auf, wie man möglicherweise Therapeutika optimieren kann, die auf das Verkleben der Fibrillenenden abzielen, indem die Wirkung der Verklebung verstärkt wird.
Quelle: Heinrich-Heine-Universität Düsseldorf (HHU)
22.10.2020