© RUB, Marquard
News • Entstehung der Erkrankung
Parkinson: Neue Einblicke in die "zelluläre Müllabfuhr"
NEMO, ein Protein, das vor allem für seine Rolle bei Signalprozessen im Immunsystem bekannt ist, verhindert die Ablagerung von Proteinaggregaten, wie sie bei der Parkinson-Erkrankung auftreten.
Es dockt dafür an bestimmte Proteinketten an, die als Kennzeichnung für die zelluläre Müllabfuhr dienen, und fördert so den Abbau der schädlichen Aggregate. Ein Forschungsteam unter Federführung von Prof. Dr. Konstanze Winklhofer von der Ruhr-Universität Bochum hat diesen Mechanismus aufgeklärt und berichtet in der Zeitschrift Nature Communications. In weiterführenden Studien untersucht das Team, wie die Erkenntnisse für therapeutische Strategien genutzt werden können.
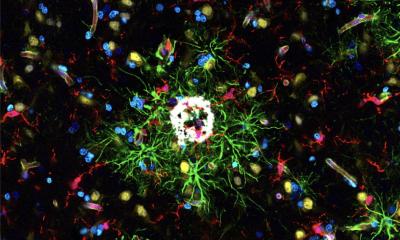
Neurodegenerative Erkrankungen, wie die Parkinson- oder Alzheimer-Erkrankung, gehen einher mit der Ablagerung von Proteinaggregaten im Gehirn. Diese Aggregate häufen sich an, wenn die zelluläre Müllabfuhr defekt oder überlastet ist. Bei der Parkinson-Erkrankung finden sich in bestimmten Gehirnregionen Aggregate, die vorwiegend aus dem Protein ⍺-Synuclein bestehen. „Das Vorhandensein solcher Aggregate, die auch Lewy-Körperchen genannt werden, ist ein wesentliches Merkmal der Parkinson-Erkrankung“, erklärt Konstanze Winklhofer.
Unsere biochemische und zellbiologische Charakterisierung der NEMO-Variante zeigte, dass diese nicht an lineare Ubiquitin-Ketten binden und somit nicht an Proteinaggregate andocken kann
Konstanze Winklhofer.
Die Fehlfaltung und Zusammenlagerung von ⍺-Synuclein ist von zentraler Bedeutung für Prozesse, die zum Funktionsverlust und Absterben von Nervenzellen führen und zum Fortschreiten der Erkrankung beitragen. Daher arbeiten weltweit Forschende aus verschiedenen Disziplinen daran, diese Prozesse auf zellulärer und molekularer Ebene zu entschlüsseln, um zielgerichtete therapeutische Ansätze entwickeln zu können.
Der Bochumer Arbeitsgruppe ist es in Zusammenarbeit mit einem interdisziplinären Team gelungen, den Mechanismus des ⍺-Synuclein-Abbaus besser zu verstehen: Zelluläre Proteine, die für den Abbau bestimmt sind, werden mit einer Markierung versehen, sodass die zelluläre Müllabfuhr diese Proteine identifizieren kann. Diese Markierung besteht aus einer Kette von kleinen Ubiquitin-Molekülen. „Je nach Art der Verknüpfung dieser Ubiquitin-Moleküle und der Länge und Struktur der Ubiquitin-Ketten kann die zelluläre Müllabfuhr erkennen, über welche Prozesse die markierten Proteine abgebaut werden sollen“, so Konstanze Winklhofer.
Vorarbeiten der Arbeitsgruppe haben gezeigt, dass eine seltene Form von Ubiquitin-Ketten, sogenannte lineare Ubiquitin-Ketten, an Proteinaggregaten in Nervenzellen angereichert werden und die Toxizität der Proteinaggregate reduzieren. Nun konnten die Forschenden den Mechanismus dieser Schutzwirkung aufklären. Es zeigte sich, dass das Protein NEMO an lineare Ubiquitin-Ketten auf den Proteinaggregaten andockt und den Abbau von ⍺-Synuclein fördert. „Interessanterweise kann der Schutzeffekt von NEMO blockiert werden, indem man die Autophagie hemmt“, berichtet Winklhofer. Autophagie ist eine wichtige Komponente der zellulären Müllabfuhr, bei der abzubauendes Material in membranumschlossene Vesikel verpackt wird, die dann mit Lysosomen verschmelzen. Lysosomen sind kleine Zellorganellen, die verschiedene Enzyme für den Abbau von Biomolekülen enthalten.
Die Arbeitsgruppe von Konstanze Winklhofer entdeckte, dass NEMO mit einem Protein der Autophagie-Maschinerie interagiert. Die Bildung eines Komplexes aus linearen Ubiquitin-Ketten, NEMO und diesem Protein namens p62 an den ⍺-Synuclein-Aggregaten erlaubt eine Anordnung von p62 in Form von Kondensaten – eine Voraussetzung für die effiziente Rekrutierung der Autophagie-Maschinerie an Proteinaggregate.
„Ein wegweisendes Ereignis im Laufe dieser Untersuchungen war ein Gespräch mit Neurologen der Universität von San Francisco, die mich wegen eines interessanten Falls kontaktiert hatten“, sagt Konstanze Winklhofer. Die US-Kollegen betreuten eine Patientin mit einer progressiv verlaufenden Parkinson-Erkrankung, die bereits mit Anfang 40 erkrankte. Daher wurde eine genetische Untersuchung durchgeführt, die ergab, dass diese Patientin eine seltene Mutation im NEMO-Gen aufweist. „Unsere biochemische und zellbiologische Charakterisierung der NEMO-Variante zeigte, dass diese nicht an lineare Ubiquitin-Ketten binden und somit nicht an Proteinaggregate andocken kann.“ Der Funktionsverlust von NEMO führt dazu, dass die Bildung von p62-Kondensaten an ⍺-Synuclein-Aggregaten beeinträchtigt und deren Abbau gestört ist.
Tatsächlich war im Gehirn der Patientin mit der NEMO-Mutation eine ausgeprägte Ablagerung von ⍺-Synuclein-Aggregaten zu sehen. „Interessanterweise waren auch andere Proteinaggregate nachweisbar, wie sie beispielsweise bei der Alzheimer-Erkrankung auftreten“, so Konstanze Winklhofer. „Dies erklärt den schwerwiegenden Verlauf der NEMO-assoziierten Erkrankung und untermauert eine generelle Rolle von NEMO bei der Qualitätskontrolle von aggregierten Proteinen.“
In weiterführenden Studien untersucht das Forschungsteam, wie NEMO und lineare Ubiquitin-Ketten für neue therapeutische Strategien genutzt werden können.
Quelle: Ruhr-Universität Bochum
21.12.2023