ALS
Neue Auslöser für eine schwere Krankheit
Bei der Suche nach den Ursachen der Amyotrophen Lateralsklerose (ALS) hat ein internationales Konsortium zwei neue Krankheitsgene entdeckt. An der Arbeit beteiligt waren Wissenschaftler vom Institut für Klinische Neurobiologie des Würzburger Universitätsklinikums.
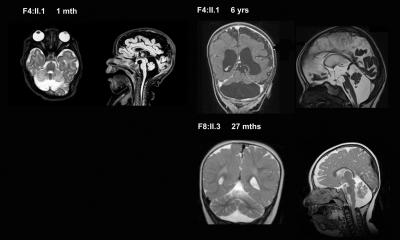
Die Amyotrophe Lateralsklerose ist eine schwere neurologische Erkrankung, die mit Muskelschwund und Lähmungen an Armen und Beinen beginnt. Die Lähmungen schreiten auf die gesamte Muskulatur einschließlich der Atemmuskulatur fort, und die Erkrankung führt so in der Regel innerhalb weniger Jahre zum Tod. Weltweit ist 1 von 400 Personen betroffen. Berühmte Patienten, wie der Astrophysiker Stephen Hawking oder der Maler Jörg Immendorf, der im Mai 2007 an den Folgen dieser Krankheit starb, haben sie in der Öffentlichkeit bekannt gemacht.
Acht Millionen genetische Variationen
Bei der Suche nach Auslösern dieser Krankheit ist jetzt ein internationales Team von Wissenschaftlern mit Würzburger Beteiligung fündig geworden. In die Studie eingeschlossen waren mehr als 15.000 Patienten mit ALS und 26.000 gesunde Teilnehmer zur Kontrolle. Mehr als acht Millionen genetische Variationen haben die Forscher im Erbgut der Studienteilnehmer gefunden, die über das ganze Genom verteilt waren. Zwei, bislang unbekannte Genvariationen konnten sie darunter identifizieren, die mit einem hohen Risiko für die Amyotrophe Lateralsklerose assoziiert sind.
Eine Arbeitsgruppe unter der Leitung von Jan Veldink an der Universität Utrecht, Niederlande, identifizierte das C21ORF2 Gen als neues Risikogen; eine weitere Gruppe unter der Leitung von John Landers, University of Massachusetts Medical School, Worchester, USA identifizierte das Gen für die NEK1 Kinase als Risikogen. Beide Arbeiten wurden in der Zeitschrift Nature Genetics am 25. Juli 2016 veröffentlicht.
Langjährige Forschung in Würzburg
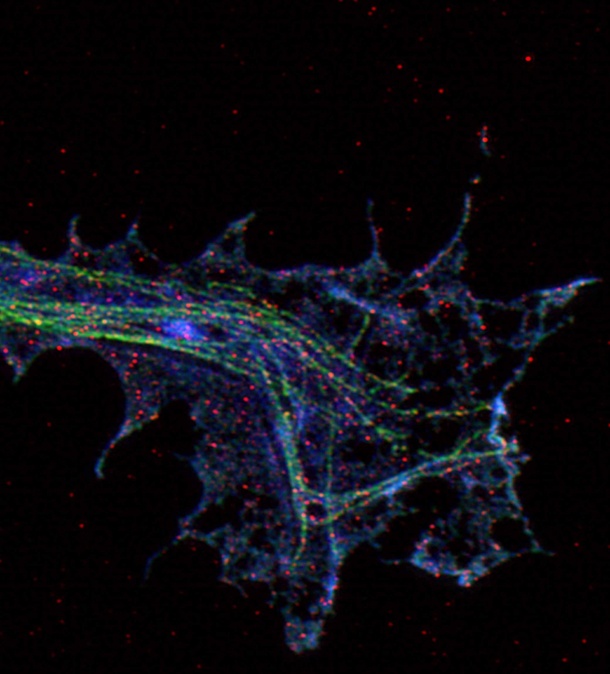
„Diese Mutationen bestätigen vorangegangene Arbeiten der Würzburger Arbeitsgruppe am Institut für Klinische Neurobiologie“, sagt Professor Michael Sendtner, Inhaber des Lehrstuhls für Klinische Neurobiologie und Leiter des Instituts. Dort wird schon seit Jahren an den Ursachen für das unaufhaltsame Absterben der Nervenzellen geforscht. Im Mittelpunkt stehen Mechanismen, die die Stabilität und das Wiederauswachsen von feinsten Strukturen, sogenannten Mikrotubuli, in den für Bewegung verantwortlichen Motoneuronen regulieren. Der NEK1 Kinase kommt dabei eine zentrale Rolle zu.
„Die NEK1 Kinase ist ein wichtiger Regulator für die Dynamik von Mikrotubuli, die die axonalen Verbindungen in motorischen Nervenzellen stabilisieren“, erklärt Michael Sendtner. Mikrotubuli sind mitverantwortlich für die Stabilität der Zelle und deren Form sowie den Transport von wichtigen Zellbestandteilen wie Proteinen und Mitochondrien zwischen dem Zellkörper und der neuromuskulären Synapse, die die Übertragung der Aktivität auf die Muskelzellen vermittelt. „Kommt es zur Störung in Mikrotubuli, degenerieren die Nervenzell-Fortsätze. Dann ist es nur eine Frage der Zeit, bis die gesamte Zelle stirbt“, so der Wissenschaftler. NEK1 organisiert die Bildung neuer Mikrotubuli.
Ansatz für neue Therapien
Darüber hinaus konnten die Wissenschaftler bereits 2014 zeigen, dass sogenannte neurotrophe Faktoren wie etwa der Ciliary Neurotrophic Factor (CNTF) die Mikrotubuli-Stabilität beeinflussen. Diese Faktoren stimulieren einerseits die Nervenzelldifferenzierung, andererseits sind sie für das Überleben von Nervenzellen mitverantwortlich. Involviert ist dabei ein Signalmolekül mit dem Namen STAT-3. Dieses Signalmolekül interagiert mit Stathmin, einem Molekül, das Mikrotubuli destabilisieren kann.
Stathmin wiederum interagiert mit anderen Filamenten im Axon, den Neurofilamenten. Diese bilden Aggregate in Axonen von ALS-Patienten wie auch bei anderen neurodegenerativen Erkrankungen, beispielsweise bei Morbus Alzheimer, und diese Aggregate destabilisieren die Mikrotubuli. „Die Blockade von Stathmin mit Hilfe spezieller Wirkstoffe bietet sich somit als Ansatz für neue Therapien bei Motoneuronerkrankungen, und eventuell auch bei anderen neurodegenerativen Erkrankungen an“, so Michael Sendtner.
Publikationen:
- Novel risk variants and genetic architecture in amyotrophic lateral sclerosis. Nature Genetics. 2016. DOI: 10.1038/ng.1622
- NEK1 identified as novel risk gene in ALS. Nature Genetics. 2016.DOI:10.1038/ng.3626
- Neurofilament depletion improves microtubule dynamics via modulation of Stat3/stathmin signaling. Acta Neuropathol. 2016. DOI: 10.1007/s00401-016-1564-y
- Local axonal function of STAT3 rescues axon degeneration in the pmn model of motoneuron disease. The Journal of Cell Biology. 2014. DOI: 10.1083/jcb.201203109
Quelle: Julius-Maximilians-Universität Würzburg
02.08.2016